Протеини - амфотерни електролити Yermolaev 1974 m
Протеини - амфотерни електролити
При изучаване на химичния състав на протеин е установено, че в молекулата има свободен амин (NH2) и карбокси (СООН) групи, които са в разтвор под формата на NH3 и СООН. Следователно, в разтвора протеини имат амфотерни свойства (ampholyte, Amphion). Когато електрическият ток преминава протеини ще се движат в зависимост от заряда на протеиновите молекули на катода или анода (фиг. 10).
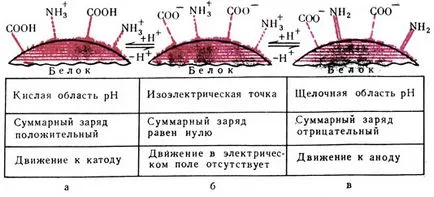
Фиг. 10. Протеини - амфотерно съединение. и - в киселинен разтвор, общият заряд на протеин и протеина става положително катион; б - изоелектричната точка; общият заряд на молекулата на протеин е равна на нула; в - в алкална среда потиска дисоциация на аминни групи. Зареждането на протеинови молекули е отрицателно и протеинът се премества към анода (анион играе ролята на протеин)
В алкални разтвори, протеин действа като анион: например, е налице загуба на Н + NH + 3 чрез действието на натриев хидроксид.
В киселинни разтвори, напротив, протеинът действа като катион, както в случая на солна киселина:
По този начин, детерминанта на поведението на протеина като анион или катион е водород йонна концентрация или рН на средата. Когато концентрацията на водородните йони (кисела среда - рН 0-7) протеин става катион, когато се понижава (сряда schelochnaya- рН 7 -14), напротив, протеинови частици станат аниони. Тази способност на протеина или проявяват киселинни или алкални свойства го характеризира като амфотерно съединение.
Въпреки това, при определени стойности на рН на броя на положителните заряди на протеина ще бъде равен на броя на отрицателен заряд и молекулата като цяло е почти равна на нула. Молекулата на протеин няма да се движат в електрическо поле. При тези условия, протеинът е в изоелектричната състояние; рН на разтвора, в който протеинът е в изоелектричната състояние се нарича изоелектричната точка. Изоелектричната точка на най-естествен протеин е в слабо кисела среда (рН 4.8-5.4). Молекулата на такива протеини съдържа повече карбоксилни групи в амино. Това показва, че в техния състав съдържа повече дикарбоксилни аминокиселини (вж. Аминокиселините). Изоелектричната точка на протеина се намира в най-стабилно състояние и с малки промени на рН в кисела или алкална страна тя лесно се утаява.
Амфотерните протеини в основата буфер система протеин, който участва в поддържането на кръвното специално реакционна среда. Амфотерните свойства на протеини се използват, за да ги разделят на отделни фракции (метод електрофореза), за да се диагностицира различни заболявания и наблюдение на състоянието на пациента.