Структурата, номенклатурата, алкалността на амините
Ако молекулата на амоняк последователно замени водородни атоми от въглеводородни радикали, един получи съединения, които са клас амини. Съответно, има първични амини (RNH2), вторични (R2NH), третични (R3N). -NH2 група, наречена амино група.
Разграничаване алифатен, ароматен, алицикличен и хетероциклични амини, в зависимост от това, което радикалите свързани към азотния атом.
Изграждане на амини, получени чрез добавяне на имена на префиксите името амино съответния въглеводород (първични амини) -амин или затваряне на горните хостинг проекта нияма радикали, свързани с азотен атом (за всички амини).
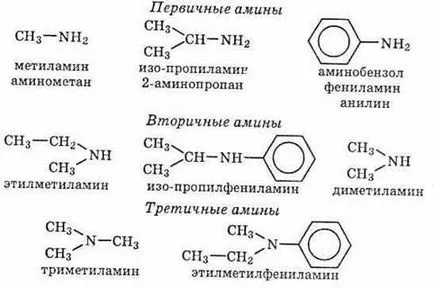
Амините са бази, тъй като азотният атом може да осигури електронна двойка за образуването на elektronnedoetatochnymi частици върху механизма на донор-акцептор (както е определено от Люис алкалност). Следователно амини, както и амоняк, са способни на взаимодействие с киселини и вода, чрез прикрепване на протонната да образуват съответните амониеви соли.
Амониеви соли са лесно разтворими във вода, но са слабо разтворими в органични разтворители. Водните разтвори са аминови алкална реакция:
Основни амини свойства зависят от естеството на заместителя. По-специално, ароматни амини - слаба база от алифатен, защото свободна електронна двойка на азот влиза в зацепване с р-ароматна пръстенна система, която намалява електронната плътност на азотен атом (-М ефект). В контраст, алкил групата е добър донор на електрони плътност (+ I-ефект).
Геометрията на амино молекули.
Методи за селективно получаване на амини.
1. Реакция Хофман. Един от най-ранните методи за получаване на първични амини - алкилиране на амоняк с алкилхалогениди:
Това не е най-добрият метод, тъй като резултатът е смес от амини с степента на заместване:
Алкилиращи агенти могат да действат не само халиди, но също така алкохоли. Към тази смес на алкохол и амоняк се прекарва през алуминиев оксид при висока температура.
При взаимодействие на амоняк с алкилхалогениди, например RCL, смес от първични, вторични и третични амини. Получената от продукт HCl е прикрепена към амин да се образува амониева сол, но солта се разлага излишък от амоняк, който позволява на процеса до образуването на кватернерни амониеви соли (Фиг. 4А). За разлика от алифатни алкилхалогениди, арилови халиди, например, С6 Н5 CI, реагира с амоняк с голяма трудност, синтезът е възможно само когато катализатори, съдържащи мед. В промишлеността, алифатни амини получени чрез взаимодействие на алкохоли с каталитични NH3 при 300-500 ° С и налягане от 1-20 МРа, при което се получава смес от първични, вторични и третични амини (Фиг. 4В).
Когато първични амини (Фиг. 4В), и взаимодействие на алдехиди и кетони с първични амини (в присъствието на НСООН мравчена киселина) води до вторични амини (фиг. 4D) взаимодействие на алдехиди и кетони с амониева сол на HCOONH4 мравчена киселина, образувана.
Съединенията нитро (съдържащи -NO2 група) в възстановяването образуват първични амини. Този метод, предложен NN Зинин малко използва за алифатни съединения, но важно за получаване на ароматни амини и формира основата за промишленото производство на анилин се използват като редуциращи агенти: Н2 (на катализатора). Понякога водород се генерира в момента на реакцията, което се третира метали (цинк, желязо) с разредена киселина. (Фиг. 4D).
Химичните свойства на амини.
Отличителният способността на амини -. Прикачване неутрални молекули (например халогеноводороди Hhal, за да се образува organoammonievyh соли такива като амониеви соли на неорганична химия за образуване на ново съобщение азот осигурява неразделен двойка електрони, действащи като донора участват в образуването поради протон Н + от (от халид). играе ролята на акцептор (приемник), връзка нарича донор-акцептор (фиг. 1). Получената ковалентна връзка, N-H е напълно еквивалентни отношения, съществуващи в амин N-H.
Третични амини са свързани HCI, но чрез нагряване на получената сол в разтвор на киселина тя се разпада, при което R се отцепва от N атом:
При сравняване на тези две реакции може да се види, че групата на С2 Н5, и Н, сякаш обратно, в резултат на третичен амин образува вторична.
Разтваря се във вода, амини по същия начин улавяне протон, в резултат разтвор на йони се появяват ОН -. което съответства на образуването на алкална среда, е възможно да се открие с конвенционалните показатели.
С образуването на амини донор-акцепторни връзка може да бъде приложен не само HCI, но халоалкили RCL, при което се образува нова връзка N-R, което също е еквивалентен на вече наличните. Когато започне да се вземе третичен амин, тетраалкил амониевата сол се получава (R четири групи в един N атом):
Тези соли се разтварят във вода и някои органични разтворители разпадат (разтваряне) за образуване йони:
Такива разтвори, както и всички разтвори, съдържащи йони провеждат електричество. соли тетраалкиламониеви могат да бъдат заместени с халоген НО-група:
Получената тетраметиламониев хидроксид е силна основа в свойства близки до основи.
Първични и вторични амини реагират с азотиста киселина HON = О, но те реагират по различни начини. Тъй като първични амини се получават първични алкохоли:
За разлика от първичните, вторични амини с азотиста киселина за образуване на жълто, умерено разтворими нитрозамини - съединения, съдържащи остатък> N-N = O:
Третични амини при стайна температура с азотиста киселина не реагират по този начин, азотиста киселина е реагент, който позволява да се направи разграничение между първични, вторични и третични амини.
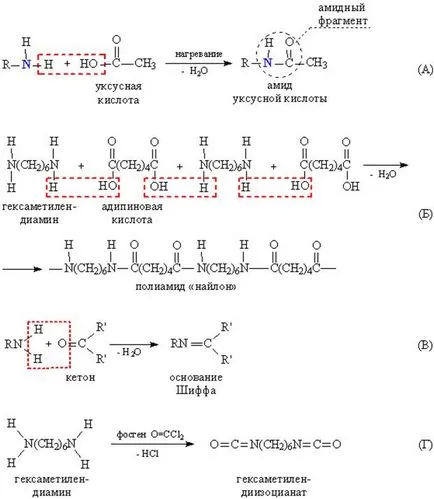
Кондензацията на амини с карбоксилни киселини, киселинни амиди, образувани - със съединение с група С (О) N<(рис. 2А). Если в качестве исходных соединений взять диамин и дикарбоновую кислоту (соединения, содержащие соответственно две амино- и две карбоксильные группы, соответственно), то они взаимодействуют по такой же схеме, но поскольку каждое соединение содержит две реагирующие группы, то образуется полимерная цепь, содержащая амидные группы (рис. 2Б). Такие полимеры называют полиамидами.
Кондензацията на амини с алдехиди и кетони, води до образуването на така наречените Шифови бази - съединения, съдържащи група -N = C<(рис. 2В). На схеме В видно, что для образования двойной связи между N и С азот должен предоставить два атома Н (для образования конденсационной воды), следовательно, в такой реакции могут участвовать только первичные амины RNH2 .
В реакцията на първични амини с фосген Cl2 С = О група, за да се образува съединение -N = С = О, наречени изоцианати (Фиг. 2G, се получава съединение с две изоцианатни групи).
Сред най-известните ароматни амини анилин (фениламин) С6 Н5 NH2. Според свойствата е близо до алифатни амини, но основната слабо изразен - във воден разтвор не образува алкална среда. Като алифатни амини със силни минерални киселини, може да се образува амониева сол на [С6 Н5 NH3] + Cl -. В реакцията на анилин с азотиста киселина (в присъствието на солна киселина), генерирани диазо съединение, включващо частта R-N = N, е под формата на йонна сол, диазониева сол, наречен (Фиг. 3a). Така, реакцията с азотиста киселина не е, както е в случая на алифатни амини. бензолното ядро в анилин е реактивен характеристика на ароматни съединения. халогенирането на водородните атоми в орто - и пара-позиция с амино група, заместена, хлороанилини получени с различни степени на заместване (Фигура 3B.). Действието на сярна киселина в сулфонирането води до пара-позиция към амино групата, така наречената сулфанилова киселина (фиг. 3B).
Горене амин при образуване на въглероден двуокис, азот и вода:
4CH3NH2 + 9O2 = 4SO2 + 2N2 + 10Н2О
Ароматни амини са спонтанно окислени на въздуха. По този начин, анилин бързо става кафяв поради окисляване във въздуха.
Присъединяване халоалкани алкил халиди Амини прикрепени, да образуват соли:
Лечение на получената сол с алкален, може да се получи свободния амин:
Реакцията на амини с азотиста киселина голямо значение е реакцията на диазотиране ароматни първични амини чрез действието на азотиста киселина, получена ин ситу чрез взаимодействие на натриев нитрит и солна киселина:
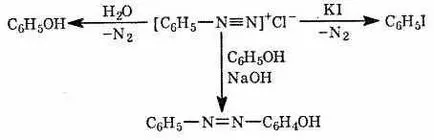
Основни алифатни амини чрез реакция с азотиста киселина, за да образуват алкохоли и вторичен алифатни и ароматни амини дават N-нитрозо производни:
R-NH2 + NaNO2 + HCl = R-OH + N2 + NaCl + H2O
R2NH + NaNO2 + HCl = R2N-N = O + NaCl + H2O