Реакцията на съединение
Много процеси, без които е невъзможно да си представим живота (като дишане, храносмилане, фотосинтеза, и други подобни), са свързани с различни химични реакции на органични съединения (и неорганичен). Нека да разгледаме основните типове и тяхното по-подробна фокус върху процеса, наречен Connect (връзка).
Какво се нарича химическа реакция
На първо място е необходимо да се даде обща дефиниция на това явление. Чрез изразът под внимание, че се отнася до различните реакционни материали с различна сложност, което води до образуването от изходните продукти. Участващите в този процес на веществото по-долу "реагенти".

писмо химическа реакция на органични съединения (и неорганичен) е записан с помощта на специализирани уравнения. Външно, те изглеждат като малки математически примери за допълнение. Въпреки това, вместо знак за равенство ( "="), използвани от стрелката ( "→" или "⇆"). Освен това понякога може да бъде повече вещества от дясната страна на уравнението, а не в ляво. Всичко, което е за стрелки - вещество, преди реакцията (от лявата страна на формулата). Всичко, което след (вдясно) - съединение, образувано в резултат на минало химичен процес.
Като пример можем да считаме, химическата реакция уравнение разлагането на водата на водород и кислород под действието на електрически ток: 2Н2 О → 2Н2 O2 ↑ + ↑. Вода - този изходен материал, с водород и кислород - продукти.
Като друг, но имат по-сложен пример на химична реакция на съединенията може да се счита явление запознат всеки собственик, след пекат сладкиши. Става дума за изчезването на сода за хляб с помощта на оцет. Преместването на действие е илюстрирано с помощта на уравнението: NaHCO 3 2 СН3 СООН → 2СН3 COONa + СО 2 ↑ + Н2 О. От това става ясно, че по време на взаимодействието на натриев хидрогенкарбонат и оцет образува натриева сол на оцетна киселина, вода и въглероден диоксид.
Съгласно своя характер на химични процеси е междинен между естествени и ядрената.
За разлика от първия, участващи в химична реакция на съединение, способно да се променя неговия състав. Това е, атоми на едно вещество могат да образуват няколко други като в горното уравнение, разлагането на вода.
За разлика от ядрената химични реакции не засягат атомните ядра взаимодействащи вещества.
Какви видове химични процеси
Разпределението на реакции на съединенията от видовете се извършва по различни критерии:

- Обръщане на / необратимост.
- В присъствието / отсъствието на катализиране вещества и процеси.
- Чрез абсорбция / отделяне на топлина (ендотермичен / екзотермична реакция).
- Според броя на фазите: хомогенна / хетерогенна и два хибридни сортове.
- Чрез промяна окисляване взаимодействие вещества.
Видове химични процеси в неорганична химия чрез процес на взаимодействие
Този критерий е специфична. С него, има четири вида реакции съединение, заместване, разлагане (разцепване) и обмен.
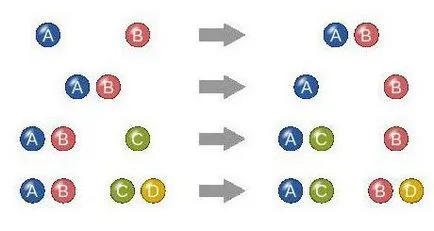
Името на всеки от тях съответства на процеса, който го описва. Това означава, че съединение вещество се смесват в заместването - са променени с други групи в реагент на разлагане е образувана от няколко, като в обмена участниците реакционни са разменени атома.
Видове процеси на процеса на взаимодействие в Organic Chemistry
Въпреки голямата сложност на реакцията на органични съединения се случи на същия принцип като неорганичното. Въпреки това, те имат няколко различни имена.
По този начин, реакцията на разлагане на съединението и се наричат "придържане" и "разцепване" (elimirovanie) и директно органичен разлагане (тип разцепване два процеса присъстват в този раздел на Chemistry).
Други реакции на органични съединения - е заместване (име не се променя), прегрупиране (обмен) и редокс процеси. Въпреки сходството на техните механизми появяване, органичните са по многообразни.
Химическа реакция на съединение
След разглеждане на различните видове процеси, вещества, които се предлагат в органична и неорганична химия, заслужава да се гледа по-подробно точно на кръстовището.
Тази реакция е различен от всички останали в това, независимо от броя на реагентите в началото, в края всички те се сливат в едно.
Като пример можем да си припомни процеса на гасене вар СаО + H2O → Са (ОН) 2. В този случай реакцията протича съединение с калциев оксид (негасена вар) оксид на водород (вода). Това води до калциев хидроксид (гасена вар) и стои топла пара. Между другото, това означава, че процесът екзотермична.
Уравнението на реакцията на съединение
Схематично, въпросния процес може да бъде представена както следва: А + BV → XYZ. Във формулата ABC - новообразувано комплекс вещество А - прост реагент и BW - вариант комплексно съединение.
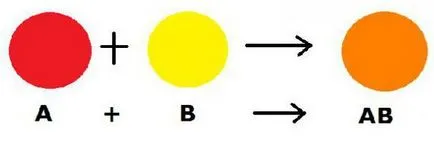
Трябва да се отбележи, че тази формула е типично за връзката и процеса на свързване.
Примери на реакцията под внимание - това взаимодействие натриев окис и въглероден двуокис (СО2 NaO2 + ↑ (т 450-550 ° С) → Na2 CO3) и серен оксид с кислород (О2 2SO2 + ↑ → 2SO3).
Също така могат да реагират един с друг по-сложни съединения: AB + SH → ABCD. Например, една и съща натриев оксид и оксид на водород: NaO2 + Н2 О → 2NaOH.
Условия на реакцията в неорганични съединения
Както е показано в предишния уравнение, изследваните вещества, които могат да влизат в взаимодействие с различна степен на сложност.
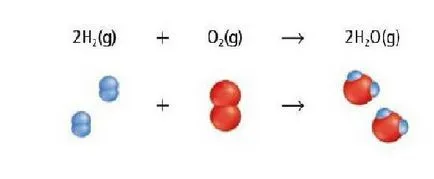
Така прости реагенти са възможни реакция неорганична редокси на съединението (А + В → AB).
Като пример, помисли за процеса на получаване на тривалентен железен хлорид. За тази реакция се провежда между хлор съединение и Ferum (желязо): 3Cl2 ↑ + 2Fe → 2FeCl3.
В случай, че е сложно взаимодействие на неорганични вещества (SH + AB → ABCD), процесите могат да се появят като засягат или не засягат тяхната валентност.
Като илюстрация на този пример е да се разгледа образуването на калциев карбонат от въглероден диоксид, оксид на водород (вода) и оцветител Е170 бяло храна (калциев карбонат) CO2 ↑ + Н 2О + СаСО3 → Са (CO3) 2. В този случай има класическата реакция на съединение. Когато валентността на нейното изпълнение на реагентите не се променя.
Малко по-ангажиран (от бившия) химично уравнение 2FeCl2 + Cl2 ↑ → 2FeCl3 е пример на редокс взаимодействия с прости и сложни неорганични реактиви газ (хлор) и соли (железен хлорид).
Видове присъединителни реакции в органичната химия
Както е посочено в четвърта алинея, в материали от органичен произход присъства реакция се нарича "присъединяване". Като правило, че присъстват сложни вещества с двойно (или тройни) връзки.
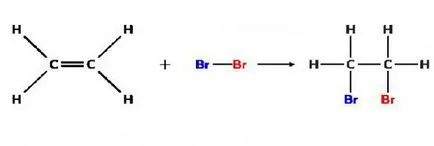
Например, реакцията между дибромо етилен, което води до образуването на 1,2-дибромоетан (С2 Н4) СН2 = СН2 + Br2 → (C₂H₄Br₂) BrCH2 - СН2 Br. Между другото, признаците Подобни на равно и знак минус ( "=" и "-") в това уравнение показва връзки между атоми на съединение. Тази функция за запис органика формули.
В зависимост от това коя от съединенията действат като реагенти са няколко вида съгласно процес, свързваща предвид:
- Хидрогенирането (H водород молекули са добавени към двойната връзка).
- Gidrogalogenirovanie (присъединява халид).
- Халогениране (добавяне на халоген Br2, Cl2 ↑ и други подобни).
- Полимеризацията (образуването на няколко малки молекули на вещества с високо молекулно тегло).
Примери на реакцията на добавяне (съединение)
След включване в списъка на видовете, които се разглеждат процес трябва да се научат да практикуват някои примери за реакцията на свързване.
Като илюстрация, хидрогенирането може да се обърне внимание уравнение взаимодействие пропен с водород, при което има пропан (С 3 Н 6 ↑) -СН = СН2 СН3 ↑ + Н2 ↑ → (С3 H8 ↑) СН3 -СН2 -СН3 ↑.
Съединенията от органичната реакционна химия (допълнение) могат да възникнат между солна киселина (неорганично вещество) и етилен до образуване хлороетан (С2 N4 ↑) = СН2 СН2 ↑ + HCl → СН3 - СН2 -С (С2 Н5 Cl). Е представена от уравнение gidrogalogenirovaniya пример.
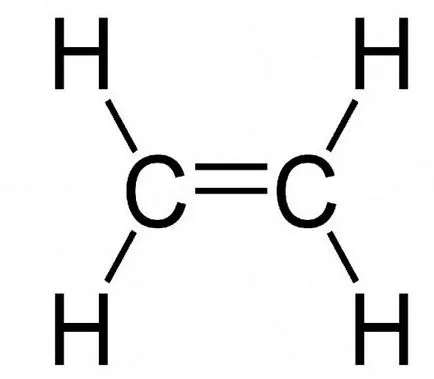
Както за халогенирането може да се илюстрира чрез реакцията между етилена и дихлор, което води до образуването на 1,2-дихлороетан (С2 Н4 ↑) СН2 = СН2 + Cl2 ↑ → (C₂H₄Cl₂) ClCH2 -СН2 Cl.
Много полезни вещества се образуват поради органичната химия. Взаимодействието на съединение (адукт) на молекули на етилен с радикал инициатор на полимеризацията под въздействието на UV светлина - доказателство: п = СН2 СН2 (R и UV светлина) → (-СН2 -СН2 -) п. Създадена по този начин е добре известно на всеки човек, при полиетилена за името.

От този материал са направени различни видове опаковки, торбички, съдове, тръби за изолационен материал и много други. Отличителна черта на този материал е възможността за рециклиране. Неговата популярност е длъжен полиетилен, който не се разгражда, защото от това, което еколозите имат негативно отношение към него. Въпреки това, през последните години е установено за безопасно изхвърляне на пластмасови изделия. За този материал се третира с азотна киселина (HNO3). След това някои видове бактерии, способни на разграждане на това вещество в безвредни компоненти.
Реакцията на съединение (връзка) играе важна роля в природата и човешкия живот. В допълнение, той често се използва от учените в лабораториите да синтезира нови съединения за различни важни изследвания.
Една невероятна трансформация: "сляп" котка улица изненада всички красотата на очите си котка почти не видях нищо и едва ли можеше да се движи. Но когато той се лекува краста, се оказа, че той не е бил сляп. Освен това, окото просто Памук университет.
