Производство на минерални торове
към списъка на лекции
към списъка с артикули
Производство на минерални торове.
Минералните торове са един от най-важните икономически дейности на човешките продукти на химическата промишленост.
Ръстът на населението се изправя срещу всички страни на един и същ проблем - умелото управление на способността на природата да се възпроизведе жизненоважни ресурси и най-вече на храната. Задачата на разширеното възпроизводство на храна отдавна е решен чрез използването на селскостопански торове.
Класификация на минерални торове.
Минералните торове са класифицирани от три основни характеристики - агрохимически цел, състав и свойства.
Предназначен за агрохимически торове са разделени на права. които са източник на хранителни вещества за растенията, и непряко. служи за мобилизиране на хранителните вещества в почвата чрез подобряване на физически, химически и биологични свойства. Индиректни торове, например, варовикови торове се използват за неутрализиране на кисели почви, торове структура стимулиращи агрегиране на частиците и тежка глинеста почва и др.
Прави торове могат да съдържат един или няколко различни хранителни вещества. По броя на хранителни вещества, торове са разделени на прост (еднопосочен) и комплекс.
С прости торове включващи само един от трите основни вещества: азот, фосфор или калий. Съответно, прост азотен тор е разделен. фосфат и поташ.
Сложни торове съдържат два или три основни хранителни вещества. По броя на основните хранителни вещества сложни торове се подразделят на две (например, като NP или RK) и трикомпонентни (NPK). Последно наричан също приключи. Торове, които съдържат значителни количества хранителни вещества и малко груб, наречена концентрирани.
Сложни торове, в допълнение, разделени в смесени и сложни. Наречен смесени механични смеси от торове, състоящи се от хетерогенни частици. Ако торът е сложен съединения, които са резултат от химическо взаимодействие, те са сложни.
Тор, предназначен за растенията с хранителни вещества, които стимулират растежа им и необходими в малки количества, се наричат микро торове. и те съдържат хранителни вещества - микроелементи. Такива торове се прилагат върху почвата, в много малки количества. Те включват соли, съдържащи бор, манган, мед, цинк и др. Елементи.
Състояние на агрегация тор разделя на твърди и течни (например, амонячна вода, водни разтвори и суспензии).
Физичните свойства на минерални торове, за да отговарят на редица изисквания. Водоразтворими соли трябва да бъдат свободно течащи, лесно да се разпръсне, не бъде силно хигроскопичен, без спичане по време на съхранение, трябва да е от такова естество, за да оцелее в почвата за известно време, не твърде бързо отмива с дъждовна вода и не издухан от вятъра. Тези изисквания са най-подходящи за едрозърнест гранулирани торове. Гранулирани торове, могат да бъдат приложени на терена с помощта на машини и сеялки тор в строго определени количества съответните агрохимически изисквания.
Ефективно намаляване на спичане собственост на повърхностна обработка с повърхностно активни гранули. През последните години са разгледани методи създаване на специални обвивки около гранули, които от една страна се предотврати спичане на тора от друга - позволява да се регулира по време на разтварянето на хранителни вещества в почвата вода, т.е. създаде дългодействащ тор.
Да разгледаме някои от процесите за получаване на фосфор, азот и сложни торове.
Съществуват редица методи за обработка на естествени фосфати в торове: механични, термични и киселинни методи храносмилането.
Един от методите е обработка смилане фосфати. Получената фосфор брашно за използване в кисели почви се разтваря бавно в почвата вода и по този начин става много ток тор.
Фосфатни торове могат да бъдат получени чрез термично разлагане на фосфат при температура 1200 - 1800 ° С Така получен termofosfaty, defluorinated фосфат, магнезиев, обработени и термо-алкални фосфати.
Основният метод за получаване на фосфатен тор е химическото разлагане на фосфатни суровини. По този начин, в, се преработва в троен суперфосфат, утаяване и сложни торове чрез обработка сярна киселина, прост суперфосфат и фосфорна киселина, която на свой ред.
Производство суперфосфат.
производство РЕЗЮМЕ суперфосфат е да се превърне природен флуорапатит, неразтворим във вода и почвени разтвори, разтворими съединения, главно в монокалциев фосфат (Са (Н2 РО4) 2)
В този процес, разлагането протича на два етапа. В първия етап около 70% от апатит взаимодейства със сярна киселина. Това представлява фосфорна киселина и калциев сулфат полухидрат (уравнение (1)). Този етап се характеризира с образуването на повърхностни филми на зърна CaSO 4 фосфат. Структурата на получения процент кора на кристализация поради твърда фаза зависи главно от ситост разтвор на калциев сулфат, който на свой ред се определя на сярна киселина концентрация, температурата и други фактори. Следователно, сярна концентрация киселина оптимално смесване на достатъчна скорост на разтваряне на апатит да се образува хлабав филм по-пропусклива за дифузията на сярна киселина към повърхността на фосфат. Първият етап завършва след 20 - 40 минути след смесването на фосфат със сярна киселина. След пълно изчезване на сярната киселина започва втория стадий на разлагане, при което останалата част от апатит (
30%) с разлагане фосфорна киселина
Получената монокалциев фосфат, калциев сулфат разлика не е веднага се утаява. Постепенно насища разтвор на фосфорна киселина, и след това започва да кристализира под формата на Са (Н2 РО4) 2 х Н 2О и протича много по-бавно от реакция (1), поради ниската активност на фосфорна киселина чрез кристализация и твърди фази. Тя започва в клетките на суперфосфат и продължава в продължение на 5 - 20 дни на съхранение в склад на суперфосфат.
За стабилно високо качество суперфосфат преди узряване се неутрализира твърди добавки (варовик брашно фосфат и т.н.) и гранулирани.
Производство на двоен суперфосфат.
Троен суперфосфат - концентрирана фосфор тор. Получената разлагането на природен фосфати фосфорна киселина. Той съдържа 42 - 50% смилаем Р 2О 5. която е 2-3 пъти по-голям от по прост суперфосфат. За разлика от последната, троен суперфосфат почти не съдържа баласт - калциев сулфат. протича процеса съгласно уравнението (2).
разлагане Азотна киселина на фосфати.
Получаването на торове.
Прогресивно посока в метода на сурово обработка фосфат е разлагането на нитрати и фосфати апатити. Този метод позволява използването на азотна киселина не само като средство за разпадане на фосфорит, но допълнителен източник на хранителни вещества. Въз нитрат разпадане фосфати обикновено се получават комплекс NP - или NPK -udobreniya.
основа разлагането на азотна киселина процес фосфат е реакция
в резултат на което се образува капака нитрат разтвор, съдържащ калциев нитрат и свободен фосфорна киселина. Съществуват няколко метода за допълнителна преработка на екстракция азотна киселина. В екстракт много процеси се неутрализира с амоняк до получаване на амониеви фосфати (NP -udobreniya). Ако преди гранулиране неутрализира суспензия се добавя към калиева сол на (. KCl K 2 SO 4), се получава троен NPK -udobrenie - NPK.
В много процеси, азотна фосфати обработка на калциев нитрат, образуван в реакция (3) се отстранява от реакционната смес чрез изпаряване. Дизайнът на такива схеми позволява сложна обработка на фосфат суровини и създаване на производствени отпадъци на практика не допуска изхвърляне на отпадъци, по-специално фосфогипс. Фосфатен метод нитрат разлагане позволява да се получи по NPK -udobreny едновременно изолирани от суровини ценни продукти като стронций, редкоземни метали и др. Намери приложение в различни отрасли (електроника, металургия, и т.н.).
Производство на азотни торове.
Най-важните видове торове са азотни торове: амониев нитрат, карбамид, амониев сулфат, воден разтвор на амоняк и други.
Азотни торове се различават един от друг в съдържанието на азот под формата на азотни съединения (нитрат, амониев, амид), фаза състояние (твърдо вещество или течност).
Производство на амониев нитрат.
Амониев нитрат или амониев нитрат (NH 4 NO 3) - кристално вещество с бял цвят, съдържащ 35% азот в амониеви нитрати и форми, и двете форми са лесно усвоими от растенията. Гранулиран амониев нитрат се използва в голям мащаб преди сеитба и за всички видове превръзки. В по-малък мащаб, тя се използва за производството на взривни вещества.
Амониевият нитрат е силно разтворим във вода и има висока хигроскопичност. Това е причината, поради която гранули тор се разтегнат, губят своята кристална форма възниква спичане торове - прахообразния материал се превръща в твърдо вещество монолитна маса.
За почти без спичане амониев нитрат използвани редица методи за обработка. Първо, гранулиране. Общата площ на гранулите е по-малко хомогенна повърхност същото количество фини кристални соли, обаче гранулиран тор бавно абсорбира влагата от въздуха. Понякога амониев нитрат е слят с по-малко хигроскопични соли, като амониев сулфат, амониев фосфат, калиев хлорид, магнезиев нитрат.
В основата на процеса на производство на амониев нитрат лежи хетерофазов реакция между газообразен амоняк и разтвор на азотна киселина
Метод е ограничено чрез разтваряне на газ в течност. За да се намали инхибиране дифузия изисква интензивно смесване на режима на реакционната маса. Реакция топлина ефективно се използва за изпаряване на водата от разтвори на амониев нитрат. Вариантът за получаване на амониев нитрат стопилка с помощта на концентрирана азотна киселина, и предварително нагряване на съставките (разтопено съдържа 95-96% амониев 4 NO 3).
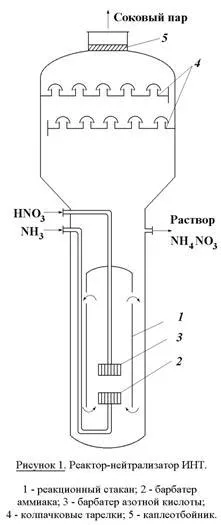
Понастоящем, най-често схемата с частично изпаряване на разтвора от топлината на неутрализация. Неутрализацията се извършва в апарат IOT (използване на топлината на неутрализация) (виж фигура 1). Апаратът се състои от два цилиндъра (външни и вътрешни). Вътрешната газообразен амоняк се подава и напръскани с азотна киселина. Вътрешната част е реакционно пространство, външният - зоната на изпаряване. отвеждане на топлината от реакционната зона е необходимо не само за изпаряване на разтвора, но също така да се избегне прегряване и разлагане на азотна киселина и амониев нитрат. Сок пара, генерирана в резултат на изпаряване на водата от реакционната смес се използва за предварително загряване на реагентите и реакционният разтвор се изпарява.
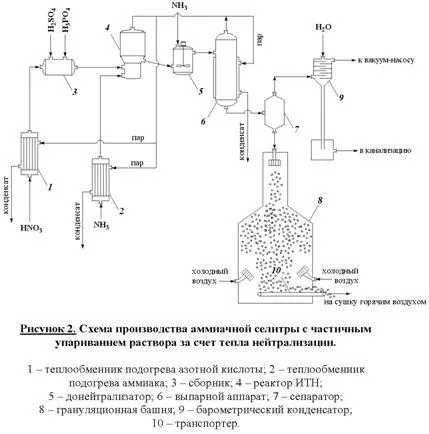
Монтаж схема, представена на фигура 2.
към списъка с артикули
към списъка на лекции