Експресия материал плътност чрез масата на молекулата и броят на молекули на единица обем
Тъй като всички вещества се състоят от молекули, всички тегловни сума на масите на молекулите по същия начин, например като масив от пакети с грах сума на масите на всички грах, които са в пакета. Лесно е да се определи масата на грах - грах опаковка трябва да се претегля. Но ако всички грах са равни, тогава грах маса може да се определя чрез умножаване на теглото на грахово зърно от броя на грах в пакета.
Молекулите на чисто вещество са идентични, и следователно, например, масата на водните капки е продукт на масата на една водна молекула на броя на молекули в спад.
Плътността на вещество показва какво е масата на 1 m 3 на веществото. Плътност на кислород газ, например 1,43 кг / м3. Този номер може да бъде получена чрез умножаване на масата на един кислороден молекула на броя на молекули, съдържащи се в 1 m3 от обема си.
плътност вещество е продукт на масата на единична молекула на веществото от броя на молекулите на единица обем.
Разбира се, на практика плътността на материята се броят греша, но в по-прост начин - с телесно тегло и обем. Но, знаейки, плътността на веществото и масата на молекула, може да се определи броят на молекули в 1 м3 на материал, който не може да бъде изчислена по друг начин. За броя на молекулите в 1 м3 вещества плътност трябва да бъдат разделени от масата на един от неговите молекула, молекула на теглото се определя емпирично.
По този начин, например, изчислени в 1м3 чист водата, съдържаща 3.34 * 28 октомври молекули и в 1 м3 на кислород-10 2,7 * 25. Тези числа са толкова големи, че, разбира се, не е възможно директно да разчита на молекулата. Дори ако освобождаването на 1 m3 на кислород до 1 милион молекули в секунда, както и че ще се наложи на 900 милиарда години.
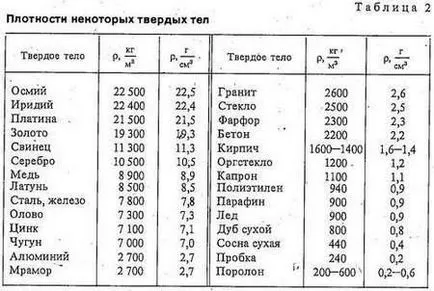
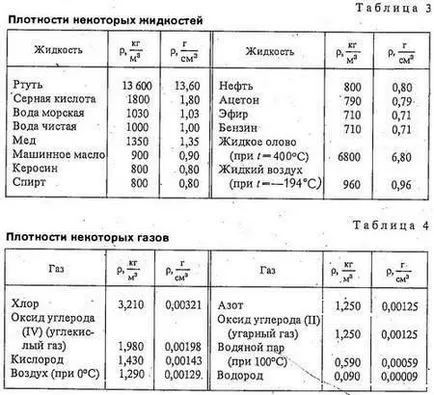
Таблици 2-4 са дадени някои плътност на твърди вещества, течности и газове. Помислете за масата и да забележите голяма разлика от плътността на плътността на твърди вещества и течности газ.
плътност кислород газ от 1,43 кг / м3. Поради това силно охлаждащ газ чрез пресоване и подготвени течен кислород, който има плътност от 1140 кг / м3. И газообразен и течен кислород се състои от идентични молекулно - кислородни молекули. Защо е толкова трудно - почти 1000 пъти - различни по плътност? Припомнете си, че газовите молекули са на голямо разстояние един от друг, отколкото в течности. Следователно брой молекули на 1 м3 газ е по-малко от 1 m3 на течност.
Въпроси. 1. Както е посочено от плътността на материала чрез масата на молекулата и броят на молекули в 1 м3? 2. Защо е плътност на газ по-малко от плътността на течности и твърди вещества? 3. Какво трябва да знаете, за да се определи броя на молекулите в 1 m3 от вещество?
Упражнения. 1. плътността на водата при 100 ° С е 950 кг / м3, и максималната плътност на водна пара при същата температура, 0.590 кг / м3. Как да се обясни разликата между плътностите на вода и пара? 2. Плътността на газ водород от 0.09 кг / м3, и твърдият водород 80 кг / м3. Въведете Причината за тази разлика. 3. Защо на сгъстен газ има по-голяма плътност, отколкото некомпресиран? 4. Проверете дали в 1 м3 вода, съдържаща 3.34 * 28 октомври молекули. Тегло на една молекула вода е равна на 2,99 / 10 до 26 кг.