живеещи полимеризация
Анионна полимеризация - е йонна полимеризация, в който кинетичните верига носители са аниони. Активното място на анионна полимеризация има частично или пълно отрицателен заряд. Обща схема инициира полимеризация чрез образуване на карбанион може да бъде представена както следва:
Като цяло, в анионни системи могат да съществуват различни форми на активни центрове в състояние на равновесие (поляризирана молекула йонна двойка свободни йони):
Това обяснява значителна зависимост от кинетиката на процеса и микроструктурата на получения полимер от свойствата на реакционната среда и противойонът.
Мономери. най-лесно полимеризация анионно, са ненаситени съединения, съдържащи електронни-отнемане заместители (-COOR, -NO2. -CN, -СН = СН2. С6 Н5 и т.н.). Чрез анионна полимеризация може също карбонил и хетероциклични съединения, имащи С = С, С = О, C = N (оксиди, лактони, лактами, силоксани и т.н.). Най-честите мономерите са относителната активност в реакциите на анионна полимеризация могат да бъдат подредени в серии:
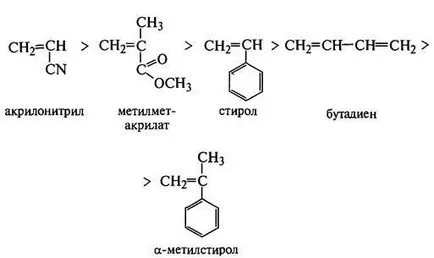
Инициатори на анионна полимеризация може да бъде вещество Ba vnogo характер - алкални и алкалоземни метали и техните производни (алкили, алкоксиди, амиди, арили). Той може също да доведе до електрически ток или йонизиращо лъчение. Типични примери на полимеризационни инициатори анионни - натриев амид (NaNH2), Metally алкален (Li, Na, К, Rb, Cs) и техните алкили, алкални metallov комплекси с ароматен yglevodorodami (Na нафтил, нафтил K).
Анионна полимеризация има определени предимства пред свободна радикалова полимеризация: тя е приложима за широк кръг от мономери; Това дава много по-големи възможности за синтез на стереорегулярността, включително оптично активни полимери; поради образуването в редица анионни системи "живот" полимери произвежда полимери на предварително определено молекулно тегло, разпределение тесен молекулно тегло и се синтезират блок и присадени съполимери на дадена структура.
Обща схема включва анионна полимеризация започване, растеж, прехвърляне и прекъсване на веригата. Последните две реакции, които често се наричат комбиниран растеж верига ограничаване реакции придружени от анионна полимеризация не е във всички случаи. Те са по-чести в полярен среда (реакция прехвърляне верига) и полярен мономер (реакция прекратяване верига), но може също да се дължи на присъствието в случайни онечиствания на реакционната система, по-специално, вещества, инактивиране на органометално съединение.
Образуването на активния център в анионна полимеризация може да се случи чрез различни механизми.
1. Откриване на механизма за свободен анион връзка се осъществява в полимеризацията на мономери в разтворители с висока полярност. например, в течен амоняк при катализа с алкални метали и техните амиди:
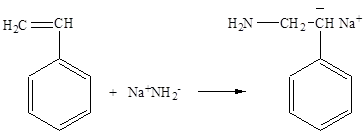
2. Съгласно механизма на електронен трансфер от инициатора на полимеризацията на мономер възниква при използване на алкален metallovv слабо полярен среда. например полимеризация на бутадиен. Първоначалното действие на откриване на образуването на анион радикал мономер:
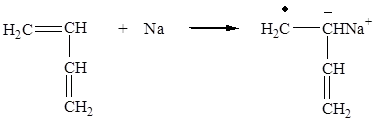
Като резултат от рекомбинация на две anionradikalov biion оформен, който е активен център на полимеризацията (при ниска температура и в неполярен среда):
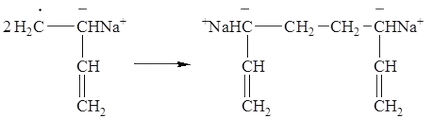
По-добър контрол на полимер молекулно тегло може да бъде постигната чрез използване на алкален метален катализатор комплекс - нафтален в полярен разтворител (тетрахидрофуран). Този тип на започване на анионна полимеризация се нарича полимеризация с електронен трансфер. Технологична схема:
Комплексът прехвърля електрони на мономер, нафталин и регенерира родителската молекула:
Тези каталитични системи са способни при отсъствие на примеси да осигуряват растеж верига без счупване до пълно изчерпване на мономер образува, когато така наречените "жива" полимери, чиито макромолекули са отрицателно заредени йони.
3. Чрез механизма на свързване към молекула мономер с двойна връзка на инициатор са алкили на алкални метали (R-Me). Инициатор системи от този тип са в някои случаи съществено различни от по-горе, тъй като имат способността да координира молекула мономер да му се даде определена пространствена позиция, която се съхранява в структурата образуващ макромолекула. Това се вижда най-ясно в полимеризацията на изопрен с п-бутиллитий:
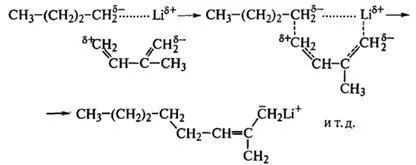
При полимеризацията на етилен с тези катализатори производни протича следващия цикъл от реакции:

Тъй полимеризация с органометални катализатори се среща в две места на катализатор (алкален метал и алкил), той се нарича механизъм два центъра на полимеризация. Координация на мономера в двата центъра ви позволява да изберете вида на полимеризация между другото, преминаващи на чисто анионен механизъм, и затова се нарича координация аниони полимеризация.
За повечето системи, верига стъпка може да бъде представен от схемата съгласно която настъпва въвеждането на всеки нов мономер молекула между алкилов остатък с отрицателен заряд, и противойон, обикновено метален йон:
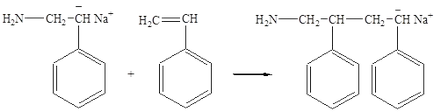
При прилагането на този механизъм е снабден строго редовни свързващите молекули на "глава на опашка" тип, тъй като молекулата на мономер поляризирана преди да поставите ориентирани под влиянието на йонна двойка. Въпреки това, докато stereoregularity, като цяло не е постигнато.
Стерео-полимери, получени при използване на органолитиеви катализатори. поради образуването на циклични комплекси с йонна двойка. в които мономерът има цис конформация. Това се дължи на факта, че Li е най-малкия радиус йон и висок потенциал за йонизация, което причинява най-ниската връзка полярността Li-C между алкалните метали. Тази връзка се съхранява в преход комплекс. Колкото по-висока стабилност на комплекса, по-високата stereoregularity.
растеж верига в анионна полимеризация е относително стабилни активни центрове, което позволява да се създадат условия за изучаване на механизма на анионна полимеризация, както и разтвори на различни синтетични задачи: Получаване на полимери с MWD зададени, включително почти монодисперсно; синтеза на полимери и олигомери с крайни функционални групи, способни на допълнителни полимеризация или поликондензация реакции от типа, както и блок съполимери, присадени съполимери и различни полимери с контролирано тип разклонения и др.
Деактивиране на активните центрове може да настъпи чрез няколко механизма.
1. Прехвърлянето на хидрид йон Н - или всеки друг анион след края на нарастващата верига на мономера или противойонът:
2. Разделяне на протон от нарастващ мономер верига или разтворител, способен на даряване на протонната (толуен, течен амоняк, органични алкохоли, киселини, и вода):
3. намаляване на реактивността на активния център, например в резултат на изомеризация реакции:
Както и при полимеризацията на катионни, в много случаи, полимеризация се извършва без да се счупи механизма кинетична верига "жива" вериги. Активността на такива полимери може да се поддържа за дълъг период от време и ако след пълното изчерпване на мономера това се добавят към системата отново, реакцията на полимеризация се възобновява. Повечето случаи въглеводородни полимери (стирен и негови производни, диени), чиято роля в полимеризацията на нежелани реакции е минимална. Съгласно механизма на "на живо" верига може да бъде полимеризация на хетероциклични съединения (етилен оксид cyclosiloxane).
Наличието на дълготрайни активни сайтове прави такива системи много удобни обекти изучава механизъм полимеризация, както и за различни синтези (блок съполимери, присадени полимери и звездообразните полимери с крайни функционални групи, и т.н.). Промишлено приложение на тези методи е ограничен чистота на изходните съединения и на необходимостта от поддържане на твърди условия синтез.
Анионна полимеризация се характеризира с голямо разнообразие от реакционни механизми и кинетични схеми. Във всеки случай, изборът на инициатори и условия на процеса, поради необходимостта от синтез на структурата на полимера и специфичен ММР. анионна полимеризация скорост особено при умерени температури много над радикал скорост полимеризация. Това се дължи на по-високата плътност на тока на активни частици (в граница, тя може да бъде равна на началната концентрация на инициатор).
Общият кинетична картина на анионна полимеризация, се усложнява значително от наличието на множество форми на активни центрове. Следователно, дори в случай на живот полимери с бърза стъпка започване, когато общата концентрация на отглеждане вериги е равна на първоначалната концентрация на инициатор, общата честота на реакция растеж верига не винаги е описано с обикновено уравнение
Дневна полимеризация. Блоксъполимерите
За първи път жив анионна полимеризация наблюдава Abkin и Медведев през 1930. но систематично изследва този процес Schwarz в 50-та. XX век. и към днешна дата, анионната полимеризация е широко разпространена. Карбанионите са относително по-стабилна и следователно по-малко реактивен частици в сравнение с карбокатиони, обаче анионната полимеризация на неполярни мономери и неполярни разтворители с ниска полярност. например, стирен или 1,3-бутадиен в бензен, тетрахидрофуран или 1,2-dimetiloksietilene липсва всички основни прекрати реакционната материал и кинетичната верига. Полимеризацията продължава до пълното изчерпване на мономера и в края му активни сайтове (аниони) се запазват макромолекули 1-2 седмици. През този период, полимеризацията може да бъде възобновено при добавяне на нов участък от мономер. Смята се, че бавната дезактивирането на активни места, свързани с реакции, започвайки с прехвърлянето на хидрид йон на плота:
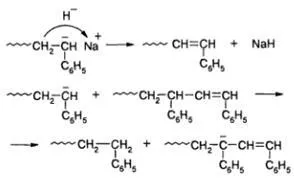
Полученият анион алилов Последната реакция не е в състояние да започне анионна полимеризация.
Дневна полимеризация на полярни мономери провеждат при много ниска температура, за да се избегне реакции трансфер и прекратяване. Всички основните характеристики на живот полимеризация верига - линейно нарастване на молекулното тегло с конверсия, разпределение тесен молекулно тегло, възможността за получаване на блокови съполимери - са най-силно изразени за живеене анионна полимеризация. По-специално, то се получава чрез този метод на практика монодисперсен полимери (обикновено полистирол), използвани като стандарти в гел хроматография. В КО = 0 и за степента на започване много по-висока от скоростта на растеж на к и >> скорост кр и степен на полимеризация са изразени чрез проста връзка:
където [Mo] и [М] - начална концентрация на мономер и ток; [I] - първоначалната концентрация на инициатор; р = 1 - [М] / [M0] - степента на превръщане на мономера; п - броят расте в макромолекулата. При започване на полимеризация п-С4 Н9 Li п = 1; в случая, където се появява етапа на започване електронен трансфер и образуването на йонни радикали, п = 2.
Дневна йонна полимеризация се използва в промишлеността за подготовката на блок-кополимери. Общ метод се състои в това, че в края на полимеризацията на един мономер с други мономер се добавя към жив вериги. В някои случаи, редът е важна, т.е. последователност на полимеризация на различни мономери. По този начин, живеещи полистиренови вериги могат да инициира полимеризацията на метил метакрилат, но не и обратно. От това следва, че има само два и триблоков (в зависимост от инициатора) блок кополимери на тези мономери. Като цяло, чрез последователно дневна анионна полимеризация на различни мономери могат да бъдат получени многоблокови кополимери, съдържащи различни блокове. Най-известните от блокови съполимери са така наречените термопластични еластомери. където една единица се отнася до еластомери, друг - за пластмаси. Термопластични еластомери притежават необичайни свойства на комплексните междинни свойства между гума и пластмаси. Сред най-често срещаните термопластични стирен блок съполимери с бутадиен и изопрен.
Ефект на условия на процеса на скоростта и степента на полимеризация
Известно е, че анионната полимеризация обикновено се провежда в разтворители. В зависимост от естеството на разтворителя (главно на своята полярност), инициатор или иницииращия комплекс различно солватирана разтворителя. В резултат на йонни двойки имат различна степен на отделяне, съответно, различни координатни мономер в своята област и да инициира процеса на полимеризация. При висока полярност разтворител. и следователно, неговата висока солватиране способност, разделяне на йонна двойка и образуването на свободни аниони. дейността на които е стотици пъти по-висока от йонни двойки в реакции растеж верига. Въпреки това, тази способност се губи координиране йонна двойка и редовността е нарушен макромолекулярно структура.
тип разтворител засяга етапа на прекъсване на веригата и като резултат на молекулното тегло на полимерите. Например, по време на полимеризацията на изопрен и бутадиен в толуен (който лесно влиза в реакция прехвърляне верига), молекулното тегло е много по-ниска, отколкото в бензол:
активиране енергия странични реакции (прехвърляне верига и подобни в разтворител, в случая на вещества с подвижна водороден атом, например, толуен) е обикновено по-висока от енергията на веригата; следователно намаляване на температурата обикновено насърчава потискане на странични реакции.
От голямо значение на скоростта на полимеризация от естеството на йон на алкален метал. обикновено прикове увеличения темп с увеличаване на йонната радиус на катиона. Солватиране способност на разтворителя при максималните солватиране органолитиеви съединения поради малкия радиус йонен литий и намалява в серия от алкалните метали: Li +> Na +> К +> Rb +> Cs +. метал-въглеродна връзка в полярността е обратно пропорционална, т. е. Ли-C полярност връзка минимално и защото малката йонен радиус на Li +. Това допринася за по-добро съгласуване мономер в комуникационни Li-С връзки, за разлика Na-С и К-С, когато механизмът за полимеризация е в близост до чист анион. В съответствие с изложеното по-горе, скоростта на полимеризация е минимално за литиев производни катализатори, но с превръщането на мономера и е в близост до максимум 100%.