стойности алкохол плътност и примери за задачи
Метанол, етанол и пропанол се смесва с вода във всякакви пропорции. С нарастването на молекулното тегло на разтворимостта на алкохол в неговата ода пада рязко. По-високите алкохоли са практически неразтворими във вода.
По-ниски алкохоли имат характерен алкохолна миризма, миризмата на средна хомолози силни и често неприятни. Висши алкохоли, имат почти никакъв мирис. Третични алкохоли плесен има специална характерна миризма.
Долна гликоли - вискозна безцветна течност, без мирис; лесно разтворим във вода и етанол, има сладък вкус.
Алкохоли имат ненормално високи точки на кипене в сравнение с класове на органични съединения, такива като алкани, халоалкани, тиоли, амини. Например, точката на кипене на етанол 78 о. докато хлороетан - 13 ° С, и етан - 88.5 ° С Тези разлики се дължат на структурни характеристики алкохоли.
химическия състав и плътността на алкохол
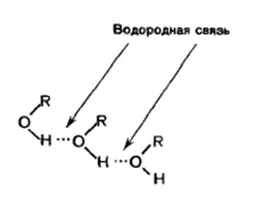
кислороден атом в молекулата на алкохол има висока Електроотрицателност и дърпа S-електронна плътност на връзките свързани атоми, по-специално водороден атом. Съобщение O-H в молекулата на алкохол е силно поляризиран в R → О ← Н. Плътността на електрон на водородния атом се намалява. Поради това може да взаимодейства с неразделен електронна двойка на кислородния атом на друга молекула на алкохол. Между две молекули възниква нековалентна връзка водород (водородна връзка изобразяват графично точките направени). Молекули свързани чрез водородни връзки да се образува сътрудници: