Стареене и рак - естеството на рак
Според съвременните концепции, възпаление играе основна роля в генезиса на почти всички, свързани с възрастта заболявания, които в крайна сметка ще доведе до тялото на смърт. Оказа се, че старите клетки, от една страна, да действа като туморен супресор (защото необратимо престане да се разделят и да се намали рискът от трансформация на околните клетки), и от друга - специфичен метаболизма на възрастните клетки може да доведе до възпаление и дегенерация на съседен премалигнени на злокачествени клетки. Понастоящем клинични изпитвания на лекарства, които селективно се премахва старите клетки в тъкани и органи, като по този начин предотвратява дегенерация на органи и рак.
Човешкото тяло присъства в около 300 типове клетки, и те се разделят на две групи: може да се раздели и да се размножават (т.е., те са митотично компетентни), а други - пост-митотични - не разделени: е достигната в етап на диференциация на неврони, кардиомиоцити, зърнеста бели кръвни клетки и др.
В телата ни има подновяване тъкани в които има басейн на непрекъснато делящи се клетки, които заменят изразходвани или умиращи клетки. Такива клетки са в чревните крипти, базалния слой на епитела на кожата, в костния мозък (хематопоетични клетки). обновяването на клетките може да бъде доста интензивен. така, в панкреаса на тъканни клетки съединителната се заменят на всеки 24 часа, на стомаха мукозните клетки - на всеки три дни, белите кръвни клетки - на всеки 10 дни, клетките на кожата - на всеки шест седмици, около 70 грама на малки чревни пролифериращи клетки се отстраняват от тялото дневно.
Стволовите клетки съществуват в почти всички органи и тъкани, могат да се разделят за неопределено време. регенерирането на тъкани, поради разпространението на стволови клетки, които могат да не само акции, но и да се диференцират в клетки на тъканта, което се случва на обновлението. Стволовите клетки съществуват в миокарда в мозъка (в хипокампуса и в обонятелния) и в други тъкани. Тя притежава голямо обещание за лечение на невродегенеративни заболявания и инфаркт на миокарда.
Непрекъснато се актуализира, тъкан от помощ, за да се увеличи продължителността на живота. В делящи се клетки настъпва подмладяване тъкан, нови клетки пристигат на мястото на нараняване, докато по-интензивно ремонт (намаляване на увреждане на ДНК) и евентуално регенериране на тъканно увреждане. Не е изненадващо, че при гръбначните животни е значително по-висока продължителност на живота в сравнение с безгръбначни - същите насекомите, които при възрастните клетки не се делят.
Но в същото време за подновяване тъкани податливи на хиперпролифериране, което води до образуването на тумори. включително - ракови х. Това се дължи на смущения регулиране на клетъчното деление и повишена честота на мутагенеза в активно делящи се клетки. Според съвременните концепции, към клетъчна неоплазия придобита собственост, тя се нуждае от 4-6 мутации. Мутациите са редки, и с цел да се превърне в ракова клетка - се очаква да е човешки фибробласти - трябва да се извършва на около 100 дивизии (като брой дивизии обикновено се случва при хора относно възрастта на 40 години).
За да се предпази от себе си, в тялото за образуване на специални клетъчни механизми на туморната супресия. Един от тях - репликативни стареене клетки (senestsentsiya), състоящи се в участък необратимо спиране клетки в G1 фаза на клетъчния цикъл. С остаряването, клетката спира разделяне, той не реагира на фактори на растежа и става устойчив на apotozu.
Hayflick граница
застаряването на явлението за първи път е открита през 1961 г. от Леонард Hayflick и колегите му върху културата на фибробласти. Установено е, че клетките в културата от човешки фибробласти при добри условия ограничават живо време и в състояние на удвояване приблизително 50 ± 10 пъти, - и че редица става известен като граница Hayflick. Преди откриването на Hayflick доминиран от мнението, че клетките са безсмъртни, и застаряването и смъртта - тя е собственост на организма като цяло.
Тази концепция се счита неопровержимо до голяма степен благодарение на експерименти Карел, които се поддържат културата на пилешки сърдечни клетки в '34 (тя беше хвърлена след смъртта му). Въпреки това, както се оказа, за безсмъртието на културата Карел беше един артефакт, като с фетален серум, който е добавен към хранителната среда за растежа на клетките, за да се падне ембрионални клетки (и, най-вероятно, култура Карел вече далеч не това, което беше станала започващ).
Наистина са безсмъртни ракови клетки. По този начин, HeLa клетки, изолирани през 1951 г. от цервикален тумор Хенриета Липсва, все още се използват цитолози (по-специално в по полиомиелитна ваксина е разработена от HeLa клетки). Тези клетки дори били в космоса.
Както се оказа, срокът Hayflick варира в зависимост от възрастта: по-старите лицето, толкова по-малко брой пъти, два пъти, като клетъчна култура. Интересното е, че замразените клетки в размразяване и последващо отглеждане на тютюн, не забравяйте, броят на разделения преди замразяване. В действителност, има "контра разделения" в рамките на клетката, а при достигане на определен лимит (Hayflick лимит) клетка спира да се раздели - става застаряващ. Стареещи (стари) клетки имат специфична морфология - те са големи, плоски, с големи ядра, силно вакуолен, те променят генна експресия профил. В повечето случаи те са устойчиви на апоптоза.
Въпреки това, процесът на стареене не може да бъде намалена само за стареенето на клетките. Това е значително по-сложен процес. Старите клетки има в едно младо тяло, но те са малко! Когато възрастта стареещи клетки се натрупват в тъканите, като се излиза дегенеративни процеси, които водят до възрастта зависими заболявания. Един от факторите на тези заболявания - така наречените сенилна "стерилен" възпаление, което е свързано с експресията на провъзпалителни цитокини стари клетки.
Друг важен фактор на биологичното стареене - структурата на хромозомите и техните съвети - теломерите.
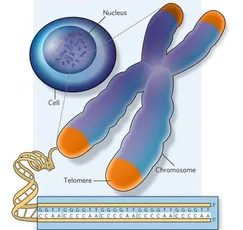
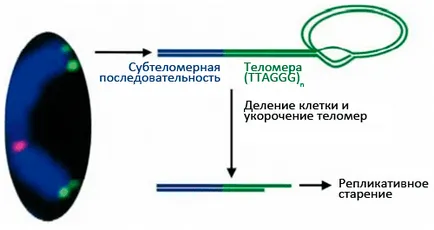
Многократното деленето на клетките в отсъствие на теломеразна активност води до скъсяване на теломерите и репликативна стареене.
Дължината на теломерите и скоростта на намаляване зависи от възрастта. При хората, теломерната дължина варира от 15 хиляди базови двойки (Kb) при раждането до 5 KB при хронични заболявания. дължината на теломерите е максимална при 18-месечно дете, а след това бързо пада до 12 KB на възраст до пет. След това скъсяване намалява проценти.
Теломерите дисфункция, което се случва, когато се скъси или неизправност shelterina активира р53. Това транскрипционен фактор причинява клетката до състояние senestsentsii или индуцира апоптоза. При липса на р53 развива хромозома нестабилност характеристика на човешки карциноми. Мутации в р53 се откриват в 50% от аденокарциноми на гърдата, и в 40-60% от случаите на колоректален аденокарцином. Ето защо, p53 често е наричан "пазителят на генома".
Теломеразата се активира в повечето тумори от епителен произход, които са характерни за по-възрастните хора. Смята се, че възобновяването на теломеразата - важен етап в злокачествени процеси, тъй като позволява на раковите клетки да "игнорира" на границата Hayflick. Теломерите дисфункция насърчава хромозомни аберации и М, в отсъствие на р53 често води до злокачественост.
Фигура. Връзката между стареенето на клетките и стареене.
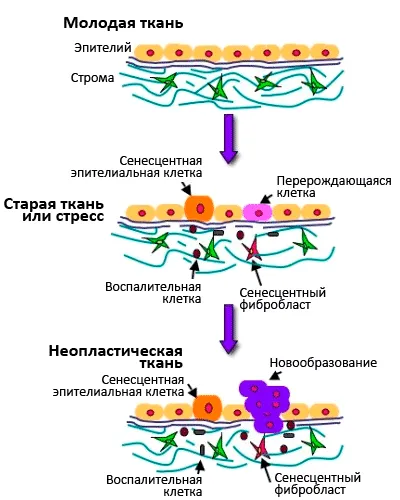
За да се разбере на молекулярните механизми са преход към състояние на стареещи клетки, аз ще ви напомня как клетъчното делене.
процес клетъчното размножаване се нарича пролиферация. Жизненият цикъл на клетките от разделяне се отнася до разделяне на клетъчния цикъл. процес пролиферация се регулира както клетката - автокринни фактори на растежа - и микросреда - паракринни сигнали.
Пролиферацията активиране възниква през клетъчната мембрана, в които има рецептори, наблюдение митогенни сигнали - това е главно растежни фактори и клетка-клетка контакт сигнали. Растежни фактори обикновено имат пептидна природа (досега известни са около 100). Това, например, получен от тромбоцити растежен фактор, който участва в образуването на тромби и заздравяване на рани, епителен растежен фактор, различни цитокини - интерлевкини, тумор некрозис фактор, колония стимулиращи фактори и т.н. След активирането на клетъчната пролиферация идва от фаза G0 покой и започва на клетъчния цикъл.
Клетъчният цикъл се регулира от циклин-зависими кинази, различни за всеки етап от клетъчния цикъл. Те се активират от циклини и инактивира редица инхибитори. Целта на такава сложна регламент - да се осигури синтеза на ДНК с най-малък брой грешки, и на дъщерните клетки имат абсолютно идентични генетичен материал. Проверява коректността на ДНК се извършва в четири "тестови точки" цикъл: Ако се открият грешки, клетъчния цикъл е спрян и е включен ремонт на ДНК. Ако нарушения на структурата на ДНК не може да се коригира - клетъчния цикъл продължава. Ако не - в клетката е по-добре да се "самоубият" (апоптоза), за да се избегне възможността да се превърне в рак.
Молекулните механизми, водещи до необратими клетъчния цикъл арест контролирано тумор супресорни гени, включително р53 и PRB, свързани с инхибитори на циклин-зависими кинази. Подтискане на клетъчния цикъл в G1 фазата от следващата протеин р53, инхибитор действа чрез циклин-зависима киназа инхибитор р21. р53 транскрипционен фактор активира от увреждане на ДНК и неговата функция е да се премахнат от пул от клетки реплициращи тези, които са потенциално онкогенни (оттук псевдоним на р53 - "настойник на генома"). Това мнение се потвърждава от факта, че р53 мутации се срещат в
50% от злокачествен opoholey. Друга проява на p53 активност е свързана с апоптоза най повредени клетки.
Senestsentsiya клетки и възрастта зависими заболявания
Стареещи клетки се натрупват с възрастта и допринасят за свързани с възрастта заболявания. Те намаляват пролиферативен капацитет на тъкани и разрушават басейна на стволови клетки, което води до тъкан дегенеративни нарушения и намалява капацитета за възстановяване и обновяване.
Стареещи клетки се характеризират чрез експресия на специфични гени, те секретират цитокини и металопротеинази, които разрушават извънклетъчната матрица. Оказва се, че старите клетки осигуряват бавен сенилна възпаление и натрупване на стари фибробластите в кожата причинява свързана с възрастта загуба на способността за лекуване на рани. Старите клетки и стимулират пролиферацията и ракообразуване на предракови съседните клетки чрез секретирането на епителен растежен фактор.
Стареещи клетки се натрупват в много човешки тъкани, присъстват в атеросклеротични плаки, в язви на кожата, в артритни стави, както и в доброкачествени лезии хиперпролиферативни и пренеопластични простатата и черния дроб. След облъчване, някои ракови клетки да станат държавните senestsentsii, чрез което се осигурява рецидив.
По този начин, клетъчни стареене демонстрира ефекта на отрицателен pleiotropy, същността на която е, че доброто за младия организъм, може да бъде лошо за старите. Най-ярък пример - процеса на възпаление. Тежка възпалителна реакция допринася за бързото възстановяване на млад организъм инфекциозни заболявания. В напреднала възраст същото активни възпалителни процеси, водещи до свързани с възрастта заболявания. Сега се приема, че възпалението играе роля в почти всички свързани с възрастта заболявания, невродегенеративни оттогава.
Оказва се, един парадокс: застаряването на клетките в организма млад предпазва от рак, но в старите - това помага!
Регистрирайте се наново и да получите ексклузивна информация за най-новите изследвания за рак на брояч. Информацията е достъпна само за абонати.