Са амини а) метиламин; б) диметил амин; в) триметил амин
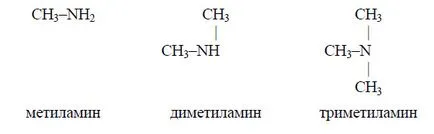
Основните свойства на амини, като амоняк, поради присъствието на азотен атом свободна електронна двойка. Следователно, по-висока плътност на електрони при азотния атом, с по-изразено основните свойства на амина. В молекула на метиламин азотен атом е свързан с метилов радикал. Електроотрицателност на водород е по-малко от въглерод и азот, така че преместването на електрони от три водородни атоми към въглероден атом, а след това - към азотния атом (показано със стрелки)
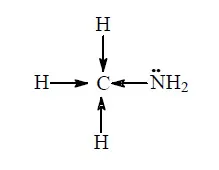
В резултат на плътността електрон на азотния атом, се увеличава и метиламин е силна база от амоняк. В молекула на диметиламин водороден атом свързан към две метилови радикали, и се прехвърля към азотен атом, с електронен плътността на шест водородни атоми, обаче, плътността електрон на азотните атоми в сравнение с молекулата на метиламин, диметиламин и е по-силна база от метиламин. Накрая, в молекула триметиламин три метилов радикал при азотния атом, и електрона е изместен към азотния атом на девет водородни атома. Ето защо, триметиламин е, от своя страна, по-силна база от диметиламин. Така, метиламин основни свойства са най-слабите, докато триметиламин - трудното.