Практическа работа № 8 стр
1) За да се различава вещества: а) MgCl2; б) NaOH; а) Na2 CO3; ж) NaNO3;
а) действия. Ние сме добавяне на всички вещества RR солна киселина. Наблюдения. В една от епруветките се освобождава газ. Реакция уравнение:
Изводи: натриев карбонат, съдържащ се в тази тръба, като протича качествена реакция за карбонат йон. б) действия. Останалият материал се разтваря във вода и към този разтвор се прибавя на фенолфталеин. Наблюдения. В една от тръбите разтвор превръща розово. Реакция уравнение:
Заключения: Разтвор на фенолфталеин става розово в алкална среда (под действие на йони ОН) -, така че в тази тръба е натриев хидроксид. в) действия. Към останалия разтвор се прибавя разтвор на сребърен нитрат (I). Наблюдения. В една от епруветките се образува бяла утайка. Реакция уравнение:
Изводи: Това качествен отговор на хлорни йони, следователно, тази тръба е магнезиев хлорид. ж) действия. Към останалия разтвор се добавя концентрирана сярна киселина и парче от мед. Отопляем. Наблюдения. При условие газ на кафяв цвят, медта се разтваря и разтворът стане син. Реакция уравнение:
Заключения: Реакцията е качествен нитрат йон, следователно, тази тръба е натриев нитрат.
2) разлики вещества: а) СаСО3; б) Ba (NO3) 2; а) Na 2SO 4; г) Na2 S
а) действия. Ние сме добавяне на всички вещества RR солна киселина. Наблюдения. В една от епруветките се освобождава и газ без мирис, а другият - с неприятна миризма. Реакция уравнение:
Заключение: Ин витро, в които стана без мирис газ съдържа
т. к. отговор качество карбонат йон. Когато газ-effusing лошомиришещи
съдържа натриев сулфид. б) действия. След разтваряне, останалите вещества във водата добавяне на разтвор на натриев сулфат. Наблюдения. В една от епруветките се образува бяла утайка. Реакция уравнение:
Изводи: Качествен реакция на бариев йон, следователно, в епруветката - бариев нитрат. в) действия. Към останалата р-Ру RR добавяне на бариев хлорид. Наблюдения. Бялата утайка. Реакция уравнение:
Изводи: Това качествена реакция сулфат йон, следователно, в тръбата за - натриев сулфат.
3) докаже, че издаденото материал - алуминиев сулфат Al2 (SO4) 3
а) действия. Тя издаде решение броене добавяне на бариев хлорид. Наблюдения. Бялата утайка. Реакция уравнение:
Изводи: Това е качествен отговор на сулфат йон. б) действия. Към малко количество алкален разтвор, разтвор на вещество издадени. Наблюдения. Бяло желеобразна утайка. Реакция уравнение:
Изводи: Резултатът е образуването на неразтворима основа
чрез свързване йони
Следователно, в изпитваното вещество съдържа алуминиев йон. в) действия. Добавянето на излишък от основа. Наблюдения. Излишният алкален утайка се разтваря. Реакция уравнение:
Заключения хидроксид има амфотерни свойства: натриев mataallyuminat оформен. Това отново показва, че издаден веществото съдържа алуминиев йон.
4), за да се разграничат разтвори: NaCl, BaCl2. AlCl3
а) действия. Всички разтворът се прибавя р-р на натриев сулфат. Наблюдения. В една от тръбите на бяла утайка. Реакция уравнение:
Изводи: Това тръба съдържа бариев хлорид, като Тази реакция - от качеството на бариеви йони. б) действия. две оставащия разтвор се прибавя малко алкален разтвор. Наблюдения. В една от тръбите образувани желатинов бяла утайка. Реакция уравнение:
Заключения: В тази епруветка - алуминиев хлорид. в) действия. Няколко капки от оставащия разтвор въвеждат в пламъка на нихром дух лампа. Наблюдения. Flame става жълт. Заключения: В тази епруветка - натриев хлорид, като жълт пламък оцветени натриеви йони.
5) докаже, че FeSO4 кристали частично окислени и съдържа примес йони Fe 3+
Действия. Кристалите се разтварят във вода и добавяне на р-р
Наблюдения. Генерирани зелени и кафяви седименти. Реакция уравнение:
Изводи: Кафявата утайка - неразтворима основа
Той е зелен. Следователно, Оригинална
съдържащ оксиди на йони
6) Две колби дадени вода. В един от тях водата съдържа MgSO 4. и в другата - Са (HCO3) 2. Експерименти направено с помощта на който постоянно и временно твърдост могат да бъдат премахнати.
а) действия. Водата, съдържаща
добави RR
Наблюдения. Образува се бяла утайка. Реакция уравнение:
Заключение: Iona
причини постоянна твърдост на водата. Тази вода може да се смекчи чрез добавяне на разтвор на натриев карбонат, т. К. Това се случва, когато йон свързващ
б) действия. Водата, съдържаща
добави: Разтвор на
варно мляко, т.е. наситен разтвор
ври него. Наблюдения. Образува се бяла утайка. Реакция уравнение:
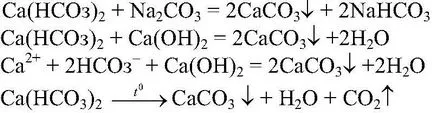
Изводи: Наличието на
Той причинява временна твърдост на водата. Тази вода може да се смекчи чрез добавяне на варно мляко или сода кипене, защото Всички тези процеси са придружени от образуването на
7) Извършване на превръщане:
а) Fe → FeCl2 → Fe (ОН) 2 → Fe (ОН) 3 → Fe (NO3) 3
1. действия. Чрез добавяне на железен прах солна киселина. Реакция уравнение:
2. действия. След отделянето на газ, добавя алкален разтвор. Реакция уравнение:
3. действия. Към остатъка се добавят някои г-ра водороден пероксид. Реакция уравнение:
4. действия. Към остатъка се прибавя разтвор на азотна киселина реакционни уравнения:
б) Al → Al (SO4) 3 → Al (ОН) 3 → NaAlO2
1. действия. За повече пелети
добави RR
Реакция уравнение:
2. действия. След отделянето на газ добавяне на алкален (на капки). Реакция уравнение:
3. действия. Към остатъка се прибавя излишък от алкален. Реакция уравнение: