Лекция 12 Първи закон на термодинамиката
Прилагане на първия закон на термодинамиката
12.1. Izoprotsessy. Работа в izoprotsessah
Сред равновесни процеси, които се случват в термодинамична система, изолиран izoprotsessy - равновесни процеси, в които един от основните параметри се поддържат постоянни.
1. изохорен процес (
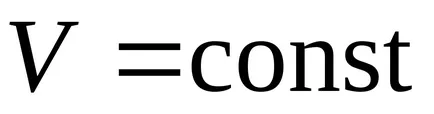
1-3 - изохорен охлаждане; 1-2 - изохорен отопление. при
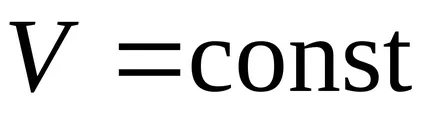
.
От първия закон на термодинамиката, така че първият закон на термодинамиката при изохорен процес:
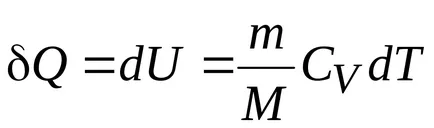
Топлината, действаща на газ в изохорен процес, има промяна (увеличение) на вътрешната енергия на системата.
2. изобарен процес (
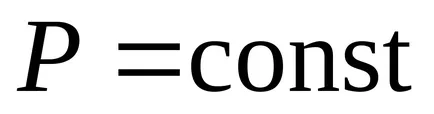
От първия закон на термодинамиката:
,
следователно, първият закон на термодинамиката при изобарен процес:
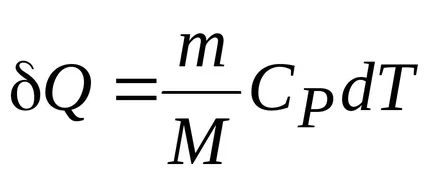
Работа при изобарен процес:
.
ако
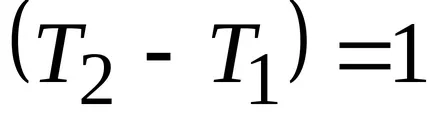
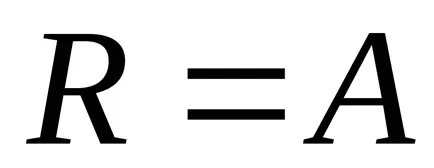
3. изотермична процес (
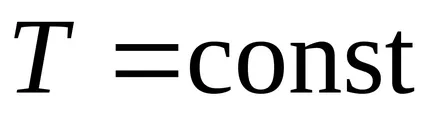
Първият закон на термодинамиката :. при
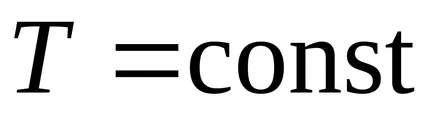
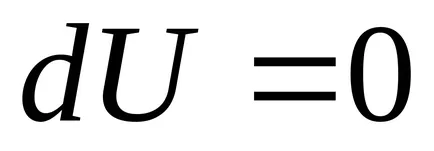
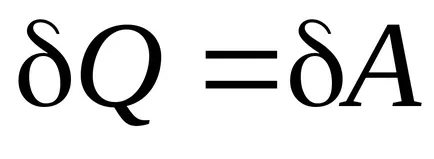
Работата на изотермични разширение:
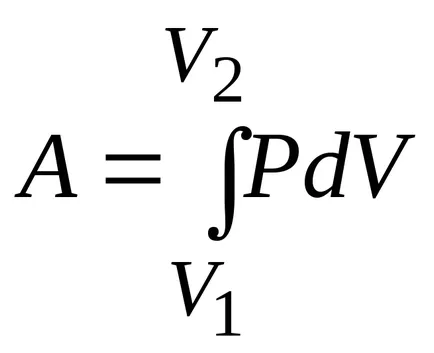
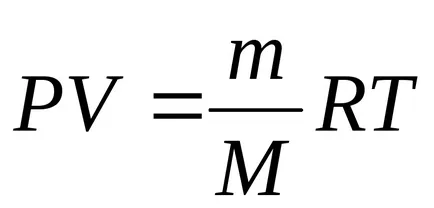
,
Затова работя в изотермичен процес:
.
Първият закон на термодинамиката за изотермичен процес:
.
Заключение. всички количеството топлина, действаща на газа се консумира, за да ги накара да работят срещу външни сили.
За време газ температурата се намалява, за газа в изотермични процес е необходимо да се предоставят на количеството топлина, еквивалентен на външния експанзия.
12.2. адиабатен процес
Izoprotsessam К може да се дължи на адиабатен процес - процес, при който не е топлообменът с околната среда.
Пример. въздух компресия и напрежение в звуковата вълна, работа на двигателя с вътрешно горене.
Първият закон на термодинамиката. системата действа за сметка на вътрешната енергия на системата.
изразяване
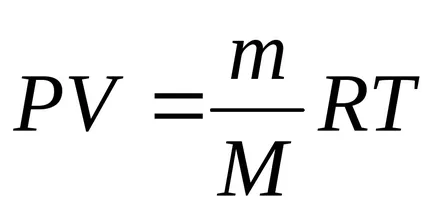
Категории (12.2) до (12.1):
,
;
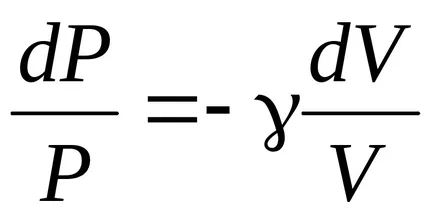
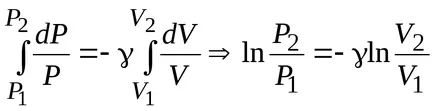
.
уравнение на Поасон
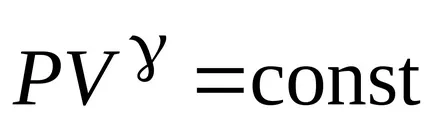
Уравнението Менделеев-Clapeyron и изразяване на налягането от него P., откъдето уравнението на Поасон в координатите (ТА V).
Express обем Менделеев-Clapeyron уравнение :, Поасон otkudauravnenie в координати (Т Р).
Уравнението на адиабатен метод:
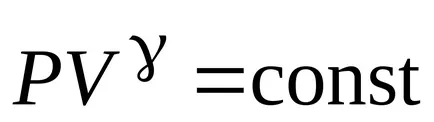
;
,
където
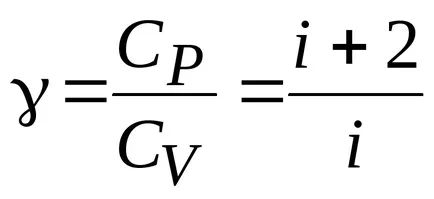
Графика адиабатно - графика, показваща връзките между параметрите на състоянието на идеален газ при
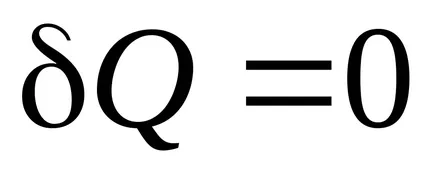
adiabat
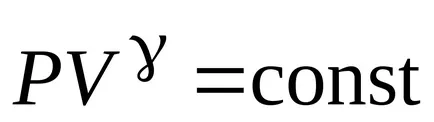
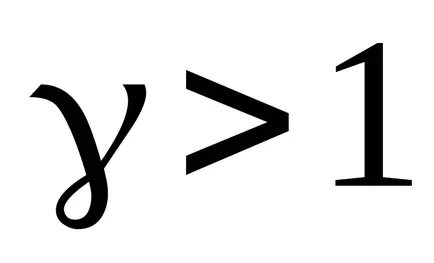
Работа газ в адиабатен процес.
.
Работа с адиабатен процес:
Заключение: ако газът се разширява адиабатно от


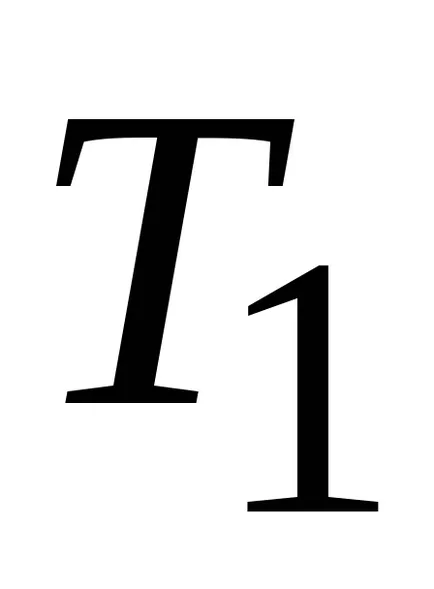

;
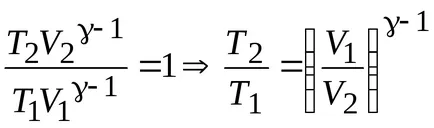
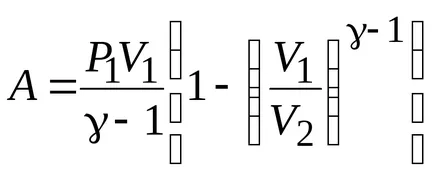
Работа по време на процеса на адиабатно разширение по-малко от за изотермично разширяване. Това се дължи на факта, че когато адиабатно разширение охлаждане на газ, докато при температура изотермично разширяване се поддържа постоянна поради притока от външната страна на еквивалентно количество топлина.
Заключение: счита изохорен, изобарен, изотермичен и адиабатни процеси имат една обща черта - те се срещат при постоянна топлинен капацитет.
Процес, при който специфичната топлина е постоянна, се нарича политропно. Политропен уравнение.
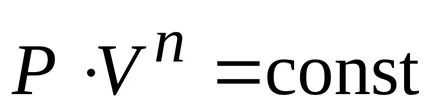
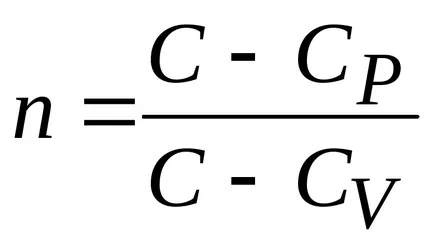
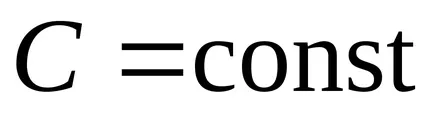
Заключение. всички тези процеси са специалните случаи на политропно процес.
Координатите R. V polytrope - графика на параметрите на състоянието в
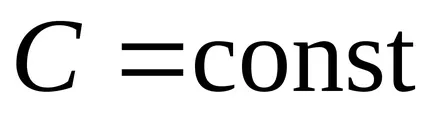
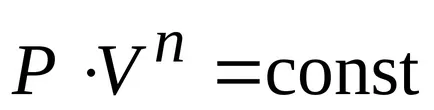
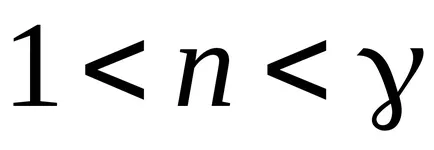
Какво е izoprotsessy? Izoprotsessy Какво искаш да знаеш?
Формули за изчисляване на работата на различни izoprotsessah и да се покаже как техните оси в графики р, V е изобразен, тази работа.
Равен (на равнината Р, V) и адиабатно изотерма. Обяснете защо адиабатно с увеличаване на V пада по-стръмен от изотерма?
Извлекат уравнението на Поасон. Каква е адиабатно индекс?
Пак посредством газ при адиабатно разширение работи срещу външни сили? Какво се случва с температурата на адиабатно разширяване идеален газ?
Какво се нарича политропно процес?
Загрява се при процеса на изотермични е
Тегло 16гр кислород е при налягане от 300 кРа и температура от 27 ° С. След нагряване при постоянно налягане на обема на газ се 10 литра. Намерете сумата на топлинна енергия, произведена газ, промяната във вътрешната енергия на газа и извършената работа по време на газ разширяване. [6142,5 J; 4387.5 J; 1755 J].
Двуатомен газ съобщава броя на 2,093 кДж на топлина. Газ разширява изобарно. Намери разширяване на работа на газ. [598 J].
Азот маса m = 56гр, разположен при нормални условия, се разширява адиабатно, обемът на газ се удвоява. Определяне на: 1) промяна на вътрешния енергиен ΔU газ; 2) работа разширяване газ. [ΔU = - 2,75 кДж; А = 2.75 кДж]