Глава 4 на втория и третия закон на термодинамиката
Ентропия (от grech.entropia- обрат, трансформация) - концепцията за първи път е въведена vtermodinamike да се определи мярка за необратимо разсейване на енергия. Ентропията vstatisticheskoy физика - мярка на вероятността за реализиране на макроскопско състояние, vteorii информация - мярка за несигурността на експеримента (тест), който може да има различни резултати. Тези тълкувания на ентропия имат дълбока вътрешна връзка.
1 ентропията. Термодинамични ентропия смисъл
По същество всички процеси в макросистеми са необратими.
Възниква въпросът: каква е причината за необратимост? Това е особено странно, като се има предвид, че всички закони на механиката са обратими във времето. И все пак, никой не е виждал, например, да се прекъсне една ваза спонтанно възстановени от отломките.
Решението на този сложен проблем дойде с откриването на нов термодинамична количество - ентропия - и разкриване на неговото физическо значение.
Концепцията за ентропия за първи път е въведен от Р. Клаузиус през 1862. Той е един от най-удивителните открития, направени "на върха на писалката", т.е. теоретично.
Въпреки това, както и липсата на инструменти, които ще измерват ентропията на веществото, това понятие се оказа изключително ползотворно.
ентропия

Необходимо е да се обърне внимание на функцията на тази формула. Както е известно,
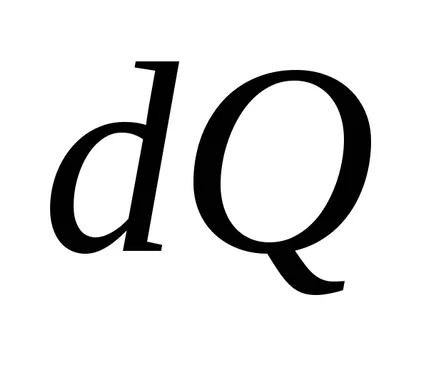
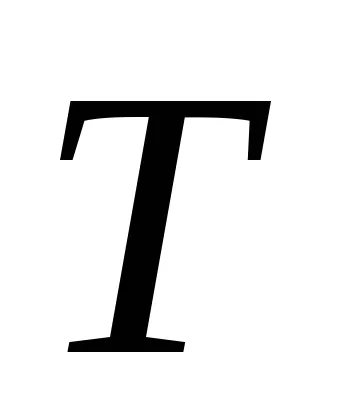


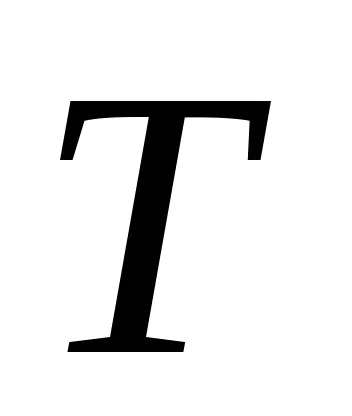
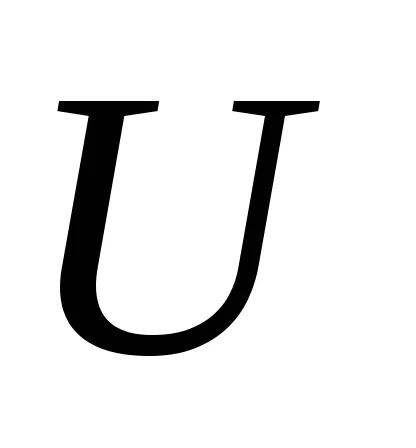
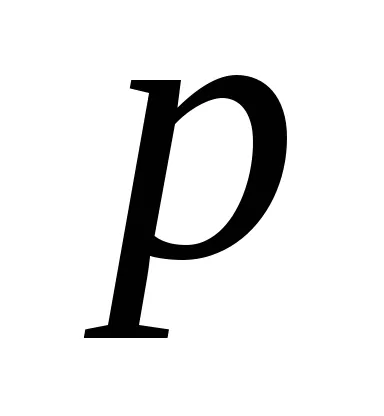


По този начин, при равновесие при температура на пренос на топлина
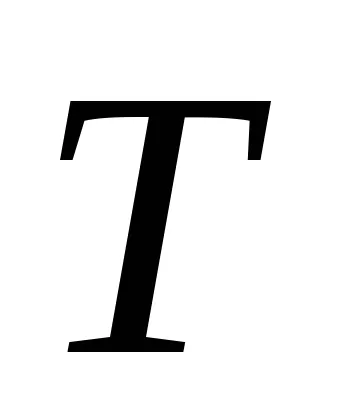
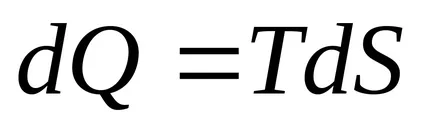
Първият закон на термодинамиката може да се запише като:
Нека първоначалното състояние на организма с температура
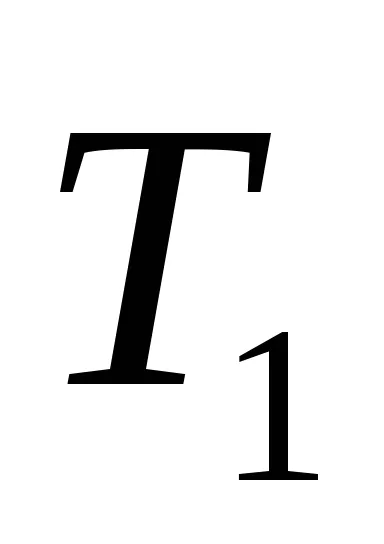
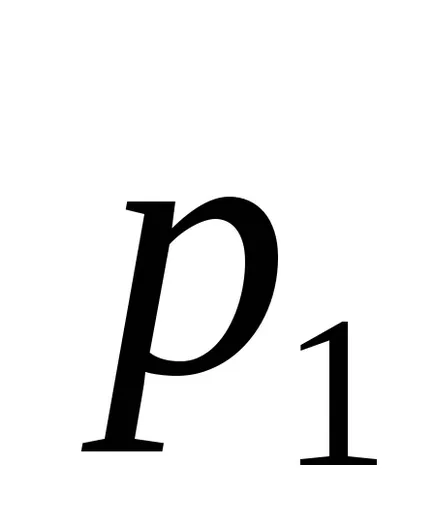
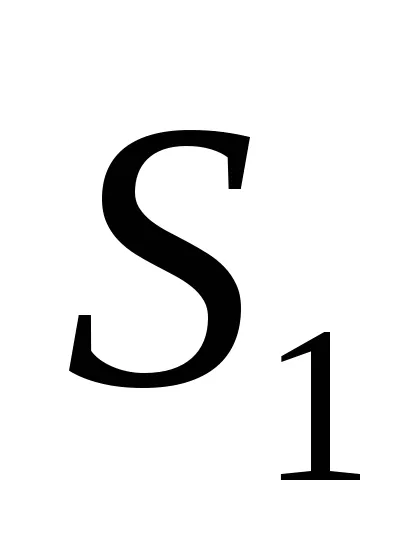
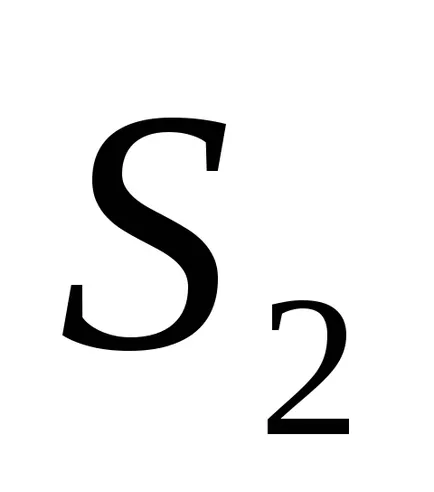
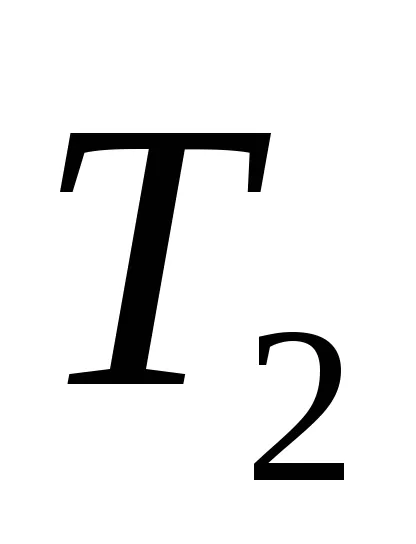
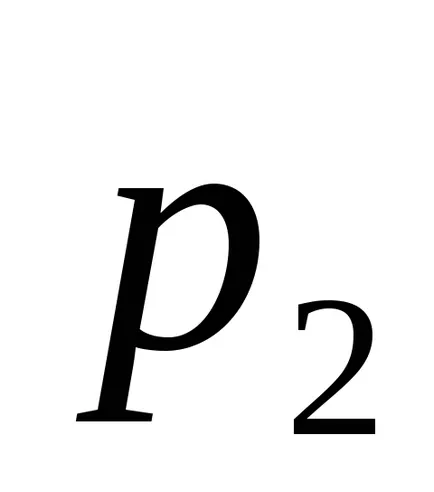
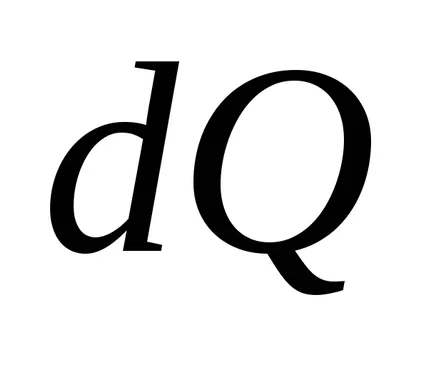
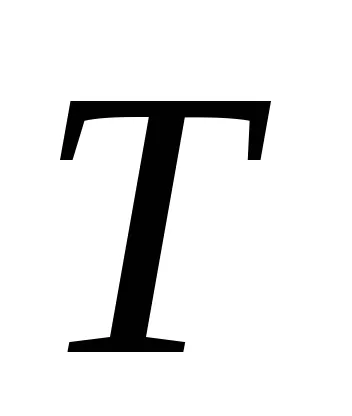
Тогава ентропията
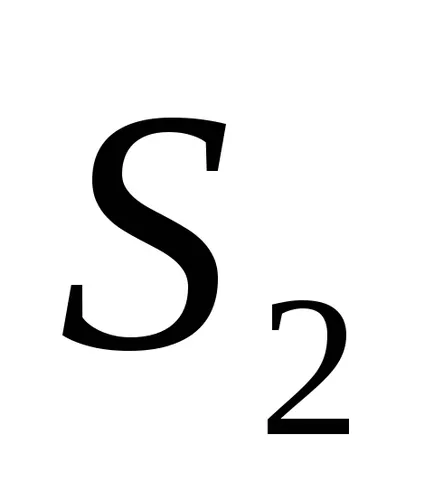
По-специално, за процеса на изотермични (
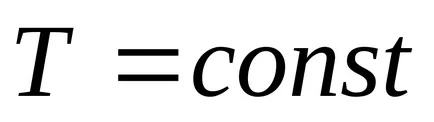
Тъй ентропията е функция от състоянието, интеграл (4.3) не зависи от формата на кривата представлява процес, но определя само от началните и крайните страни, т.е. граници на интеграция.
1) ентропията - стойността на добавката: ентропията на система от няколко тела, е сумата на ентропията на всеки орган
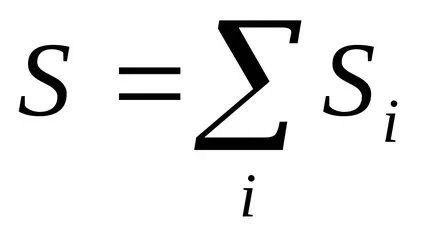
2) равновесие обработва без топлопредаване ентропията не се променя.
В адиабатен процес
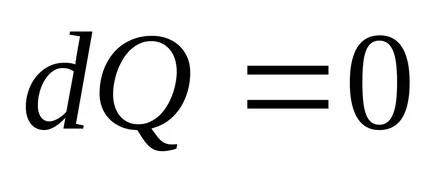
Следователно, съгласно формула (4.1) в равновесие адиабатно процеса
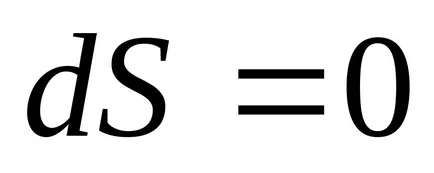
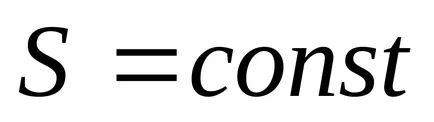
3) при постоянен обем, ентропията е монотонно нарастваща функция на вътрешната енергия на тялото.
В действителност, когато
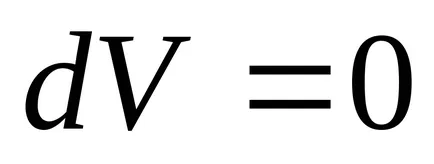
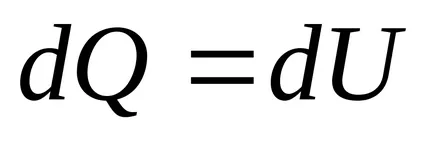
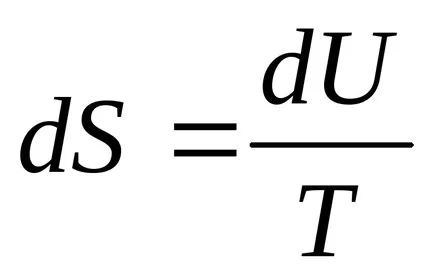
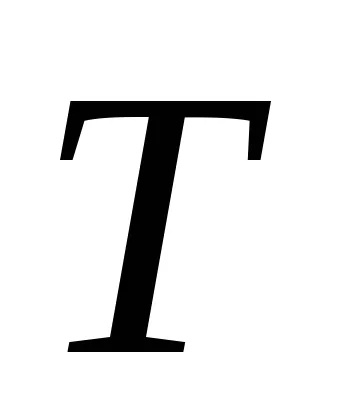
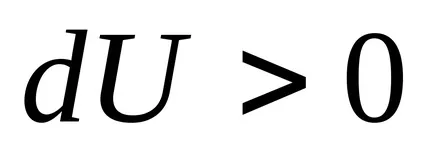
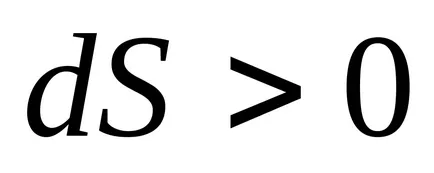
4) ентропията се определя само до произволна константа.
В действителност, според (4.3) можем да изчислим само разликата в ентропии

5) Насочване вътрешен енергиен като функция на силата на звука и ентропията
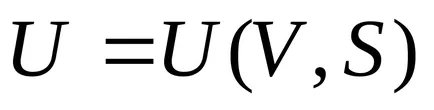
В действителност, според правилото за диференциране на функция на две променливи
.
Като се има предвид (4.2), че
,
Тези уравнения определят температурата и налягането на вътрешната енергия
Имайте предвид, че равенството
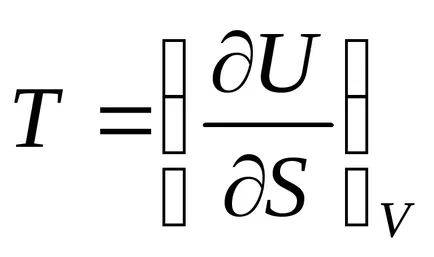
абсолютна температура