Експлозиите на газ въздушни смеси
Ако може да се възпламени горими газова смес е в затворено пространство като вътрешен, устройството или тръбопровода достатъчно голям диаметър, при възникване на всяка точка на отворен обем на пламък, електрическа искра или нагрява тяло, чиято температура е достатъчна за запалването на газ, експлозия възниква , Експлозията е явление изключително бързо запалване и изгаряне на всички веднага достъпно смес обем газ. Взривят не може само газово гориво. При определени обстоятелства, може да се появят експлозии смеси от пари и течни горива с въздух и прах във въздуха на твърди горива.
Бързото изгаряне на горивото в експлозията са придружени от много бързо повишаване на температурата и, като следствие,
рязко увеличение на налягането от загрят газ. Това е почти мигновен и внезапно повишаване на налягането в затворен обем, който се занимава с горивната смес преди експлозията, може да доведе до катастрофални последици. Налягане, генерирана от експлозия на газ-въздушни смеси може да бъде до 0,7 - 0,8 МРа, ако сместа на експлозията са при нормално атмосферно налягане. Ако сместа газ преди експлозията вече при повишено налягане, налягането на експлозията е толкова висока, колкото налягането на сместа е - над нормалното. В експлозии налягане газ кислород смеси могат да бъдат значително по-високи, отколкото при експлозии на газ въздушни смеси.
Големината на налягането развива в експлозията на газовата смес, могат да бъдат определени като се използва формулата:
Rvzr където - абсолютното налягане по време на експлозията, MPa;
Rnach - първоначално абсолютно налягане на сместа MPa;
tvzr - температури развиващи се по време на експлозията, които са на границата на максималната стойност;
Tstart - началната температура на газовата смес; ° С;
m - брой на обем (m 3) на газ от продуктите на горенето с вземайки предвид атмосферния азот;
п - номер на обем (m 3) въздушно-газова смес на експлозията, като се вземат предвид атмосферния азот.
Тъй като максималната температура на горене почти не се постига, но смес от газ и въздух само може случайно да бъде такава, че няма да има излишък от него, нито липса на въздух в сравнение с теоретичния размер, действителното налягане в експлозии на газ ще бъде по-малко от максимално възможно, т д. 0.7 -. 0,8 МРа. Особено опасни срещу експлозия газове са по-ниски LEL, тъй като в този случай сместа от газ се образува по-скоро в състояние да възпламени при равни други условия. В близки стойности взривоопасни газове две опасно един, който има широка област експлозивна и под температурата на запалване.
За въглеводородни газове Cm · реакция Нп химически уравнение изгаряне на кислород под формата
т-, където броят на въглерод въглеводороден газ;
п - брой водородни атоми в газа;
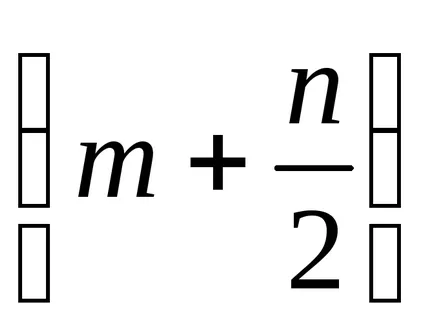
Съгласно формула (8), уравнението за изгаряне на горими газове ще бъде:
От практическа гледна точка газ кислород горене не се взема в чист вид, а като съставна част на въздуха.
Тъй въздух се състои от обем от 79% азот и 21% кислород обем кислород на изисква 100. 21 = 4,76 обем на въздух или 79. 21 = 3,76 обем азот.
По този начин, реакцията на горене на метан във въздуха може да се опише чрез уравнение на формата
От това уравнение е ясно, че за изгаряне на 1 м3 на метан изисква 2 м 3 от кислород и азот, или 2 7.52 + 7.52 = 9.52 m 3 на въздух (вж. Таблица 6).
Токсичните свойства и задушаване газове
Природният газ (метан, етан, пропан, бутан, и т.н.), различни от тези, които съдържат значителни количества от сероводород обикновено не са токсични. Въпреки това, при високи концентрации на природен газ във въздуха има липса на кислород до задушливи. Чрез понижаване на съдържанието на кислород в вдишвания въздух се наблюдават следните физиологични състояния: 17% - задух и сърцебиене, 12% - силно ограничено дишане, с 9% - припадък. Хомолози метан - етан, пропан, бутан, също се съдържат в природния газ да действа върху човешкото малко наркотик.
Таблица 6 - брой на кислород и въздух по време на горивните газове
Универсална газ уравнение на състоянието разгледахме в глава 3. В допълнение, погледнете в уравнението на състоянието на водата, с virial коефициентите
В това уравнение, за намален Z supercompressibility фактор на серия мощност. В, С, D - съответно двойни и тройни четворни virial коефициенти са функция само на температура и зависят до голяма степен от молекулни взаимодействия, при които едновременно се ангажират съответно две, три и четири молекули на газа. Определяне на supercompressibility virial коефициенти и коефициенти могат да бъдат по-точно само за газове, състоящи се от прости молекули, например, кислород, азот.
Според теорията кинетична молекулно с фактор вземе предвид силата молекулно Z. взаимодействие И ако Z <1 то преобладают силы притяжения если же Z> 1 е доминиран от отблъскваща сила при Z = 1 състояние на равновесие молекулно сили.
Фигура 1 показва supercompressibility фактор поведение вариация в зависимост от налягането при постоянна температура газ.
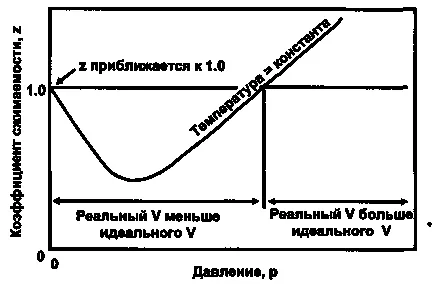
Фигура 1. Типичен съотношение промяна графика supercompressibility на налягане при постоянна температура
Най-широко определящ фактор на supercompressibility за смесите от полета за природен газ, газ при налягане до 70 МРа, получени по метода на определяне на графиката, показана на фигура 2. В този графика основа за конструиране на принципа на съответните страни, т.е. за същите стойности, дадени налягания и температури RPR Tcal различни вещества имат подобни стойности supercompressibility фактор Z.
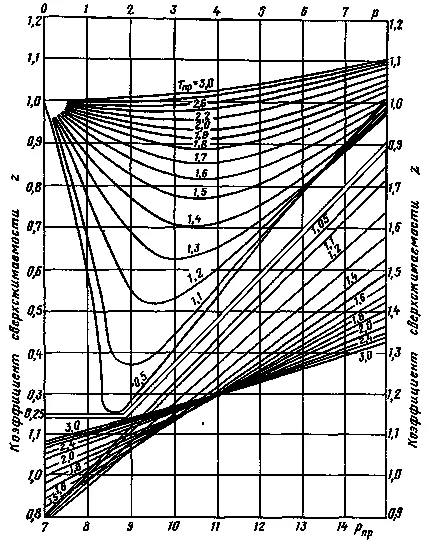
Фигура 2. Зависимост supercompressibility фактор Z природен газ от горното налягане и температура.
Методи за определяне на коефициента на supercompressibility Z е следното. Първоначално, Фигури 2 и 3 или формула (2) в зависимост от относителната плътност и състав на газа се определя srednekriticheskie налягане и температура, и за дадено налягане и температура.
Srednekriticheskie (pseudocritical) налягането и температурата на сместа може да бъде изчислен съгласно формула (2):
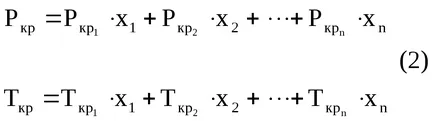
където x1. х2 ..., хп - обемни фракции на компонентите на състава на газ;
Rkr1. Rkr2 ... Rkrn - критични компоненти налягане;
TP1. TR2 ... TRN - критичната температура на компонентите.
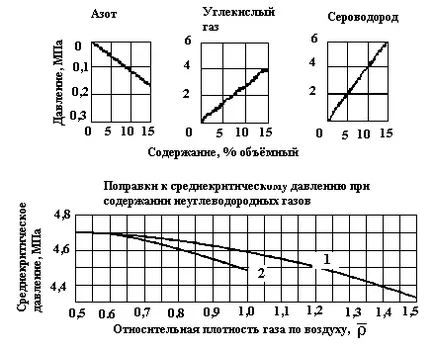
Фигура 3. Зависимост налягане srednekriticheskogo на относителната плътност на газа във въздуха: 1 - газови находища; 2 - газ кондензат полета (
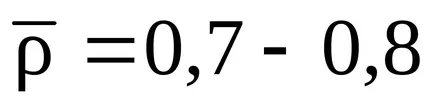
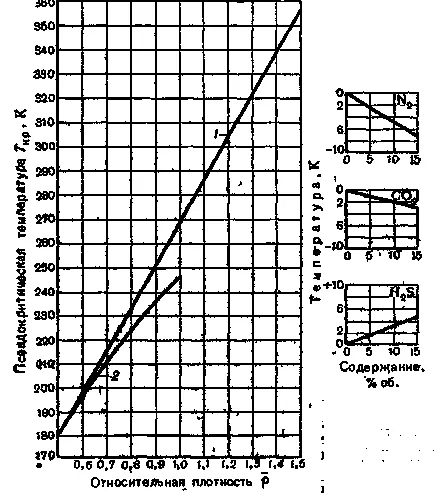
Фигура 4. Зависимостта температура srednekriticheskoy на относителната плътност на газа във въздуха:
1 - газови находища;
2 - поле газ кондензат ().
Когато съдържанието на N2 газ. СО2 и Н2 S над 15% от уравнение обем може да се използва вместо графиките да се определи и Тсг PCR (2).
След това зависимостта, показана на фигура 1 се определя и съответния RRP и TPR стойност supercompressibility фактор Z.
Таблица 1 показва данни за някои физикохимични параметри на компонентите, включени в природния газ.
Както вече споменахме, в условия резервоар в областта на кондензат са висококипящи въглеводороди (С5 + Н 12), които присъстват в състава на бензин, керосин и петролни фракции, кипящи при температури до 500 ° С маса фракция етан В и пропан - бутан фракция достигне 25%
Таблица 1. Основни свойства на компонентите на природния газ
В състава на високо кипене система въглеводород кондензат резервоар, съдържаща три химични групи въглеводороди: метан, нафтенови и ароматни, и техните връзки са много различни за различните депозити газ кондензат. Таблица 2 дава кратко описание на броя на газов кондензат депозити от ОНД.
на по-високо налягане за образуване и температурата. Трябва да се отбележи, че условията, при които се образуват отлагания могат да оказват съществено влияние върху модела.
В тази връзка, в природата могат да се срещнат три вида депозити кондензни газови - наситени и Ненаситената прегряване. За последния тип на депозитите характеристика, че температурата на резервоар горе система критична температура кондензация резервоар.
Наситен система кондензат образува ако по време на образуването на отлагания са източниците на висококипящи въглеводороди от фазата на газ (масло ръб или близо до петролни полета, лежащи).
Таблица 2. качествените характеристики кондензати
притискане системи резервоара дори при високо съдържание на С5 + въглеводороди височина на резервоара газове под налягане е винаги под образуването на оросяване.
Трябва да се отбележи, че характерна особеност на кондензата газ е да се намали концентрацията на етан и пропан с пропан да бутан, докато в бутан, споменатият редовността отсъства.
депозити газ кондензат, тази стойност е 2 - 6. Съотношението на метан в размер на C1 / C2 + тежки въглеводороди в газ-кондензат депозити е около 10, докато в газове, разтворен в маслото до 13.
- ниско съдържание на сяра и maloaromatizirovannye;