Водород в стомана, ефект на водород върху стоманени свойства
Неговата разтворимост в стомана и ефекта на водород върху стоманените свойства. Н2 разтваря в стомана и железни сплави в атомната (йонен) състояние. Атомите (йони) на водород поради малкия си размер разпределени в междините между железните атоми, създавайки интерстициални разтвори.
Разтворимостта на водород в желязото може да бъде описан от уравнения:
Следователно, разтворимостта е пропорционална на квадратния корен на налягането от него. Този модел е създаден сиверт и след това потвърдена експериментално М. М. Karnauhovym и A. Н. Morozovym, VI Yavoyskim и други изследователи. Беше установено обаче, че разтворимостта на водород в стоманата зависи от температурата и варира периодично с алотропна трансформация (промяна стойност / KH).
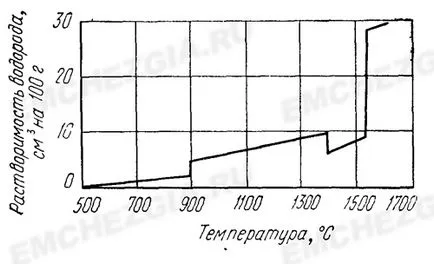
Резултатите от изследванията, представени под формата на isobars на фиг. 1 показват. че с повишаване на температурата на разтворимостта на водород в стомана обикновено се увеличава. В превръщане на а-у-желязото в желязо, както и разтворимостта на точка на топене от водородни увеличава рязко. В прехода от модификация на желязото в бета модификацията е малко понижена.
Други елементи влияят върху разтворимостта на водород в стомана. Този ефект се характеризира с параметрите на взаимодействие.
Следователно, кислород, силиций и въглерод намали разтворимостта на Н2 в течното желязо, което е особено силни кислородни актове в тази посока. Титан, напротив, увеличава разтворимостта на водород в стомана. Ефект на други елементи (Ni, Al, Cr, и т.н.). Незначително.
От особено значение е драматично намаляване на разтворимостта на Н2 в стоманата по време на втвърдяване и по-нататъшно понижаване на температурата. Фиг. 1 показва, че при 1600 ° С и рН 2 = 10.223 кН / т2 (760 mm Hg. V.), разтворимостта на водород в течна желязо е около 28 cm 3 на 100 г, и твърдият желязото при стайна температура, е практически нула , Следователно, по време на Н2 кристализация до голяма степен протича в матерната луга, което причинява силна си зонален сегрегация в слитъка, и след втвърдяване напълно от разтвор в метала.
отделянето на водород се среща в металната решетка и дефектен празно пространство. Тук H2 атома комбинират, за да образуват молекули, и преминава в газообразно състояние.
Ако празният обем е достатъчно голям, както е случаят в метала на отливката, Н2 налягане в тях голям и влиянието на водород върху стоманените свойства не са значително. Ако празният обем е малък (например валцувани и подправени метал) водород преминава само микропори и дефектни решетъчни места, където има високо налягане (до 1 кН / m 2 или 100 кгс / mm 2), увреждащ свойствата на стоманата.