Периодичен закон в модерната форма
Сподели с приятели:
Периодичен закон в модерната форма. Периодичната система. физически
смисъла на периодичния закон. Структура на периодичната система. Промяна на свойствата на атома
химични елементи основната група. Плановете на химичен елемент.
Периодичен закон в съвременната формулировка:
Свойствата на прости вещества, както и формата и свойствата на съединенията от елементи, намерени в периодичната таблица в зависимост от заряда на ядрото (= атомния номер)
Периодичната система:
Периодичната таблица: тя е графично представяне на периодичния закон.
Физическият смисъл на периодичния закон:
Периодичният промяната на свойствата на химични елементи и техните съединения в увеличаване на заряд на ядрото на атома се дължи на факта, че периодично повтаряща се структура на външен електронен слой атоми елементи.
Структура на периодичната система на химичните елементи:
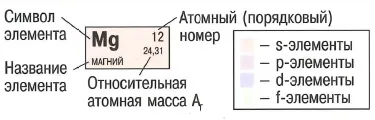
- Всеки химичен елемент е представен от символ и заема клетка, която показва някои от неговите свойства.
- Атомна номер: броя на протоните = електрони
- Относително атомно тегло: тегловно съотношение е 1/12 атом с въглеродния атом на атомна маса. Заоблени стойност, равна на общия брой на протоните и неутроните.
- Период: хоризонтална елементи серия подредени във възходящ ред на техния атомен заряд ядро. Атомите на елементи от същия период имат същия брой заети електронен слой.
- Кратък период (първо, второ, трето) се състои от един хоризонтален ред
- Големи периоди (4-7) се състоят от две хоризонтални редове
- период номер: показва броя на заетите нива електронна енергия в атомите на елементи, принадлежащи към този период съответства на броя на последния електронен ниво, където има най-малко един електрон
- В началото на всеки период съвпада с началото на нов електронен слой пълнеж.
- Всеки период започва елемент чиито атоми образуват вещество метал, но краен елемент, който атоми образуват инертен (= благороден) газ
- Група: Тази вертикална колона от елементи, чиито атоми имат същия брой на валентните електрони. Всяка група се състои от основна (А) и страничен (B) подгрупи.
- Подгрупи оформени елементи с подобни свойства.
- номер група показва броя на валентните електрони в атомите на елементи, принадлежащи към групата. Номерът на група за елементите на 2-ри и 3-ти периоди показва броя на електроните в последния електронен ниво.
- Начало подгрупа съдържа елементи на малки и големи периоди от време. Инцидентно подгрупа съдържа елементи само големи периоди.