Основните параметри на държавата - studopediya
Физичните величини, характеризиращи състоянието на системата на АП се нарича параметрите AP. Основните параметри са температура, налягане, и специфичен обем. Те включват също така вътрешната енергия, ентропия, енталпия, и др.
Термодинамичните параметри, които не зависят от размера и теглото на системата, наречена параметрите на интензивност. Това налягане, температура и специфичен обем моларен и специфичен вътрешната енергия на мол, и моларното специфичен енталпия и специфичен ентропията мол и сътр.
Термодинамичните параметри пропорционални на количеството на материала или тегло на системата, наречени обширни. Те включват маса, обем, вътрешна енергия, ентропия, енталпия и др.
Тяло, представляващо термодинамична система може да бъде в една от три състояния: течност, твърди или газообразни. При различни условия и състоянието на един и същ орган може да бъде различна. Въпреки това, при същите обстоятелства на тялото винаги ще бъде в същото състояние. Например, при атмосферно налягане и температура от 500 ° С водата ще бъде само под формата на пара, но не течна или твърда. За определяне на физическите условия, при които се считат за тялото и недвусмислено определяне на неговото състояние се прилага характеристики статус - Статус параметри.
Обем - геометричните размери на тялото. защото газ има тенденция да заема целия обем, предоставена от него, обемът на газа е геометричните размери на съда, в който е поставен. Международната система единици обем се измерва в m 3 производни единици са литра, с 1000 л = 1 м 3.
Специфичното количество на веществото, - обем заета от единица маса на дадено вещество. специфичен обем V се свързва с маса m вещество и съотношение неговия обем V:
Ако изрично V в m 3 и m в кг, че V се изразява в m 3 / кг.
Реципрочната стойност на специфичния обем, наречен плътност (с). Физическият смисъл на плътност - това е теглото на един кубичен метър газ.
Единицата за плътност е SI кг / м 3 в системата CGS - г / см 3.
Плътността и специфичният обем в зависимост от температурата и налягането, което е от термично състояние на материала.
Количеството вещество - е физическото количество определя от редица структурни елементи. Единицата за количество вещество в Международната система единици е мол.
Mol - количество вещество, съдържащ същия брой структурни елементи (атоми, молекули, йони, електрони, и т.н.) като атомите, съдържащи се в 0,012 кг въглерод-12 изотоп.
Моларен (мол) обем - обем заета от 1 мол на газ. Тази стойност се определя като отношението на обема на веществото за неговото количество.
където Vm -molyarny обем, V - обем, п - количество на веществото.
Моларен обем изразена в m 3 / мол.
Моларен маса е масата на вещество на 1 мол вещество. Тя е свързана с масата на веществото и съотношението количество:
където m - моларното тегло, изразено в кг / мол.
Налягане - физическа величина е числено равно на нормалната сила компонент по отношение на площта, върху която действа сила.
защото за газ, състоящ се от голям брой хаотично движещи се молекули е невъзможно да се определи нормалната компонента, които често се използват по-прости налягане дефиниция: налягане - сила, с която молекулите се удрят в стената на съда, в който е приложен газ.
Единицата за налягане в системата SI е Паскал (Ра), - налягането, причинено от сила на 1 N, равномерно разпределени по повърхността на 1 m 2 (1 Pa = 1 N / т2). В други системи за измерване на налягане се измерва също в мм живачен стълб mmAq, барове, атмосфери х кг / см2 и т.н.
налягане преобразуване таблица е даден в допълнение 1.
Разграничаване атмосферно (барометричното) RATM налягане. абсолютна Manpower. прецени (манометър) Rizb. подналягане (вакуум) Rvak.
Абсолютното налягане се нарича налягане, измерено от нула (абсолютен вакуум).
Атмосферно (барометричното) нарича налягането, генерирано от атмосферен въздух. Тя се измерва с барометър.
Излишък (манометър) налягане над атмосферното налягане се нарича, т.е. свръхналягане - разликата между абсолютните и атмосферното налягането:
Прекалено налягане, измерено чрез манометър.
Засмукване или вакуумно налягане е разликата между атмосферното налягане и абсолютното налягане на средата, където се измерва налягането.
вакуумно налягане се измерва с уред за измерване на вакуум.
Термодинамичните уравнения винаги е стойността на абсолютното налягане се дължи на факта, че тя е параметър, който характеризира състоянието на системата.
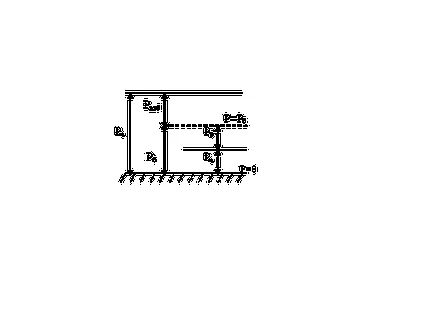
Фигура 1. Видове налягане.
Атмосферно налягане - променлива, така че нормално атмосферно налягане се прилага в областта. P0 = 101325 Ра (760 Torr или 1 атм).
Молекулно - кинетичната теория на газове позволява да се установи връзка между налягането и кинетичната енергия на топлинната движение на молекулите на газа. Според тази теория, която счита се предполага идеална газ че газовите молекули са разпределени равномерно в обема и огромен брой съхранява в хаотичния топлинна движение. Молекули непрекъснато въздействат на един от друг и по стените на съда, при което затвореното газ. В резултат на сблъсъци на молекулите на налягането на стена е създаден нормално да стенни повърхности и равномерно във всички посоки.
Абсолютно налягане газ се определя от формулата:
,
където п - брой молекули на единица обем;
m - маса в хомогенна молекула газ, всички молекули на същите се приема;
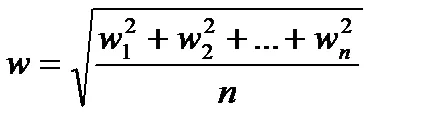
Стойност определя средната кинетичната енергия на постъпателно движение на една молекула.
Температура - нагрява мярка тяло. Температура определя посоката на пренос на топлина. Ако две тела А и В имат съответната температура Т1 и Т2 и Т1> T2. топлината се пренася от спонтанно на тялото и тялото Б. тяло температурата намалява и температура В - увеличаване.
Ако се съди с еднакви или различни температури на две тела А и В, не е необходимо да ги приведат в термичен контакт един с друг. Тя може да се използва за тази трета последователно тяло C забит в контакт с органите на А и В. Тя се нарича тяло От thermoscope.
За количествено определяне на телесната температура се използва скалата на температура. Калибриране на всяко правило thermoscope превръща в термометър. т.е. устройство за измерване на температурата.
Един цифров отчитане на температурата, произведен от скалата на температура. В момента се използват различни мащаби: Келвин, Целзий, Фаренхайт, Reaumur, Ранкин.
Решението на Международния комитет за мерки и теглилки прие две скали: термодинамична температурна скала, която прие основен, практичен и международен мащаб (ИПТИ-68), подбрани така, че температурата, измерена на тази скала е бил близо до термодинамична (използва по Целзий).
Най-гъвкавият е абсолютната температура мащаб термодинамични - Келвин скалата.
Температурата на двете скали може да се изразява в градуси Келвин и градуса по Целзий. Съотношението между тези температури следното:
По отношение на молекулна - кинетичната теория на температурата е мярка за интензивността на топлинна движение на молекули. Неговата числова стойност е свързана със средната кинетична енергия на молекулите на дадено вещество. За идеален газ, тази функционална връзка се определя от уравнението:
,
където к - Болцман константа (k≈1.3806 · 10 -23 J / K).
температура Т, което е определено, се нарича абсолютна. Следователно, в това термодинамиката на температурата като средно статистическа стойност, която характеризира система, състояща се от голям брой молекули в хаотичен (топлинна) движение. Следователно, за да единични молекули на концепцията на температурата не е приемливо. От последния експресия показва, че стойността Т = 0 съответства w = 0; в абсолютна нула температура на топлинна движение на молекули отсъства. Това ограничава температура се нарича минималната абсолютна нула и е изходна точка за референтната температура. Разбираемо е, че може да има T <0, т.е. абсолютная температура всегда положительна.
Съотношението между различните мащаби са дадени в Приложение 2
Абсолютната налягане и абсолютната температура са взаимосвързани
където к - Болцман константа равна на 1,3806 х 10 -23 J / K
п - молекулярна концентрация (брой молекули на единица обем).
Това уравнение се нарича основно уравнение на кинетичната теория на газовете.