Определяне на заряд на пептид молекула
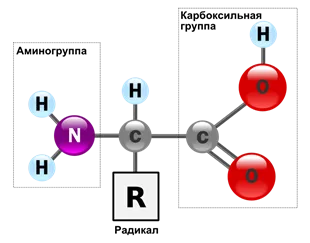
Пептиди - органични съединения от аминокиселини. свързани с пептидни връзки.
Аминокиселините в по-голямата си част, такива молекули са:

Връзката на пептид се образува както следва:
R (радикал) може да бъде различен. Радикалите протеиногенни аминокиселини, които трябва да се научат, са представени в таблицата по-долу:

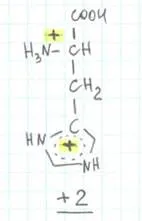
Нека разгледаме няколко възможни варианти на киселинността на средата:

2. По-малко кисела среда близо до неутрално, да предположим, рН от около 5 (т.е. количеството на Н + се намалява). Протоните са вече не е достатъчно за карбоксилна група (първото нещо, на протона е винаги тя губи), но другите две разпоредби все още са протонирани.

3. неутрална среда и специален случай - изоелектричната точка (това съответства на хистидин при рН 7.6). Изоелектричната точка на аминокиселини заряд е нула. Протоните са само в амино група.
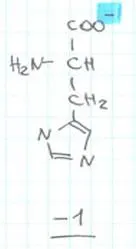
Съответно, за да се определи заряд на пептида е необходимо да се определи заряд на аминокиселината влизат в състава си, в зависимост от киселинността на средата.
Какво зареждане ще има пептид, състоящ се от 3 хистидинови молекули в много кисела среда? За да направите това, нека да преброим колко позиции потенциално биха могли да бъдат протонирани (прикачите протон).
1. Две от 3-амино групите и две от три-карбоксилни групи са включени в образуването на пептидната връзка - не може да бъде протониран.
2. наличност остане една амино група, (N-края на пептида) и една карбоксилна група (С-края). Също така, 3 имидазол остатък.
N-терминалната амино група ще ни даде малко плюс три имидазол остатък три повече знака плюс, и карбоксил - нула.
Общо. зареждане на пептида His-His-му в кисела среда е много 4+
И това, което ще отговаря на пептида Gly-Gly в киселата среда? Повторете процедурата.
1. Две от 3-амино групите и две от три-карбоксилни групи са включени в образуването на пептидната връзка - не може да бъде протониран.
2. наличност остане една амино група, (N-края на пептида) и една карбоксилна група (С-края). Глицин радикал - Н. протониран не може.
N-терминалната амино група ще ни даде малко плюс три радикал ни три нули и карбокси друг нула.
Общо. зареждане на пептида Gly-Gly-Gly в кисела среда е равна 1+.
По този начин (на разглеждането избиратели) и пептид такса решен.