молекули стереоизомер с два или повече центъра на хиралност, енантиомери и диастереомери
Диастереомерите наречени стереоизомери, не са свързани един с друг, като предмет, и е в противоречие с това флип, т. Е. не са енантиомери.
Най-важните групи са диастереомери # 963; -diastereomers и я-диастереомери.
# 963; -diastereomers. Много биологично важни вещества, съдържащи в молекулата повече от един център на хиралност. Това увеличава броя на конфигурационни изомери, които се определят като 2 п. където п - брой на хирални центрове. Например, когато има два асиметрични атома на съединението могат да съществуват като стереоизомери четири (2 2 = 4), представляващи двете двойки от енантиомери.
2-амино-3-хидроксибутанова киселина има два хирални центъра (атома С-2 и С-3) и следователно трябва да съществуват като четири конфигурационни изомери, един от които е естествена аминокиселина.
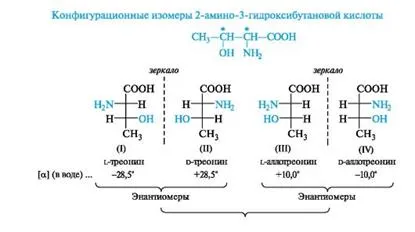
Структурите (I) и (II), съответната L- и D-треонин, и (III) и (IV), съответната L- и D-алотреонин (от гръцката alios -. Други) се отнасят един към друг, като предмет и несъвместими с него огледален образ т. е. те представляват една двойка енантиомери. Когато се сравняват структурите (I) и (III), (I) и (IV), (II) и (III), (II) и (IV) се вижда, че в тези двойки съединения имат една конфигурация асиметричен център е същото, и друга - обратното. Такива двойки стереоизомери са диастереомери. Подобни изомери се наричат # 963; -diastereomers като заместители в тях са свързани с центъра на хиралност # 963; -връзките.
Аминокиселините и хидроксикиселини с два центъра на хиралност, посочени като D- или L-конфигурация серия асиметричен въглероден атом с най-малък номер.
Диастереомерите, за разлика от енантиомери, различни физични и химични свойства. Например L-треонин, част от протеина, и L-алотреонин имат различни стойности на специфичното въртене (както е показано по-горе).
Meso съединение. Понякога в молекулата, съдържа две асиметрични центрове и повече, но молекулата като цяло остава балансиран. Примери за такива съединения могат да служат като един от стереоизомерите на винена (2,3-дихидроксибутандионова киселина).
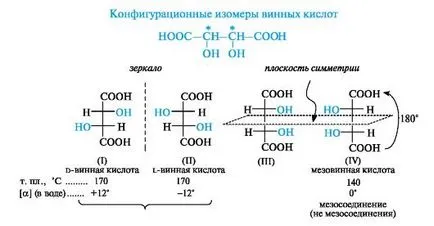
Теоретично, тази киселина, в която има два хирални центъра, може да съществува като стереоизомери на четири (I) - (IV).
Структурите (I) и (II) съответстват енантиомери D- и L-серия (класификация извършва на "отгоре" хирален център). Тя може да изглежда, че структурите (III) и (IV) и отговарят на двойка енантиомери. В действителност, тази формула същото съединение - mezovinnoy оптически неактивна киселина. Идентичността на формули (III) и (IV) може лесно да се провери, чрез завъртане на формула (IV) от 180 °, без да го извеждане на самолета. Въпреки двата центъра на хиралност, молекула mezovinnoy киселина като цяло е ахирална тъй като има равнина на симетрия, простираща се през центъра на С-2-С-3. По отношение на D- и L-винени киселини mezovinnaya киселина е диастереомер.
По този начин, има три (вместо четири) стереоизомер винена киселини, с изключение на рацемичната форма.
Рацемичната смес (рацемична смес) - смес от равни части от две вещества enantiomerov- проявяващи оптична активност. Един от тях - дясновъртящи, т.е. въртене на плоскостта на поляризация на светлината, която преминава през тях, от дясната страна; друга - лявовъртящи, се различава само по посоката на въртене. В резултат на двете реакции се анулират взаимно взаимно и рацемичната смес не показва оптична активност. Името идва от рацемичен винена киселина е смес от равни количества от D- (дясновъртящ) и L- (лявовъртящ) винена киселини.
пи-диастереомери. Те включват конфигурационни изомери, съдържащи π-връзка. Този тип изомерия се характеризира по-специално с алкени. Спрямо равнината π-свързване на две еднакви заместители на въглеродните атоми може да бъде разположен на същите (цис) или различни (транс) страна. В тази връзка са стереоизомери, известни като цис и транс изомери, както е показано в примера от цис- и транс-бутени (вж. 3.2.2). π-диастереомери са прости ненаситена дикарбоксилна киселина - малеинова и фумарова.
Малеинова киселина е термодинамично по-малко стабилна цис-изомер в сравнение с транс-изомер - фумарова киселина. Под влиянието на определени вещества или ултравиолетови лъчи между двете киселини се установява равновесие; чрез нагряване (
150 ° С) се измества към по-стабилно транс-изомер.