Кой е изобретил на батерията - когато е измислил
Строго погледнато, общо име "батерията" не е съвсем вярна. Тя комбинира няколко вида източници на енергия за автономно устройство захранване. Това може да бъде единичен електрохимична клетка, батерията или свързване на няколко такива елементи на батерията, за да се увеличи освобождаване на напрежението. Именно тази връзка и е довел до запознати името на нашето ухо.
Батерии и електрохимични клетки и батерии са химически източник на електрически ток. Първият подобен източник е изобретен като толкова често се случва в областта на науката случайно италиански лекар и физиолог Луиджи Галвани в края на ХVIII век.
Въпреки, че електроенергията е феномен, познат на човечеството от древни времена, много векове, тези наблюдения нямат никакво практическо приложение. Само през 1600 г., на английски физик Уилям Гилбърт публикува трактат "За магнита, магнитни органи и големия Земята магнит", където бяха обобщени известен в данните път на електричеството и магнетизма, а през 1650 г. Ото фон Gerike създаден електростатичен машина е сярна балон се монтира върху металната пръчка. Един век по-късно, холандецът Питер ван Мьосхенбрук първи път успя да спаси с "Лейден буркана" на първия кондензатор малко количество електричество. Въпреки това, той е бил твърде малък, за сериозни експерименти. Проучвания "естествени" учени електроенергия ангажирани като Бенджамин Франклин, Джордж Ричман, Джон Uolsh. Това беше последното дело на скатове интересуват Галвани.
Истинската цел на добре известния експеримент на Галвани, революция в физиология и завинаги в Почетната науката, сега никой няма да си спомня. Галвани дисекция на жаба и да го сложи на масата, където имаше електростатичен машина. помощникът му случайно докосна върха на скалпел за отваряне на бедрената нерв на жаба и мъртъв мускул внезапно намалява. Друг помощник каза, че това се случва само, когато автомобилът се извлича искра.
Вдъхновен от откриването на Галвани започна да изследва методично наблюдаваното явление е способността на един мъртъв наркотици демонстрира жизненоважен свиването под влиянието на електроенергия. След като прекара цяла серия от експерименти, Галвани е особено интересен резултат използват медни куки и сребро плоча. Ако куката държеше на крака, да докосвате табела, крак, докосва плочата, веднага намаля и стана. След като губи контакт с плочата, мускулите на краката веднага спокойна, тя падна на запис, е намалял и възкръсна.

Луиджи Галвани. Списание илюстрация. Франция. 1880
Така че след серия от експерименти, старание и нов източник на електроенергия е била отворена. Самият Галвани, обаче, не мисля за това, което той е открил причината за контактни явления различни метали. Според него, източник на ток е много мускул, който се вълнува от действието на мозъка, което предават нервите. Откриване Галвани предизвика сензация и доведе до много експерименти в различните клонове на науката. Сред последователите на италианския физиолог доказа своя сънародник физик Алесандро Волта.
През 1800 г., Volta не само с оглед на точното обяснение на явлението отворен Галвани, но също така за цел устройство, което се превърна в първия в света изкуствен химичен източник на електрически ток, прародител на всички съвременни батерии. Той се състои от два електрода на анода съдържащ окислител и катод, съдържащ редуктор в контакт с електролита (солев разтвор, киселини или основи). Потенциалната разлика, че се наблюдава между електродите в този случай съответства на свободната енергия на редокси реакция (електролиза), в която са намалени катиони електролитни (положително заредени йони) и аниони (отрицателно заредени йони) се окисляват на съответните електроди. Реакцията може да започне само когато електродите са свързани към външна верига (Волта присъедини им обикновен тел), на която свободни електрони се движат от катода към анода, като по този начин създаване на разряден ток. Въпреки че съвременните батерии имат малко общо с В напрежение на устройството, принципа на действие остава непроменена: двата електрода, потопени в разтвор на електролита и свързани към външна верига.
Volta на изобретението е дал значителен тласък на изследванията, свързани с електричеството. През същата година, учени и Уилям Nikolson Entoni Karlayl разлага чрез електролиза на водата на водород и кислород, малко по-късно Hemfri Деви същия начин отвори калиев метал.
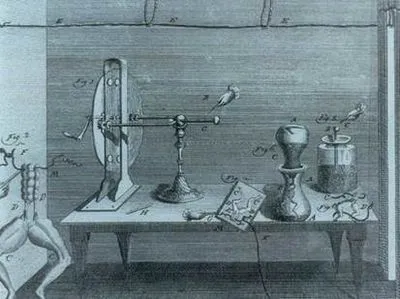
Галвани експерименти с една жаба. гравиране 1793
Но преди всичко галванични клетки със сигурност е най-важният източник на електрически ток. От средата на XIX век. когато първите електродомакински уреди, започнали масово производство на химически батерии.
Всички тези елементи могат да бъдат разделени на два основни вида: първични, в който химична реакция е необратим и вторична, че могат да се презареждат.
Какво сме свикнали да наричаме батерията е основното химическо захранване източници, с други думи, без възможност за зареждане елемент. Първите батериите, работещи в масово производство, е изобретението през 1865 г. от французин Georges Leklanshe цинк-манганови батерии с физиологичен разтвор и след това с суспендира електролит. До началото на 1940, тя е почти единственият вид, използван в електрохимични клетки, което се дължи на ниската цена на широко разпространеното досега. Тези батерии се наричат сухи или въглерод-цинкови елементи.

Гигантски електрическа батерия, конструирана от Уилям Wollaston за експерименти X. Дейви.
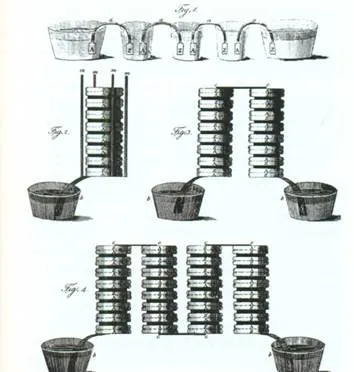
Схема на изкуствен химичен ток източник А. Волта.
През 1803 Василий Петров създадена най-мощната в света галванична батерия, използвайки 4200 метални кръгове. Той бе в състояние да разработи напрежение 2500 V, както и за откриване на такъв важен феномен като електрически дъга, която по-късно започва да се използва в електрожен, както и за електрически предпазители експлозиви.
Но истински технологичен пробив е появата на алкални батерии. Въпреки че химичният състав не са особено различен от Leklanshe елементи и тяхното номинално напрежение се сравнява със сух клетка се увеличава леко, поради основна промяна в алкални дизайн може да служи четири до пет пъти по-сух, обаче, при определени условия.
Най-важната задача в развитието на батериите е да се повиши капацитета на клетките, като същевременно намали неговия размер и тегло. За да направите това, в постоянно търсене на нови химични системи. Най-високотехнологичните първична елементи днес са литий. Техният капацитет е два пъти повече от капацитета на сухи клетки и значително по-дълъг експлоатационен живот. Освен това, ако алкални батерии са сухи и постепенно, зауствани, литий холдинг напрежение по време на практически цялата си живот, и едва след това бързо го изгуби. Но дори и най-добрият батерията не може да се сравни по ефективност с акумулаторна батерия, принципа на действие се основава на обратима химична реакция.
За възможността за такова устройство започнах да мисля в XIX век. През 1859 г. французинът Gaston Plante изобретил оловно-киселинен акумулатор. Електрическият ток в него се появява в резултат от реакциите на олово и оловен диоксид в среда на сярна киселина. По време на генерирането на ток изтощен акумулатор консумира сярна киселина за образуване на оловен сулфат и вода. За зареждане на необходимо ток, получен от друг източник, да премине през веригата в обратна посока, водата, която ще се използва за образуване на сярна киселина за освобождаване на олово и оловни диоксид.
Въпреки, че на принципа на действие на такава батерия е описан за дълго време, неговото масово производство започва едва през ХХ век. като за презареждане устройство изисква високо напрежение, както и спазването на редица други условия. С развитието на електрическите оловно-кисели батерии са се превърнали в неизменна и все още се използва днес в автомобили, тролейбуси, трамваи и други средства за електрически транспорт, както и за аварийно захранване.
Много малки домакински електроуреди и работим за един "за многократна употреба батерии" акумулаторни батерии, които имат същата форма като невъзстановими клетката. развитие на електрониката, зависи от развитието в тази област.

Батерията J. Leklanshe.

Суха батерия.
Първи да заменят галванични клетки са никел-кадмиеви и никел-метал-хидридни батерии. Техният основен недостатък е "ефект на паметта" Спадът в качеството, по време на зареждане се извършва, когато батерията не е напълно разредена. Освен това, те постепенно губят заряд дори и при липса на натоварване. Тези проблеми до голяма степен са решени в развитието на литиево-йонни и литиево-полимерни батерии, които сега са широко използвани в мобилни устройства. Техният капацитет е много по-висока, те Lossless зарежда по всяко време и да запази доброто заплащане в очакване.


Modern устройство за зареждане на акумулаторни АА клетки.