Инхибиторите - химическа енциклопедия
Инхибитори (от латински mhibeo - спират, ограничават), на островите, което пречи химикал. р-ТА. Инхибиране характеристика katalitich верига и р-ции, притежавани до възникнат с активни сайтове или активни частици. Инхибиторният ефект се дължи на факта, че AI блокове активните центрове на катализатора или реагират с активните частици да образуват ниска активност радикал не е в състояние да продължи верига. IA се прилага в концентрация, по-ниска от концентрацията в реакция-ин (10 - -10 2-5 мол%). Кинетика на р-ции, включващи I. коренно различна за каталитични и верижни р-ции. В katalitich. р-ТА на броя на активните центрове е фиксиран и И. блокира част от тях не се консумира по време на процеса. Следователно, когато се прилага скорост р-ТА IM е намалена, и тогава процесът е дълъг. време с постоянна скорост. В някои случаи този процент може да се увеличи бавно поради разходите за I. НАСЛЕДСТВО Инцидентно р-ТА. активни частици верига р-ционни непрекъснато генерирани, в резултат на разходите на I. и постепенно самостоятелно ускорение на р-ТА (в случай на права верига р-ТА обикновено възстановява първоначалната скорост).
реакции Инхибиране верига. Продължителност т спирачен ефект наречен GI. Индукционен период; брой вериги е. еднозначна молекула се разпада I. последователно се присъедини към прекратяване на р-ТА се нарича. стехиометрично. коефициенти. инхибиране. Когато първоначалната концентрация I. [и] 0 и VI скорост на верига индукция започване период е: т = F [и] 0 / VI. Напр. хинон инхибира полимеризацията на винилови мономери, подадена следа. р-ТА:
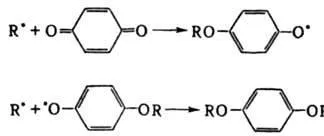
В този случай, F = 2 и т = 2 [и] 0 / VI. В определени системи, регенерация се среща в ции верига терминатор р-VI, при което една молекула IV и в резултат на това радикал многократно участва в счупване на р-ции. Напр. въвеждането на медни йони в окислен изопропилов алкохол верига са отрязани в резултат на трасето на потока. променлив р-ции:
В такива системи, периодите на индукционни наблюдавани и в излишък от 2 [и] 0 / VI. За всеки р-ТА съществува специфика. Определете I. р-ТА на водород с хлор и инхибират NCl3 O2. реактивни хлорни атоми; полимеризация на винилов мономер -hinony, нитро, I2. стабилни радикали (diphenylpicrylhydrazyl, нитроксилни радикали) алкил поглъщане macroradicals; ORG Порт окисление. (Въглеводородни гума и полиолефини) феноли, ароматни. амини, аминофеноли, взаимодействие с пероксидни радикали RO2; олефини, крекинг на въглеводороди и азотни окиси, които реагират с алкилови радикали. За да гасят горене орг комп. употреба халовъглероди CF3 Br, CF2 ClBr, С2 F4 Br2. Тяхната инхибиторен ефект се дължи на факта, че разклоняване агент по време на горене са Н атоми, с К-rymi I. влезе в р-ТА: RBr + НВг Получените причини допълват. прекъсване на веригата на р-tsiyam:
(М - всеки трети частиците). За да гасят горивни пожарогасителни прахове се използват също (напр. На NaHCO 3. Phospho-амониеви соли), притежавани до са комбинирани с. действие: намаляване на концентрацията на радикали поради прекратяване на тежката верига на превръзка-STI и причиняват повишена. радиатор (вж. горенето). Разграничаване слаб и силен I. Това р-ТА. Се счита за силна VI до позиция, ако се въведе във висока концентрация е достатъчна, за да намали единица дължина на веригата или намалява скоростта на р-му в V0 / VI пъти, където v0 - референтната скорост R-нето. I. Light въведена дори в относително високи концентрации намалява скоростта на р-ТА на VI-бодното до определена стойност V> VI. Това се дължи на факта, че молекулите на слаб I. образуват радикали имат възможност да продължат верига, при което съотношението на v0 / обем намалява с увеличаване [И] 0. достигайки стойности на v0 / VI. AI има силен инхибиторен ефект в ниска концентрация, наречен. ефективна. I. ефективността характеризират производно стойност -dv / г [И]. Напр. окисление на въглеводороди в присъствие на RH. инициатор генериране скорост започване VI, се определя от скоростта на разпространение верига с пероксидни радикали:
така че първоначалната скорост на окисление верига V = KP. [RH] []. Предварително зададените. I. напр. фенол верига са отрязани от продукти р-ционни тип. квази-стационарна условия за започване и прекратяване процент равен на: VI = FKT [И] [RO2], следователно [] = VI / FKT [И] и V = KP [RH] VI / FKT [И]. Ефективността на инхибиране се характеризира с FKT / KP връзка. За инхибиране разклонена верига, р-ции се характеризират с критично. явления към ryh същност се състои в рязкото намаляване на скоростта р-нето на много незначително. увеличаване на концентрацията на I. Един пример се инхибира. автоокисляване на въглеводороди RH, в ром DOS. източник на радикали е ROOH на окисление продукт. Когато достатъчно висока T-D или в присъствието. катализатор интензивно превръщане ROOH в радикалите RH окисляване може да се осъществи в режим на квази-неподвижен, когато скоростта на образуване на ROOH практически равна на неговата скорост на потребление. защото Скорост на образуване на ROOH зависи от концентрацията и концентрацията на IA ROOH, има врата-рай от решаващо значение. концентрация IM в рояк от нестабилна система се движи към квазистационарното режим с много ниско (на 0,1-1%) концентрация се променя I. Това води до резки промени в скоростта или р-ТА индукционен период И. И. Две наложени реакция система може взаимно засилване на инхибиращия ефект на всеки друг (т.нар синергизъм VI ..) или (антагонизъм VI) отслабва; често се наблюдава адитивен ефект на две Н. Ако т 1 и т 2 - продължителност на инхибиращия ефект на първата и втората УИ въвежда отделно, и 12 т - продължителност на съвместното им действие, в случай на синергизъм 12 тон> (т 1 + Т2), в случай на антагонизъм т 12 <( t 1+ t 2 ). На диаграмме t - концентрация И. в случае синергизма наблюдается максимум. Синергизм И. может быть обусловлен либо разл. механизмами тормозящего действия И. (напр. при ингибир. окислении RH один И. обрывает цепи, а другой разрушает ROOH), либо хим. взаимодействием между двумя И. или продуктами их превращения.
Инхибиране на хетерогенни каталитични реакции извършва в-ви притежавани до т.нар. каталитични отрови. Инхибиране на р-ТА, причинени от намаляване катализатор активност поради адсорбция върху AI превързочни-STI.
Инхибирането на ензимната т. Б. обратими и необратими. И в двата случая, I., способен да образува комплекс с ензима, но не и т. Б. katalitich подложени. завъртане и предотвратява образуването на ензима - субстрат. Напр. бутанол инхибира хидролиза на естери, катализирана от карбоксипептидаза. Разграничаване следното. случаи на обратимо инхибиране. Директно конкурентно инхибиране на ром молекула I. I S и субстрат се конкурират за свързване към активния център на ензима Е. метода, описан от (Р - реакционен продукт):
С такъв механизъм на инхибиране, когато [Е] <<[S]0 и Е <<[I]0. начальная скорость превращ. субстрата S равна:
Неконкурентно инхибиране на ром I. присъединява към активния ензим или ензимен комплекс със субстрат за да се образува каталитично неактивна форма на:
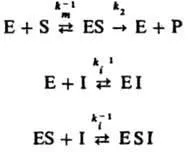
В този случай, началната скорост на р-ТА е:
Не-конкурентно инхибиране с ром I. форми каталитично неактивен комплекс с субстрат:
Началната скорост р-ТА е:
Трябва да се отбележи инхибиране на ензим, субстрат, когато неактивен ензим образува комплекс с втора молекула на субстрат (субстрат инхибиране). Необратимо взаимодействие IV реагира с ензима, тя дезактивиране; За разлика от обратимо инхибиране на ензимната активност намалява с времето.
Заявление. Инхибирането е широко използван за контролиране на скоростта на радикалова полимеризация, по-специално при получаването на голям обем продукти. I. окисление се използва за стабилизиране на полиолефини и каучуци в тяхната обработка и условия на използване (вж. Разграждане на полимери), за стабилизиране на смазочни материали и въглеводородни горива pishch съхранение. мазнини и лек. лекарства; в технологията на мономери се използват за предотвратяване окисляват. полимеризация. В изследвания работи I. използват за изучаване на механизма на веригата р-ции, по-специално определянето на скоростта на откриване на процедурата.
===
App. Литература за "инхибитор" на статията: P. Ashmore катализа и инхибиране на химични реакции, на. от английски език. М. 1966; L. Webb инхибитори на ензими и метаболизъм, транс. от английски език. М. 1966; Kuliev A. М. химия и добавка технология за масла и горива, М. 1972 Денисов ЕТ Ковальов GI окисляване и стабилизиране на реактивни горива, М. 1983 ЕТ Denisov.
Page "инхибитор", изготвен на базата на химически енциклопедия.