И нейното измерване на температурата
При термично равновесие 2-тяло:
- не съществува топлообмен и фазови преходи
- Y 2 органи същата температура и кинетичната енергия на молекулите
- Това не променя налягането и обема.
Температура - физическа величина описва състоянието на термодинамично равновесие, което е характерно за интензитета на случаен движение на молекули.
измерване на температурата се осъществява чрез термометри.
Термометър - устройство, където обем на газ или течност, зависи от температурата.
Термометри са газ и течност (живак и алкохол).
Термометри винаги се довеждат в контакт с измерване на тялото преди термично равновесие.
Температура - описание на цялото тяло, а не една единствена молекула.

Билет №8. Уравнение Менделеев-Клапейрон. Клапейрон. Izoprotsessy в газове.
Това уравнение описва състоянието на термодинамична система.
Уравнението се отнася macroparameters на даден газ (налягане. Обем и температура), за да му маса.
P - налягане (Ра) V - обем () T - абсолютна температура (K) m - тегло (кг) # 120641; - моларна маса (кг / мол)
# 120642; - количество вещество (мол) R - е универсален газ постоянна R = 8,31 J / Molkov
Това уравнение описва състоянието на термодинамична система с постоянна маса на газ.
Уравнението се отнася macroparameters на даден газ (налягане. Обем и температура) постоянно тегло.
- налягане (Ра) - Volume () - абсолютна температура (К) - nachalnomsostoyanii Газовият
- налягане (Ра) - Volume () - абсолютна температура (К) - в крайното състояние на газ
=
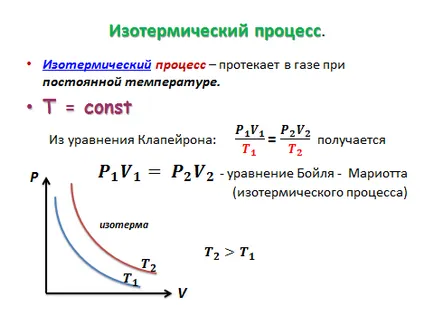
Izoprotsessy в газове.
Izoprotsess - процес, при който един от макроскопски параметри на състоянието на дадена маса на газа остава постоянна.


Билет № 9. изпаряване и кондензация. Наситени и ненаситени двойка. Относителната влажност на въздуха и измерването му.
За разлика от идеален газ, действителната газ не е напълно подчинява закона на Бойл: първото смачкване увеличава натиска си, а след това се втечнява при постоянно налягане, а след това силата на звука не се намалява.
Изпаряването - преминаването на молекулите на течност в газообразно състояние. Той се среща с усвояване на енергия.
Кондензацията - преходната част на молекулите на газа в течен обем. Той се среща с освобождаването на енергия.
Динамично равновесие - състояние, в което броят е равен на броя на молекулите изпарява prokondensirovavshih.
Наситена пара - е в динамично равновесие с течност. наситен Налягането на парите зависи само от температурата. Example- течност в затворен контейнер.
Ненаситените двойки - под налягане под налягането на наситената пара. Пример - течност в отворен съд.
Кипене - изпаряване на течен обем. Кипене започва само когато налягането в балона газ се изравнява с атмосферното.
Точката на кипене зависи от налягането на околната среда. С увеличаване на налягането, точка на кипене се увеличава и обратно.
влажност - абсолютно и относително.
Влажност - броят на водна пара в 1 м 3 на въздух. (Т.е., парциално налягане).
Относителна влажност - съотношението на парциалното налягане на налягането на наситената пара, изразени като процент.
P - парциално налягане (Ра) Ph - наситен налягане на парите (Ра) - Относителна влажност (%)
Частичното налягане - частта налягане на настоящето газ в газовата смес.
Относителна влажност се измерва чрез влагомери и психрометри.
Psychrometer - коса, свързан със стрелка, която се променя дължината му, в зависимост от влажността.
Влагомер - два термометъра, един измерва температурата на сух въздух и овлажнен друг. Чрез разликата на сухо и мокро термометри и psychrometric таблицата определи относителната влажност.