Химичните свойства на алкохоли

Начало | За нас | обратна връзка
алкохоли дисоциация на йони се осъществява в малка степен, така алкохоли дават неутрална реакция - в тяхното присъствие не променя цвета на фенолфталеина или лакмус.
Киселинните свойства на алкохоли са много слаби. Нисши алкохоли реагират бързо с алкоксиди на алкални метали, за да образуват (в този пример - калиев etilalkogolyata):
Алкохоли реагират с заместване водородни халиди:
С киселини (органични или неорганични) алкохоли влизат в реакция на естерификация в присъствието на сярна киселина за образуване на естери:
етилов естер на оцетна киселина
оцетна киселина
При нагряване на алкохола в присъствието на силна киселина се отцепва водни молекули от две алкохолни молекули в резултат на дехидратация и междумолекулно етер произвежда (в този пример - етер):
Диетил етер или сяра - добър разтворител на много органични вещества, се използва за почистване на тъкани и медицински - хирургични операции, както е упойка действие.
Алкохоли реагират елиминиране на вода - елиминиране. или вътрешномолекулен обезводняване. за да се образува ненаситени въглеводороди. Тази реакция става преобладаващ при използване на големи количества киселина:
Алкохоли тъпчат в реакцията на окисление. Окисляване - процес на увеличаване на броя на кислородните атоми в молекулите на органични съединения и да се намали броят на водородните атоми. Първични алкохоли се окисляват до алдехиди, които на свой ред могат да бъдат окислени до карбоксилни киселини:
Вторични алкохоли се окисляват до кетони:
Третични алкохоли са по-устойчиви на окисление. Под действието на силни окислители може да настъпи разделяне на въглеродния скелет на молекулата да образува третичен алкохол на карбоксилни киселини и кетони с по-малък брой въглеродни атоми в молекулата от изходния третичен алкохол. Окислението обикновено се провежда с калиев перманганат или дихромат със сярна киселина.
В реакцията на меден хидроксид (II) с глицерол и други поливалентни алкохоли се разтварят хидроксид и комплексно съединение образува синьо. Тази реакция се използва за откриване на полиоли:

За поливалентни алкохоли, характеризиращи се с образуване на естери. По-специално, се образува реакцията на глицерол с азотна киселина в присъствието на каталитични количества сярна киселина глицерил тринитрат (нитроглицерин)
се използва етиленгликол: Използването на алкохоли:
1) като охладител; 2) за синтез на високомолекулни съединения (например, Dacron).
1) в парфюмерията и в медицината (за производството на мехлеми, които омекотяват кожата); 2) в кожарската промишленост и в текстилната промишленост;
3) за получаване на нитроглицерин.
Органични съединения на молекула, която има карбонилна група> С = О, наречени карбонилни съединения, или оксо. Карбонилни съединения са разделени в две големи групи - алдехиди и кетони.
Алдехиди съдържат в молекулата карбонилна група, свързана с водороден атом, т.е., алдехидна група - .. СН = О. Кетони съдържат карбонилна група, свързана с две въглеводородни радикали, R. Д. кетонна група.
В зависимост от структурата на въглеводородни радикали с алдехиди и кетони са алифатни, алициклични и ароматни.
Изомерия алдехиди, свързани само с радикал структура. Изомерия кетони радикали, свързани към структурата и позицията на карбонилната група във въглеродната верига.
Номенклатура. За алдехиди често използвани тривиални имена, имена на съответните киселини (със същия брой въглеродни атоми), в които се движат в алдехиди чрез окисление. При събирането на имената на алдехида е посочено наименованието на съответния въглеводород, към която се прибавя наставката "Al". например, МЕТАНАЛ Н2 С = О, етанал H3 СС (Н) = О, H3 пропанал SSN2 С (Н) = О.
СН3 -СНО - ацеталдехид - etanalCH3 -СН2 -СНО - пропионалдехид - propanalCH3 -СН2 -СН2 -СНО - бутиралдехид - butanalCH2 = СН-СНО - акролеин (akrilaldegid) - propenalS6 H5 -СНО - бензалдехид
В по-сложни случаи R групи въглеродни вериги са номерирани, започвайки от карбонилния въглерод, след това с помощта на цифров индекс показва позицията на различни функционални групи и заместители.
За разлика от алдехид, кетон група> С = О може да бъде в средата на въглеводородната верига, обаче в прости случаи показват имената на органични групи (тях се споменава във възходящ ред) и думата "кетон": диметил СН3 -СО-СН3. метилетилкетон СН3 СН2 -СО-СН3. В по-сложни случаи, позицията на групата кетон в въглеводородната верига посочи числения индекс чрез прибавяне на суфикса "той". Номериране въглеводородни вериги започват с тази цел, която е най-близо до кето групата.
молекулни кетонни радикали могат да бъдат еднакви или различни. Следователно, кетони, такива като етери, разделени в симетричен и се смесва.
Структура оксо група. Алдехиди се характеризират с висока реактивност. Повечето от техните реакции, причинени от присъствието на карбонилната група. въглероден атом в карбонилната група е в SP 2 хибридизация и образува три # 963 - връзка (един от тях е - C-O връзка), които са разположени в една равнина под ъгъл от 0 до 120 един към друг.
Структурата на съединение от групата карбонил
Най-важните реакциите на алдехиди са реакции на нуклеофилно допълнение към двойната връзка на карбонилната група.
1. Реакция с циановодородна киселина. Един от типични реакции на нуклеофилно присъединяване е добавянето на алдехиди с циановодородна (tsianovodorodnoy) киселина, което води до образуването # 940; - oksinitrilov:
2. Взаимодействие с алкохоли. Алдехидите могат да взаимодействат с една или две молекули на алкохол за да се образува ацетали и полуацетали съответно. Полуацетали са съединения, съдържащи въглероден атом с една хидроксилна група и алкокси група. Ацетали - съединение, съдържащо един въглероден атом с две алкокси групи:
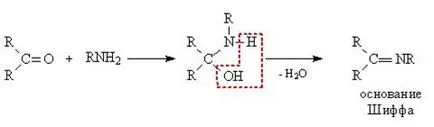
3. Взаимодействие с амоняк и амини. Реакция с амоняк и амини е от тип "закрепване-разцепване" на първия етап, връзката на амоняк или амин, и в един втори етап, премахването на вода, за да образуват двойна връзка между карбонил въглероден атом и амино азотен атом. Така оформен съединения, наречени Шифови бази - съединения, съдържащи група> С = NR. Съединения, образувани чрез добавяне на амини, наречени имин. хидроксиламин - оксим. хидразин - хидразон.
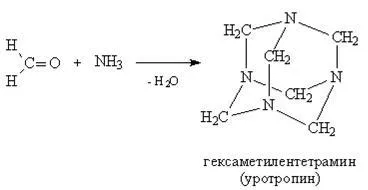
формалдехид с амоняк реакционният продукт на малко по-различен - е резултат от три под-молекулна циклизация, в резултат на скелет хексаметилентетрамин съединение се използва в медицината като метенамин препарат.