Belousov - Zhabotinsky реакция - химически енциклопедия
Belousov - Zhabotinsky реакция. протичащ в avtokolebat. Режим katalitich. окисляване декември намаляване на бромна към едно NVrO3. В същото време има колебания в концентрацията на окислени и редуцирани форми на катализатора и на някои междинно съединение. продукти. P-TION е в киселинен воден р-D; катализатори в Qual-ве използване на променлива валентност метални йони. напр. Ce или Мп, в Kutch-положителни намаляване - малонова до ТУ, ацетилацетон и др Belousov -. Zhabotinsky реакция - Naib. учи хомогенна осцилаторна реакция. откриване на рояк, предизвика рязко покачване на химически изследвания. колебания и е довело до създаването на нова област на химически. кинетика.
Опростена схема Belousov - Zhabotinskii реакция включва няколко. Метод: 1. разклонена верига, р-ТА окислител автокатализаторите NVrO2; Резултатът е самоускоряващо окислителен катализатор Мп +.
2. Инхибиране на окисляване чрез бързо р-ТА, разклонена верига терминатори:
4. Редукция на окислена форма на катализатора М (п + 1) + и образуване инхибитор едновременно - BR -.
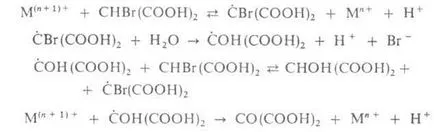
Т. Пр. механизъм р-ТА може да бъде представен mnemonich. схема (фиг. 1), където автокатализаторите осигурява NVrO2
директно Lay. обратна връзка (показано от +), и затваря веригата otritsat инхибитор. обратна връзка (-). Kolebat. цикъл може да бъде качествено, описана както следва. начин. Когато концентрацията на M (п + 1) + в системата е достатъчно голям, скоростта на Br - и концентрацията му в р-D също висока. В резултат, р-ТА окисляване верига Мп + се инхибира, и концентрацията на M (п + 1) + капки, с тенденция към своята прагова стойност, докато постигане притежавани до Br концентрация - пада рязко и NVrO2 увеличава концентрация. Разклонена верига, р-ТА и концентрация ускорява М (п + 1) + започва да се увеличава, с тенденция към върха. праг, когато концентрацията притежавани до Br - отново увеличава рязко прекъсване разклонена верига, и цикълът се повтаря. Колебанията в концентрациите на окислени и редуцирани форми на катализатора са придружени от трептения оцветяване г-ра от безцветен до жълт ако катализаторът - цериеви йони. или от синьо до червено в случай фенантролин железен комплекс [Fe (фен) 3].

Фиг. 1. Реакционна схема Belousov - Zhabotinskii (RBr-бромо редуктор).
Белоусов - Zhabotinsky реакция показва голям брой разл. kolebat. режими, притежавани до зависят от m-тура, киселинността и концентрацията на изходните реагенти. Периодът на осцилация може да варира от десети от секунди до десетки минути. Има прост периодичност. колебания декември образуват сложни трептения с няколко. максимуми за един период, а номеронабиране стохастичен. колебания (вж. фиг. 2). По време на Белоусов - Zhabotinsky реакция в затворена система, може да се наблюдава до няколко. хиляда цикъла; колебания в реактор поток се поддържат неопределено време. В неразбърквания р-Re, където се елиминира конвекция, има използвате концентрация. вълна самоподдържаща формиране динамично. структура (фиг. 3).
P-ЛИЗАЦИЯ B. P. Belousovym открит през 1951 г., тя е изследван подробно A. М. Zhabotinskim през 1964.
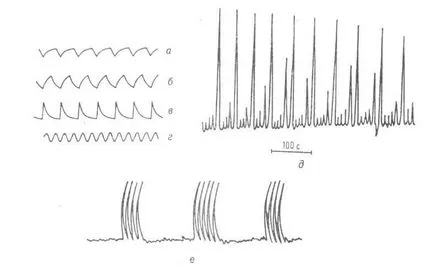
Фиг. 2. декември Видове концентрация трептения Ce 4+ идеално смесване в реактора. и - в - трионообразно трептения с разлагане. съотношението на дължината на предния и задния край; R - синусоидални трептения; Д-р хаотично. колебания; Е-преходно трудно периодични трептения.
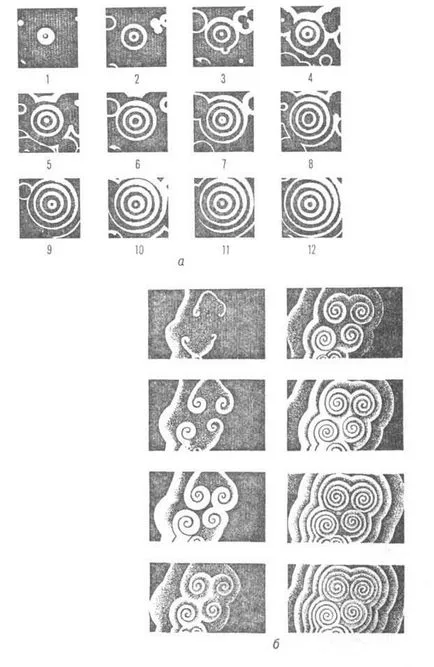
Фиг. 3. Dynamic. структури, образувани от течаща концентрация. вълни в слой neperemeshnvaemogo катализатор тънък г-ра ([Fe (фен) 3], интервалът между рамки 15с; voln0,01 скорост см / сек): и - концентричността. вълна от точков източник - главния център; дължина на вълната на 0.55 cm; б - спирални вълни; 0.15 cm.
===
App. Литература за статията "Белоусов - Zhabotinsky реакция". Zhabotinskiy A. М. Концентрация трептения, М. 1974 LS Polak, Михайлов A. S. Самостоятелно организация nonequilibrium физико-химични системи, М. 1983; Трептения и пътуващи вълни в химически системи, N.7 Y. 1985.