8 курс на химия, дистанционно обучение Разбира се, Chemistry, 8 клас оксиди и основни химични свойства
Вие се срещна с клас "оксиди" класификация оксиди.
Важно е да се научат да се разграничат киселинни, основни оксиди, и техните реакционни продукти с вода представляват различни класове на неорганични съединения.
Ако дори тези оксиди ви отличават лоши, трябва да се върнете към предишния урок и да разберат разликите между киселинни оксиди от основната.
Надявам се, че сте се научили да се прави разлика между основни и киселинни оксиди.
И така, химичните свойства на оксиди:
1. Взаимодействие с вода оксиди. Взаимодействието на водоразтворими окиси образуват хидроксиди. С други думи, ако оксид хидроксид съответства разтворим, оксид реагира с вода, е възможно.
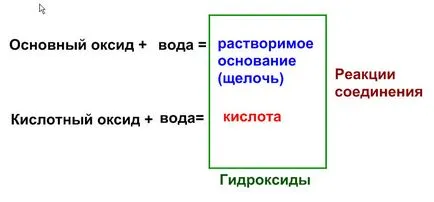
1) Взаимодействие на основни оксиди с вода.
Ние твърдим, по случая. натриев оксид - основен оксид, тъй като това е равно на валентността на метален оксид е 1. Съгласно настоящото схемата, реакцията протича с образуването на разтворима основа.
Ние образуване на база получени формула:
натриев валентност е 1, така формулата на натриев хидроксид
Според разтворимост Таблица - е разтворима основа (алкални) по този начин такава реакция е възможно.
Част от пълното уравнение:
Na2O + H2O = 2NaOH
Тъй като този оксид bariya- основен оксид, то съответства на база - Ва (ОН) 2. Ако си спомняте, броят на хидроксилни групи се определя от валентността на метала. Бариев - Група 2 елемент, валентност е равно на 2.
разтворимост Таблица се определя като разтворима основа (алкални). Следователно, такава реакция е възможно.
Реакция уравнение: BaO + H2O = Ва (ОН) 2
Пример 3.
Основен меден оксид (II) съответства на основата на Cu (OH) 2. Тази база е неразтворим (вж. Таблица разтворимост). Следователно, такава реакция не може да се случи.
При написването на тези уравнения реакции използват подобни разсъждения.
2.Vzaimodeystvie кисела вода-оксид
Серен оксид (IV) е киселинно, тъй като това е не-метален оксид, където сярата има валентност, равна на 4.
Форма съответния киселинен формула. Киселините на място в първото място писмено водород и кислород на последно място. Запишете реда марка водород, сяра, кислород. Броят на атомите на всеки елемент е решен от лявата страна на уравнението:
SO2 + H2O = H2SO3

Имайте предвид, че формулата хидроксиди киселини, получени чрез добавяне формули оксиди и вода. Тази техника може да се използва и когато трябва да се направи формула, съответстваща на тази киселина оксид.
Р2О5 + H2O = [H2P2O6] = 2HPO3 или Р2О5 + 3H2O = 2H3PO4
Формулата в скобите - е междинен запис, ако броят на атомите на всички елементи - е четно число. Е намалял с 2, ние се получи желаната формула. 2 става фактор. Във втория случай, фосфорна киселина (формула сте научи) в гореща вода. Коефициентите са разположени известни искате.
Не забравяйте, киселини и основи са общо име - хидроксиди.
Взаимодействие на основни и амфотерни оксиди с киселини.
Основни оксиди + = киселина сол и вода.
Тези реакции протичат в зависимост от вида на обмен.
Пример 1.
BaO + HNO3
от дясната страна на уравнение е необходимо да се соли с формула: запис до метал, образувайки основния оксид - Ва, и киселинен остатък на NO3 азотна киселина. Направете сол на формула валентност формула за добавяне на вода от дясната страна на уравнението и да организира коефициенти.
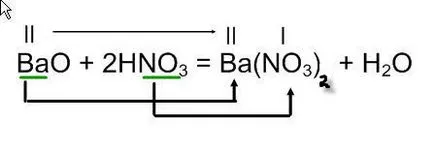
В резултат на реакцията на бариев оксид с азотна киселина се образува от бариев нитрат и вода.
Пример 2.
K2O + H2SO4 =
Получената сол на реакцията (от дясната страна на уравнението) писане на първо място метален калий в vtorom- сярна киселина остатък SO4 kicloty
Според валентност образува сол с формула, формули и проверка на запълване вода коефициенти.
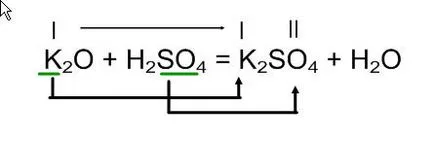
Взаимодействието на калиеви оксиди със сярна киселина за получаване на калиев сулфат и вода.
Подобни уравнения реакция е съгласно този алгоритъм.
Киселинни оксиди реагират с разтворими основи (алкални). Не забравяйте какво основание принадлежат към групата на основи.
Киселият оксид + = алкална сол + вода
Пример 1.
КОН + CO2 =
В този случай, за да се сол с формула, е необходимо да се разбере, която съответства киселина киселинен оксид.
В дясната страна на уравнение, запис части сол: метална база, и К CO3 киселинен остатък на киселина Н2СО3. което съответства на киселина оксиди СО2. След това се сол съгласно валентността формула добавяне дясната страна на уравнението и да осигури съотношение вода.
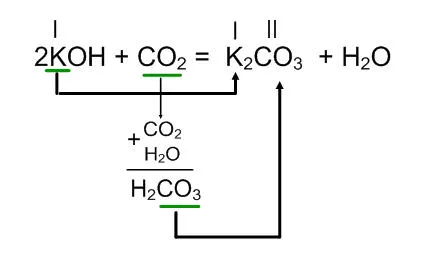
Взаимодействието на калиев хидроксид (алкален) с въглероден диоксид газ (въглероден оксид (IV)) са оформени с натриев карбонат и вода.
Пример 2.
Ва (ОН) 2 + SO3
Изравнява за описаната по-горе алгоритъм:
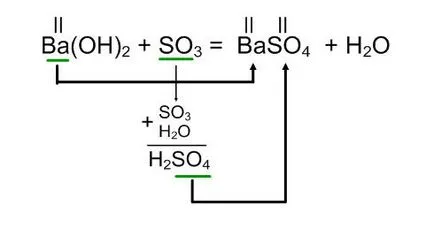
Реакцията на бариев хидроксид с окис на сяра (VI) е оформен на бариев сулфат и вода.
Прекарано в близост тази последователност от действия.
И още един общ имот на оксиди:
Взаимодействие на киселинни и основни оксиди помежду си.
Киселият оксид + = основен оксид сол
Пример 1.
Na2O + Р2О5 =
Реакцията на киселинната сол се получава, което съответства на даден оксид. Алгоритъмът е подобен на алгоритъм за съставяне на уравнения взаимодействие киселинен оксид с основа.
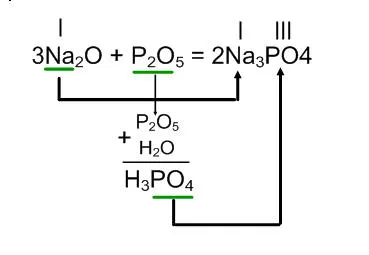
Реакцията на натриев оксид, фосфорен оксид (V) е оформена с натриев фосфат.
Пример 2.
BaO + SO3 =
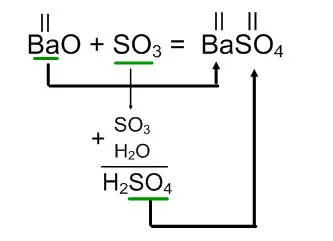
Реакцията на бариев оксид с окис на сяра (VI) е оформен на бариев сулфат.
Прекарано на алгоритъма на действията.
Ние разгледа химичните свойства на оксиди, които са общи за солеобразуващи (киселинни, основни) оксиди. Оксиди със специфични свойства, ние постепенно ще се запознаят с други теми.
За да обобщим и представя общите свойства на киселини и получаване под формата на таблици.
Таблица 1. Химични свойства.