процес Chemistry назначаване на сярна киселина алкилиране на изопарафини с олефини
Процесът на назначаване на сярна алкилиране на изопарафини с олефини киселина. Основните и странични реакции, осигуряват механизъм. условията на процеса. Технологични особености на процеса и технически решения, свързани с тях, на какъв етап е процесът. Избор на вида и конструкцията на реактора
Този метод за синтез на високооктанов компоненти на авиацията и автомобилни бензини. При алкилиране на изобутан с изобутилен реакция може да бъде представена както следва:
Реакцията на алкилиране на сярна киселина с изопарафини олефини протича селективно. Най-лесно е да се подложи на алкилиране на изобутан и изопентан, т.е. изопарафинови въглеводороди с третичен въглероден атом в молекулата. Парафинови въглеводороди с кватернерен въглероден атом в молекулата на тип 2,2-диметилбутан алкилирани значително по-трудно и по-строги условия. С права или разклонена верига, парафини, съдържащи както третичен кватернерен въглероден атом не е по същество алкилира в присъствието на сярна киселина.
Олефини за алкилиране могат да се предприемат различни. Въпреки това, най-малко ефективна етилена алкилиращ агент. Алкилиране на пропилей и п-бутен дава добри резултати при алкилирането на изоамилени започват да се формира в голямо количество разрушителни продукти на алкилиране и по-високи олефини в алкилирането на тези реакции започват да преобладават.
Обикновено, изобутан се алкилира с н-бутени, защото където образува изомерен въглеводороди C8H18 (trimethylpentanes) при температурата на кипене на най-подходящи като компонент на моторни горива. Въглеводороди C8H18, но друг вид (диметил) се получават в алкилирането на изопентан с пропилей, в допълнение, изопентан е ценна суровина за производство на изопрен, така че се използва за алкилиране рядко (понякога се добавя към изобутан).
Структурата на продуктите, образувани по време на каталитично алкилиране на изопарафини с олефини, обикновено не е в съответствие с очакваната структура на изходните материали. В реакцията на N-бутени с изобутан, смес от 2,2,4-, 2,3,4 и 2,3,3-триметилпентан.
Причината за несъответствие на структурата на продуктите е в характеристиките на механизма за реакция, сложния процес на изомеризация. Механизмът на алкилиране карбониев йон верига:
малки количества от олефин (бутен-2) взаимодействат с протонна киселина;
срещащи вторичен carbocation образуван от п-бутен, по-малко стабилен от третичен, при което има бърз обмен на хидрид йон с изобутан;
трет-butilkation образува допълнителни реагира с изходния олефин carbocation да се образува по-високо молекулно тегло;
Получената carbocation податливи на вътрешномолекулни пренареждане, придружени от миграцията на водородни и метилови групи;
Тези карбокатиони реагират с изобутан, чрез което се произвежда въглеводород C8H18 tretbutilkation и осигурява поток от процес йон верига
1. Условията на реакцията алкилиране в част карбокатиони, образувани от изопарафини в присъствието на катализатор губи протон за да се образува съответния олефин, който взаимодейства с новия carbocation по обичайния начин и образува наситен въглеводород, т.е. avtoalkilirovanie изопарафини появява.
2. В случай на липса олефин avtoalkilirovanie води до прекомерна консумация на изопарафин.
3. Izooktilkation също способен на взаимодействие с олефини. Така се случи серия паралелна реакция на алкилиране, и за потискане на образуването на висши въглеводороди, изисква излишък на изопарафин по отношение на олефина.
4. Реакция avtoalkilirovaniya сложни, освен това, че унищожаването на част от въглеводородите формира, като по този начин производство на продукти ниско молекулно тегло. Тази реакция допринася за повишаването на температурата.
5. Друга страна реакция - катионна полимеризация олефини, които се получават при ниско молекулно тегло ненаситени полимери, някои влошаване качеството на алкилиране и да доведе до повишена консумация на катализатор.
6. Част от олефини взаимодейства с концентрирана сярна киселина с освобождаването на две молекули вода.
Обосновка на условия на алкилиране сярна киселина на изобутан с бутени:
Реакцията на алкилиране на изопарафин с олефини е екзотермична. При температури под 1000 ° С, равновесието се измества надясно, реакцията е практически необратими. Температурата на алкилиране се избира така, че максималната потиска странични реакции и разграждане на полимеризацията, но остава достатъчно висока скорост процес. В този случай, температурата се поддържа 5-130S.
Налягането няма значителен ефект върху процеса на течна фаза при ниска температура. Той е избран за технологични причини малко по-големи от налягането на обработваните въглеводороди при температура в реактора, за да се осигури поддържането им в течна фаза. При отстраняване на реакционната топлина чрез изпаряване на част от увеличението на въглеводород налягане не е практично, защото затруднява изпаряване. При алкилиране на изобутан с бутени поддържат при налягане от 0.35-0.4 МРа.
Концентрацията на киселина трябва да бъде най-малко 88-86%. в процеса да се разреди с високо молекулно съединения (естери на сярна киселина, VM въглеводороди) и вода, идващи от суровината и освободени в резултат на някои странични реакции. Следователно, киселината трябва да бъдат засилени.
Съотношението на киселина. въглеводороди подкрепят от 1. 1 до 2. 1.
Съотношението на изобутан. олефин вземат от 1 до 10. 4. 1. Колкото по-висока концентрация на изобутан в суровината, на по-благоприятни условия за поява на реакция на алкилиране първичен и потискане на полимеризацията и други странични реакции.
Технологични особености на процеса:
Трябва да се създаде стабилна емулсия киселина - въглеводороди - необходимо интензивно смесване;
реакцията протича при ниски температури и екзотермичната - изисква интензивно пренос на топлина и поддържа режима на изотермични;
Използването на голям излишък на изобутан води до голямо множество циркулация на реакционната маса и необходимостта да се разделят и да се възстанови нереагирал изобутан;
в разреждане сярна киселина - трябва да се премахне част от него да се засили и да добавите пресни.
трябва да се твърди, сярна киселина и да се измие неговите останки от реакционната маса.
Етапите, които правят процеса на алкилиране сярна киселина:
подготовка суровина - почистване на примеси от въглеводородни потоци (сероводород, меркаптани, вода) - алкална и воден пране, сушене от вода чрез използване на адсорбенти.
обработка на въглеводородна смес, излизаща от реакторите - защитата на киселина неутрализиране на остатъчна киселина с алкален, промиване гореща вода
фракциониране продукти - първо в първата колона се разделят изобутан и пропан от други стоки, и след това се отделят от изобутан с пропан, п-бутан е повече отделени от алкилиране.
се използват реактори алкилиране на различни видове:
Капацитивен използвайки дистанционно циркулационни помпи за реакционната смес (на дъното на плаките или прегради подредени за интензивно смесване на компонентите);
Контактор с вътрешни циркулационни устройства и охлаждащите елементи (вертикална и хоризонтална - отличителна черта на последния - охлаждане с поток продукт изходящ от реактора, и изходна суровина инжектиране и се прилага киселина);
каскада с вътрешен охлаждане и циркулационни устройства без вътрешни елементи охлаждане (хоризонтална апарат, разделени с прегради в реакционната зона и утаяването)
В зависимост от системата за охлаждане прилагат реактори също са разделени на три типа:
затворен охлаждащ цикъл с помощта на охладител и - амоняк, пропан, бутан (капацитивни и контактор реактори);
охлажда изтичащия поток поради изпаряване, когато налягането в устройството след реактора и допълнително кондензиране поток пара преди връщане към реактора (контактор реактори);
с вътрешно охлаждане чрез изпаряване, съдържащи се в реакционната смес от пропан и изобутан при понижено налягане във вътрешността на реактора (каскада реактор) на.
Пиролиза. Процесът на назначаване. Добави пиролиза механизъм например пентан. Редица съединения за увеличаване на стабилността по време на пиролизата на метан до пентан, включително изомери и ненаситени съединения. методи за преработка по време на пиролиза за увеличаване на добивите на продукта.
Пиролиза - метод за получаване на по-ниски олефини.

Метан - Етилен - Етан - Пропан - пропилен - Основно - Средно - Висше
Увеличаване на капацитета й с пара или да предоставят още по-добре водород
Реформиране. Процесът на назначаване. Реформиране на катализатори. Какви са възможно схемата за реактор реформиране. Обяснете как те работят. Както промяна на температурата по време на процеса в зависимост от времето на катализатора и на схемата на процеса. Формулите на реакциите.
Основната цел KT за реформиране досега остава увеличение antiknock моторни горива, но не по-малко важно е използването на този метод за получаване на ароматни г / в - бензен, толуен и ксилен.
Като катализатори се използват бифункционален катализатор, съдържащ метал от платиновата група поддържа върху двуалуминиев триоксид и повишен с халоген. Катализатори са monmetalicheskimi (платина върху двуалуминиев триоксид) и полиметални.
Kt полиметални реформиране заедно с Pt съдържа няколко други метали. Използвани за насърчаване на метали могат да бъдат разделени на 2 групи. Първият от тях са иридий, рений, добре известен като кт хидро дехидрогениране gidrogenaliza. Друга по-широка група от промотори включват метали, които са практически неактивни в горните реакции. Такива метали включват мед, кадмий, германий, калай, олово, и т.н. Повечето от системите също да съдържа, в допълнение към платина, два елемента, единият от които принадлежи на първата група, а другият -. Секунда. Така, ако Al - KT Pt повишен repiem, КТ прилага един от следните метали: Cu, Ag, кадмий, цинк, индий, редкоземни елементи - лантан, церий, неодим и други.
Технологично процес е фиксиран или легло движещ катализатор. Когато суровина с неподвижен слой се подава в каскада от три адиабатни реактори. Растението с реактор с движещ се слой катализатор, използвайки три, оформен в една структура и разположени една над друга.
Във всеки вариант, съотношението на обем катализатор в секциите на 1/2/4. Това се дължи на факта, че съотношението на скоростта на дехидрогениране, дехидроциклизация и изомеризация е 4/2/1.
основни реформинг реакции.
В основата на този процес са три вида реакции. в / в най-важните реакции, водещи до образуването на аргон.
1. дехидрогенирането на шест-членни нафтени:
2. dehydroisomerization петчленни нафтени:
3. ароматизация (дехидроциклизация) парафини:
Друг тип реакция характеристика на реформиране - изомеризация. Заедно с изомеризация на 5-членен и 6-членен нафтен изомеризация изложени като парафини и ароматни съединения в / инч
Методи за получаване на естери. Основните продукти и тяхното приложение. Условия за реакцията на естерификация на органични киселини с алкохоли. процесни катализатори. Технологични имоти реакция на мястото клирънс естерификация.
1. Взаимодействието на киселини с алкохоли:
Това е най-често срещаният метод за получаване на естери.
2. Синтез на естери чрез кондензация на алдехиди:
Синтез на естери от алдехиди (реакция Тишенко) се провежда в присъствието на алуминиев алкоксид, железен хлорид или активиран по-добре, алуминиев хлорид и цинков оксид. Този метод има промишлено значение.
3. Свързване на органични киселини на алкени:
4. Синтез на естери чрез дехидриране на алкохоли:
5. Получаване на естери от трансестерификация.
Тази реакция има два варианта: реакцията обмен между етер и алкохолни радикали алкохол (алкохолиза реакция):
и реакцията обмен на киселинни радикали в алкохолната група с етер:
6. Синтез на естери от киселинни анхидриди и алкохоли:
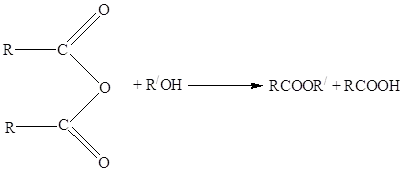
7. взаимодействие на кетони с алкохоли:
8. Взаимодействието между халогениди и алкохоли:
9. Реакцията между сребро или калиеви соли и алифатна киселина халогенни производни:
10. Взаимодействието на киселини с алифатни диазо съединения (главно с диазометан):
Основните продукти на реакцията на естерификация са естери, използвани като разтворители, пластификатори, синтетични масла и хидравлични течности, ароматични вещества, мономери.
Естерификацията на алкохоли с карбоксилни киселини може да се проведе в отсъствие на катализатор, но в този случай това е бавен и за да се постигне достатъчна скорост изисква високи температури (200-300 С). Но когато се използва катализаторът е трудно да се измие, тя се използва не-каталитичен процес. В присъствието на киселинни катализатори на естерификацията протича при температура от 70-150 ° С за
Най-честите етерифициране катализатори са минерални киселини: сярна, фосфорна. бензенсулфонова киселина може да се използва, толуенсулфонова киселина и т.н. Голяма група катализатори включват соли с органични и неорганични киселини. Те могат да се използват като катализатори на естерификацията :. Титанов пероксид молибден върху инертен носител, активен алуминий етоксид, титанови алкоксиди и др нарастващото използване на йонообменни смоли се получават като катализатори.