Процедурата за държавна регистрация на БАН в Русия
Съжаляваме, но вашият браузър не поддържа възпроизвеждане на аудио файла. Опитайте с друг браузър
Съжаляваме, но вашият браузър не поддържа възпроизвеждане на аудио файла. Опитайте с друг браузър
BAD процедура държавна регистрация
на територията на България
Помислете за процедурите на юридическото лице (производител или продавач), взе решение да произвежда и / или снабдяване на пазара с биологично активни добавки (по-нататък - БАН).
Трябва да се отбележи веднага, че нито една организация не е разрешено да извършат продажба на дребно на хранителни добавки (в съответствие с ал. 7.4. SanPin 2.3.2.1290-03. Дребно добавки чрез аптеки (аптеки, аптеки, магазини, аптека, и т.н.), или специализирани магазини за продажба на здравословни храни, хранителни магазини (специални отдели, секции, павилиони), не се вземат добавки, без реализацията на съответните разпоредители с документи, а именно:
- сертификат за държавна регистрация на територията на България;
- сертификат за качество за BAA от производителя.
Първият документ, с лице на производителя - е SanPin 2.3.2.1290 - 03 "хигиенните изисквания за производство и оборот от биологично активни добавки (БАД)". Той определя редица акценти, полага основите за по-нататъшното съдбата на хранителни добавки, а именно:
- изисквания за производство на БАД на техническа документация (razdelIIISanPiN 2.3.2.1290 - 03). Заслужава да остане и да се наблегне на факта, че не можете да вземете захар и лимонена киселина, разбърква се и запис като хранителна добавка. Такъв продукт ще бъде прекратено на етапа на проучване на техническата документация: технически спецификации (ТУ) и технологичната инструкция (Ti);
- изисквания за опаковките и допълнения в информацията върху етикетите (razdelIVSanPiN 2.3.2.1290 - 03). Когато се кандидатства за разглеждане BAA потребителска опаковка трябва да бъде снабден с винетка, на която информацията се регулира от законодателството, прилагано в бъдеще, ако BAA ще бъде домакин успешна регистрация, производителят ще трябва да се приложи към всеки номер етикет на удостоверението за държавна регистрация и датата на издаването му;
- Санитарно - епидемиологични изисквания за производство на хранителни добавки. Тази позиция се отнася преди всичко до производителя. Без получаване на санитарно - епидемиологично заключение, в което териториалния орган Rospotrebnadzor (Приложение 2 на броя на административните разпоредби) ще даде положителна оценка на условия (с други думи, да ги наричаме "значение"), производство и регистрация на хранителни добавки не са възможни.
По този начин, производителят е разработил спецификации, TI е разработена и произведена оформление етикет, получил санитарно - епидемиологичен сертификат за производство.
Сега той може да пристъпи към следващия етап на регистрация BAA: производството BAA партида, това се опаковат в пакет потребител, съответстваща SanPiN2.3.2.1290 - 03. си етикети и в съответствие със същия нормативен документ и да започне процеса на регистрация.
Регистрация власт ( "опит" център Rospotrebnadzor www.crc.ru) следните документи (приложение № 5 към броя на административните разпоредби):
- отчет, изготвен в съответствие с приложение 4 към административните разпоредби - ТУ, вт рецепта за добавки, които се предполага да извършва промишлено производство на продукти, сертифицирани в съответствие със законодателството на Република България;
- Ако ТУ и TI Производител вече са преминали преди прегледа, трябва да предоставите на санитарно - епидемиологично заключение за потвърждение, сертифицирани в съответствие със законодателството на Република България;
- Санитарно - епидемиологичен сертификат за съответствие с условията на изискванията за производство на държавни санитарно-епидемиологично правила и норми, сертифицирани в съответствие със законодателството на Република България;
- инструкции за употреба (вложени в опаковката, абстрактно) (ако цялата необходима информация, не могат да се поставят на етикета), заверени от упълномощен подпис и печат на производителя;
- на потребителите (или тара) етикет или неговия проект, сертифициран от упълномощен подпис и печат на производителя;
- протоколи за изпитване на акредитираните лаборатории за изпитване (центрове), заключенията на акредитираните организации (органолептични, физикохимични, микробиологични, радиологични изследвания (тестове), изучаване на допустимото съдържание на химически, радиологични, биологични, забранени компоненти и техните съединения, микроорганизми и други биологични агенти, представляващи опасност за човешкото здраве, в съответствие с държавния санитарен и епидемиологичен правила и разпоредби);
- актът на вземане на проби (извадки) фиксирана форма - с търговска марка - копие на търговска марка, надлежно заверени
- Когато производителят и заявителят са различни юридически лица (или от производителя, представя на органа за регистрация на физическо лице), при подаване на заявление и набор от документи, необходим адвокат на производителя, че той се доверява на заявителя да представлява техните интереси на територията на България за прилагане на държавна регистрация на продукти на производителя както и пълномощно за правото да получи сертификат за държавна регистрация на хранителни добавки.
Връщайки се малко назад, ние се отбележи, че в ръцете на нас имат всички документи от списъка, с изключение на един: протокола от изпитването от акредитирана тест център (лаборатория).
Експертиза (санитарно-епидемиологичната експертиза, както и изследвания, тестове, токсикологични, хигиенни и други видове оценки), необходими за държавна регистрация, се упражнява от федерални агенции - хигиена и епидемиология центрове (списък от съоръжения на разположение на официалната интернет страница на Федералната служба за надзор в защита на правата на потребителите и благополучието на хората: www.rospotrebnadzor.ru), други организации, акредитирани в съответствие с установената процедура (списък на организациите първо, публикувана на официалния сайт на Федералната агенция за техническо регулиране и метрология: www.gost.ru).
Чума "Федералната център по хигиена и епидемиология" на Rospotrebnadzor.
«Център за хигиена и епидемиология в Москва" Rospotrebnadzor.
Научноизследователски институт по трудова медицина на медицинските науки (по споразумение).
Научно-изследователски институт по екология на човека и околната среда ги хигиена. AN Sysina науките (по споразумение).
Федерален изследователски център по хигиена тях. F.F.Erismana Rospotrebnadzor.
Научно-изследователски институт по хранене (да се съгласи).
Научно-изследователски институт по хигиена и здравеопазване за деца и юноши на медицинските науки (по споразумение).
Институт за физични и химични медицина (по споразумение).
Българската академия на следдипломно обучение Медицински университет (както е договорено).
FSIS "Sofiyasky изследователски институт на Радиационна хигиена след професор PV Ramzaev "Rospotrebnadzor.
Разбира се, това не отрича правото да кандидатстват за протокол от изпитване на производителя в друга акредитирана за такива изследователски център или лаборатория, обаче, е посочено в списъка на лабораторни центрове са легитимни и издава своите доклади ще бъдат със сигурност, предприети държавна регистрация орган БАА на.
Процедурата по регистрация е завършена.
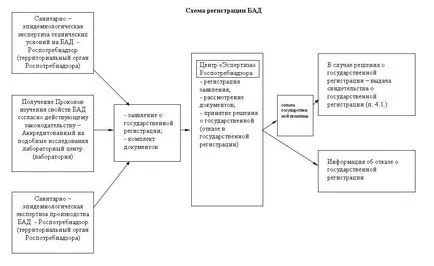
1. административна уредба
Федералната служба за надзор за защита на потребителите и правата на човешкото благополучие
Изпълнение на публични функции на държавна регистрация представен за първи път в производството в миналото да не се използват химични и биологични вещества и произведени въз основа на тях потенциална опасност за човешкото (с изключение на наркотици); Специфични продукти могат да създадат опасност за човешкото (с изключение на наркотици); Определен вид продукти включително прехрана, до внесения първата област, България (MS Word документ 404 KB)
2. SanPin 2.3.2.1078-01.doc (MS Word документ 3448 KB).
3. SanPin 2.3.2.1290-03.doc (MS Word документ 249 KB).