Опитно определяне на молекулно скорости
Експериментите за определяне на скоростта на молекули доказали валидността на формула (4.7.3). Един от експериментите се извършват от името на немския физик О. Стърн през 1920 г.
Експерименталната настройка е показана на фигура 4.15. Устройството се състои от съд 1, система от прегради 2, 3 и 4 цилиндър въртящи се при висока ъглова скорост.
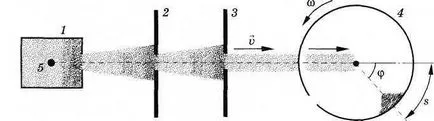
Съдът 1 е опъната тънка тел платина 5 покрити със слой от сребро. По жицата електрически ток се предава. Когато текущият слой от сребро се изпарява и съдът се напълва с газ на сребърни атома. Газът е в състояние на равновесие при температура Т, която може да бъде измерена.
В стената на съда 1 има малък отвор, през който малко количество сребро атома плаващи на контейнера в пространство, където се създава висок вакуум. Тук атомите не се сблъскват една с друга.
Използване жигльорни плочи 2, 3 се разпределя лъч атома насочени по диаметъра на въртящия цилиндър. Цилиндърът има тесен процеп. В момента, когато разликата е в пътя на лъча, малка част атома попада в цилиндъра и се движат към отсрещната стена. Разстояние равна на цилиндър с диаметър D на, летящите атомите време
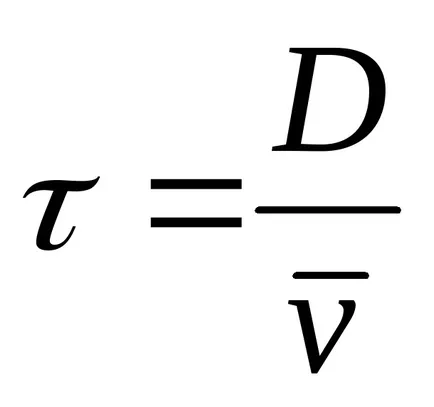

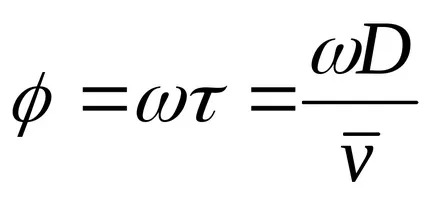
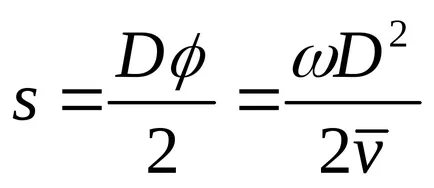
На вътрешната повърхност на цилиндъра, образуван от следа на сребро се утаява под формата на тъмни петна. дебелина петно не е същото навсякъде. В известна част от максималната дебелина на сребърен слой. Измерване на дъга дължина S, съответната максимална дебелина на сребърен слой, и познаването на диаметъра на цилиндъра и ъгловата скорост, е възможно да се определи средната скорост на молекулите съгласно формулата:
Изразява съгласие със стойност на средното квадратично скоростта изчислява по формулата (4.7.3), е съвсем задоволително. Това е експериментално доказателство за валидността на (4.7.3), и по този начин експресията (4.5.5), което предполага, че средната кинетична енергия е пряко пропорционална на абсолютната температура.
Измерване на дебелината на сребърни петна в различни места, е възможно да се изчисли броя на атомите приблизително, скоростта на които се намират в различни интервали от време. По този начин се извършва експериментална проверка на Maxwellian разпределение на скоростта. Споразумението с експеримент за разпределение Максуел също е задоволителен.
Средната скорост на Брауновото частиците
Формула (4.7.2) ни позволява да се разбере защо интензивността на Брауновото движение се увеличава с повишаване на температурата течност и намалява с увеличаване на масата на частицата. След брауново частиците участва в термично движение на молекулите. Затова, неговата средна кинетична енергия също се определя от формула (4.5.5) и средното квадратично скоростта - формула
където TB - масата на Брауновото частица. Ако масата на частиците е голям, средната скорост на движение му е толкова малка, че движението на частиците е почти невъзможно да се открие.
Брауново скорост на частиците в течност не може да се измерва директно, поради изключителната нередовността на брауново движение.
Средно молекулно скорост надвишава скоростта на звука и да достигне стотици метри до 1. Тези скорости са в състояние да се измери, тъй като макроскопски тяло (цилиндър на кърмата) могат да се отчитат по-голяма ъглова скорост на това по време на преминаването на молекулите във вътрешността на цилиндър се върти от значително количество.