Общи механизми на сърдечна недостатъчност
Инфаркт форма на сърдечна недостатъчност се характеризира с намаляване на напрежението, разработен от сърцето. Това се проявява есен сила и скорост на свиване и отпускане.
Претоварване форма на сърдечна недостатъчност се генерира, а повече или по-малко дълъг период на хиперфункция. Последният в крайна сметка води до намаляване на силата и скоростта на свиване и отпускане на сърцето.
В двата случая (и в случай на претоварване, и сърдечни увреждания) намаляване на контрактилната функция придружава от включването на екстра- и интракардиално компенсира това механизми за смяна. Всички от тях, независимо от най-известните идентичност, от гледна точка на целия организъм са свързани помежду си по такъв начин, че активирането на един от тях значително да повлияе на изпълнението на другия.
Mehanizmyekstrennoykompensatsiisokratitelnoyfunktsii
Механизми допълнително заплащане намалена съкратителната функция на сърцето, са показани на фиг. 22-25.

Фиг. 22-25. Допълнителни компенсаторни механизми намалени съкратителната функция на сърцето.
• Повишаване на свиването на миокарда под напрежение постъпващия кръв (механизъм Франк -Starlinga). Тя осигурява нарастващо напрежение, разработена от миокарда и скоростта на свиване и отпускане.
† Увеличаването на напрежението на развиващите се сърцето, извършена в отговор на нарастващото напрежение на миокарда. В тази връзка, механизъм, наречен Франк -Starlinga geterometricheskim, т.е. свързани с увеличаване на дължината на мускулните влакна.
† Увеличете свиване кардиомицит и скорост релаксация се развива в резултат на по-бързо освобождаване на Ca 2+ от калциеви депа (sarcotubules) и последващо бързо помпени Ca 2+ (Ca 2+ -ATPase) в саркоплазмичната ретикулум на резервоара.
• По-голяма сила от миокардни контракции в отговор на повишено натоварване. Той се среща с постоянна дължина на Миоцитно. Този механизъм се нарича gomeometricheskim, тъй като тя се осъществява без да се променя значително дължината на мускулните влакна.
• Увеличаване на сърдечните съкращения от увеличаване на сърдечната честота.
• Увеличение на сърдечните съкращения чрез увеличаване simpatikoadrenalovyh влияния. Характеризира се с увеличаване на честотата и силата на контракциите.
Симпатична инервация † инфаркт извършва Axon окончания адренергичните неврони на шийните горна, средна и звездообразна врата (цервикален-гръдни) ганглии.
† Активирането на симпатикови нерви води до положителен инотропен ефект. Повишена честота на спонтанни деполяризация мембрани пейсмейкъри, притежаващи импулс се улеснява в Purkinje влакна. увеличаване на честотата и силата на свиване, типични за кардиомиоцити.
† действие на катехоламини на кардиомиоцитите чрез 1 адреноцептори поради редица следващи събития: адреноцептор стимулация адреноцепторни агонисти (например, норепинефрин) чрез G-протеин активиран аденилил циклаза за образуване на сАМР активиране на сАМР-зависима протеин киназа фосфорилиране сарколемалното протеин р27 се увеличава в sarcoplasm влизане калций през отворените волтаж-зависимите Са2 + -channels засилено калций-индуцирана Са2 + мобилизация в цитозола чрез рианодинови рецептори активира в капачка koplazme значително повишава концентрацията на Са2 + Са2 + свързване с тропонин С тропомиозина облекчава инхибиторен ефект върху взаимодействието на актин с миозин произвежда повече актомиози-нова връзки увеличават намаляването на сила.
Kompensatornayagiperfunktsiyaserdtsa
Експлоатация на гореспоменатите механизми осигури допълнително плащане контрактилната функция на повредени или претоварен миокарда. То е придружено от значително и повече или по-дългосрочно увеличаване на интензивността на функционирането на сърцето - своята компенсаторна хиперактивността.
Kompensatornayagipertrofiyaserdtsa
Инфаркт на хиперфункция предизвиква експресия на отделни гени кардиомиоцити. Той проявява увеличение на интензивността на синтеза на нуклеинови киселини и протеини. Ускоряване на синтезата на нуклеинови киселини и протеини на миокарда води до увеличаване на неговата маса - хипертрофия. Биологичното значение на компенсаторна хипертрофия на сърцето се крие във факта, че повишеното телесно функция изпълнява увеличената тежест.
Mehanizmydekompensatsiigipertrofirovannogoserdtsa
Потенциалът на хипертрофирано миокард и увеличаване на силата и да се намали скоростта не е неограничен. Ако сърцето продължава да работи с повишено натоварване или го е допълнително повредена, силата и скоростта на падането му курс и техните енергийни "Разходи" се увеличава: развиващите декомпенсация хипертрофирано сърце.
Механизми декомпенсация хипертрофирани сърца са посочени на фиг. 22-26.
Фиг. 22-26. Основните механизми на хипертрофирано сърдечна декомпенсация.
В сърцето на декомпенсация дълго хипертрофирано миокард е нарушение на балансиран растеж в различните й структури. Тези промени - заедно с друга (виж фигура 22-26.) - в крайна сметка води до намаляване на сърдечната честота и сила на скоростта на свиване на процеса, т.е. - развитието на сърдечна недостатъчност.
Cell-molekulyarnyemehanizmyserdechnoynedostatochnosti
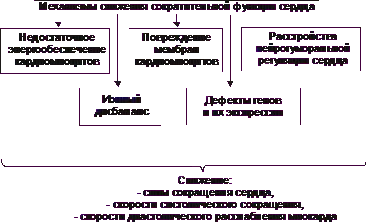
Намаляването на съкратителната функция на сърцето е резултат от сърдечна недостатъчност на различни етиология. Въпреки разликата в причините и известен Особеността на първоначалния патогенезата на сърдечна недостатъчност, механизмите на клетъчно и молекулно едно ниво. Основните от тези механизми са показани на Фиг. 22-27.

Фиг. 22-27. Основните механизми за намаляване на миокардната функция контрактилна сърдечна недостатъчност.
• Липса на миокардните клетки за доставка на енергия
Разстроен доставка на основните процеси, протичащи в миокардните клетки (основно своята свиване и отпускане), се развива в резултат на нарушения: ресинтез macroergs, транспорта им енергия за ефекторни структури на кардиомиоцити, използване на енергията на съединения високо енергийни фосфат. Те обикновено патогенеза обсъдени в Глава 4, "Патология клетки" (виж "Общи механизми за щети", подраздел "нарушения на клетките на доставка на енергия").
Нарушаването на предоставяне кардиомицит енергия за етапи на производството, транспортирането и обезвреждането може да бъде изходен механизъм за намаляване на съкратителната функция на сърцето, както и важен фактор за растежа на своята депресия.
• Увреждане на мембраните и ензими кардиомиоцитите
Увреждане на клетъчните мембрани и ензими обсъдени в Глава 4, "Патология клетки" (виж "Общи механизми увреждане", подраздел "увреждане на мембрани и ензими").
Промяна на мембрани и ензими на миокардни клетки - основна и често ПЪРВОНАЧАЛНА връзката на патогенезата на сърдечна недостатъчност. Промени в физикохимичните свойства и структурата на молекулите на протеин (структурни и ензими), липиди, фосфолипиди и PL придружени от значително обратим и често - необратимо увреждане на структурата и функцията на мембраните и ензими, включително - митохондриите, саркоплазмения ретикулум, миофибрили, плазмена мембрана, осигуряване на изпълнението на функцията на свиване на сърцето и ритъм.
Доклад и съотношения между отделните йони в и извън клетките са обсъдени в Глава 4, "Патология клетки" (виж "Общи механизми увреждане", подраздел "йонен дисбаланс и вода в клетка"). По-долу са специфични за развитието на сърдечна недостатъчност, особено йонен дисбаланс.
Йонен дисбаланс в сърдечна недостатъчност се проявява съотношение нарушение между отделните йони в различните сектори на кардиомиоцити: в органели (митохондрии, саркоплазмени ретикулум миофибрили) в цитозола, на противоположната страна на плазмената мембрана на кардиомиоцити. За най-голяма степен се отнася до йоните: К +. Na +. Са2 +. Тези катиони се определят главно от прилагането на процеси като възбуждане, електро-конюгиране, контракция и релаксация на миокарда.
• Нарушения в генетичните програми на кардиомиоцитите
Нарушенията в генетичната програма на клетки и / или механизми за прилагането му са обсъдени в Глава 4, "Патологията на клетката" ( "Общи механизми на увреждане", подраздел "генетични заболявания").
При сърдечна недостатъчност активиране на гени, които контролират процесите актуализират субклетъчни структури на кардиомиоцити, както и растеж микроваскуларни и нервни влакна. По-специално, исхемично увреждане на сърцето и стрес потиска експресията на иРНК за Са2 + -зависими ATPase саркоплазмения ретикулум. Това инхибиране потенцира улавяне и освобождаване процес ретикулум Са2 + миоцити. В условията на исхемия и инфаркт на миокарда, хронична емоционален стрес потиска болка като процес на транслация на генетичната информация. Това е придружено от нарушение на синтеза на различни протеини миокардни клетки.
• нарушения на неврохуморален регулиране на сърцето
Общи характеристики на нарушение на регулирането на клетъчните функции, се отнасят до Глава 4, "Патологията на клетката" ( "Общи механизми на увреждане", подраздел "Нарушения на регулирането на вътреклетъчните процеси"). The се обмислят следните важни за развитието на сърдечна недостатъчност, промени в симпатична и парасимпатиковата регулиране на сърцето.
† Променете симпатични механизми за регулиране.
‡ Намаляване на симпатиковата нервна система невротрансмитер - норадреналин в сърдечната тъкан.
Предизвиква. Намаляване на норадреналин синтез в неврони на симпатиковата нервна система (нормална него формира около 80% от посредник, съдържаща се в миокарда). Това е резултат от подтискане на тирозин хидроксилаза ензим активност и инхибиране на норадреналин поглъщане от нервните окончания.
‡ Намалете адренергични свойства на сърцето, т.е. тежестта ino-, хронологичен, Дром и bathmotropic норепинефрин и епинефрин.
† промени парасимпатиковите Механизмите за регулиране.
Ацетилхолин ‡ чрез т-холинергични рецептори предизвиква намаляване на сърдечната честота, инхибиране на образуването на сАМР и цГМФ активиране на образуване. цГМФ активира цГМФ-зависима киназа инхибиторна активност на волтаж-зависимите Са2 + -channels.
‡ Променете парасимпатиковата регулиране на механизмите за сърдечна недостатъчност е значително по-малко от симпатичен. Това е в резултат на по-високо съпротивление парасимпатиковите механизми на различни вредни фактори.
Последици от нарушения на симпатиковата и парасимпатиковата ефекти върху миокарда е да се намали степента на контрол и надеждност на регулацията на сърцето. Това води до спад в темповете и степента на мобилизиране на контрактилната функция на сърцето, особено при спешни състояния.