Киселинен дъжд (6)
Задълбочаването на човешките дейности в началото на миналия век е довело до значителен дисбаланс съществуващ в природата, което води до много проблеми, свързани с опазването на околната среда.
Сред много сериозни проблеми на най-голяма загриженост за околната среда план се увеличава замърсяването на въздуха басейна на примесите на Земята, които имат антропогенен произход. Атмосферния въздух е основната активност на средата на биосферата, включително хора. По предварителни данни, изпускани в атмосферата годишно стотици милиони тона оксиди на сяра, азот и други халогенирани съединения. Основните източници на замърсяване на въздуха са електроцентрали, които използват минерални горива, черни и цветната металургия, химическата и нефтохимическата промишленост, авиацията и автомобилната транспорт.
След в атмосферата, много замърсяване претърпяват химични или фотохимични реакции, включващи въздушни компоненти. Крайните продукти от химични реакции се отстраняват от атмосферното утаяване или да падне на земята повърхност с аерозоли. Получаване на повърхността на биологични обекти, конструкции и други неща, примеси и продукти от тяхното превръщане засили физикохимични процеси на разрушаване на органични материали, метали и неорганични материали.
Увреждане на дивата природа атмосферното замърсяване и продукти, производство на човешките дейности, е трудно да се прецени, но унищожаване на горите, замърсяването на водните басейни, разпространение на алергични заболявания, нарушение на биологичното равновесие в екосистеми, не на последно място, свързани с високите концентрации на агресивни вещества в атмосферата.
киселина дъжд
Терминът "киселинен дъжд" се отнася до всички видове метеорологични утаяване - дъжд, сняг, градушка, мъгла, дъжд и сняг, - рН на което е по-малко от средната рН на дъждовна вода (рН среда за дъждовна вода е равно на 5.6). Издаден през човешката дейност на серен диоксид (SO2) и азотни окиси (NOx) се трансформира в земята атмосфера подкиселяващи частици. ( "XX век :. През последните 10 години." 91) Частиците реагират с атмосферно вода, превръщайки го в кисели разтвори, което понижава рН на дъждовна вода. За първи път е въведен терминът "киселинен дъжд" през 1872 г. от английския изследовател Ангъс Смит. Вниманието му беше привлечено от викторианска смог в Манчестър. Въпреки, че учените в момента отхвърлят теорията за съществуването на киселинни дъждове, днес никой не се съмнява, че киселинните дъждове е една от причините за смъртта на живота във водните тела, гори, култури и растителност. Също киселинни дъждове разрушават сгради и културни обекти, тръбопроводи, оказват безполезни автомобили, намаляване на почвеното плодородие и може да доведе до изтичане на токсични метали в водоносни почви.
Вода конвенционален дъжд също представлява слабо кисел разтвор. Това се дължи на факта, че естествени вещества от атмосферата, като например въглероден диоксид (СО2) влизат в реакция с дъждовна вода. Това образува слаб карбонова киселина (СО2 + H3O -> H3CO3). ( "Химия и общество", American Chemical Society. Стр. 423-424) Макар че в идеалния случай рН на дъждовна вода е равно на 5.6-5.7, в реалния живот, киселинността (рН) на дъждовна вода в една област може да се различава от индекса на киселинността на дъждовна вода в други площи. Това зависи главно от състава на газове в атмосферата на определена област, като серни окиси и азотни окиси.
През 1883 г., шведски учен Сванте Арениус е влязъл в две лечение - киселина и основа. Той нарича киселини вещества, които, когато се разтварят във вода свободна форма положително заредени водородни йони (Н +). Той нарича площадки вещества, които, когато се разтварят във вода свободна форма отрицателно заредени йони хидроксид (ОН). Терминът рН се използва като индикатор на вода киселинност. "Терминът рН означава, на английски" експонента концентрацията на водородните йони. "(Chemistry и обществото. Стр. 428)
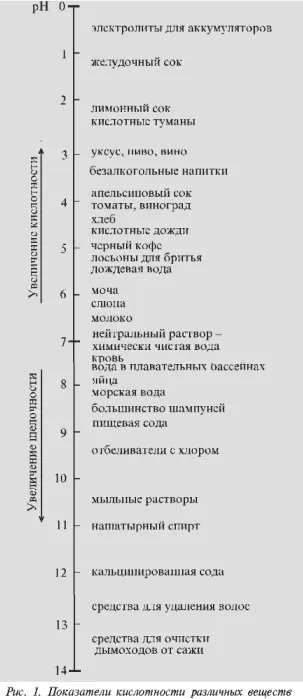
РН се измерва по скала от 0 до 14 са представени като водородни йони (Н +) и хидроксидни йони (ОН) във вода и водни разтвори. Когато концентрацията на водородните йони (Н +) във вода или в разтвор, равна на концентрацията на хидроксидни йони (ОН-) в същия разтвор, например разтвор е неутрален. рН неутрален разтвор равна на 7 (по скала от 0 до 14). Както е известно, когато разтваряне киселина във вода повишава концентрацията на свободни водородни йони (Н +). След това те се повиши киселинността на водата или, с други думи, рН на водата. По този начин, с увеличаване на концентрацията на водородните йони (Н +) концентрация намалява хидроксилни йони (ОН-). Тези разтвори, стойността на рН, при която намалява скалата е от 0 до 7 до 14, наречени основни.
Ако обърнем внимание на една характеристика на скалата на рН. Всяка следваща стъпка по скалата на рН показва намаление десетократно в концентрацията на водородните йони (Н +) (и следователно киселинността) в разтвора и увеличаване на концентрацията на хидроксиден йон (ОН-). Например, киселинността на вещество със стойност на рН 4 е десет пъти повече кисели субстанции на стойност рН 5, сто пъти по-високи от киселинността на вещество със стойност на рН 6 и стотици хиляди пъти по-високи от киселинността на вещество със стойност на рН 9.
Киселинен дъжд се произвежда от реакционната смес между вода и замърсители като серен диоксид (SO2) и различни азотни окиси (NOx). Тези вещества се отделят в атмосферата по шосе, като резултат от металургични заводи и електроцентрали, както и изгарянето на въглища и дърва. Реагира с атмосферно вода, те се превръщат в разтвори на киселини - сярна, серниста, азотна и азотна. След това, заедно със снега или дъжд, те падат на земята.
Киселинността на водния разтвор се определя от наличието в него на положителни йони водородни H + и се характеризира с концентрацията на тези йони в един литър разтвор С (Н +) (мол / л или г / л). Алкалността на водния разтвор от присъствието на хидроксилни йони, ОН и се характеризира с тяхната концентрация С (ОН -).
Изчисленията показват, че за водни разтвори на продукта от моларните концентрации на водородни йони и хидроксил - постоянна стойност, равна на
С (Н +) С (ОН -) = 10-14,
с други думи, киселинността и алкалността са взаимосвързани: увеличение на киселинност води до намаляване на алкалността, както и обратното.
P
От това следва, че условието за киселинни среди:
алкални среди:
На практика, степента на киселинност (или алкалност), изразени в по-удобно разтвор с рН, което е отрицателен логаритъм на моларната концентрация на водородни йони:
Например, ако концентрацията на разтвора на водородни йони е 5,10 мола / L, на киселина стойността на рН на разтвора = 5. Тази промяна в киселинност рН индикатор единица, съответстваща на промяна десетократно в концентрация водороден йон в разтвора. Така, концентрацията на водородните йони в среда с рН = 2 до 10, 100 и 1000 пъти по-висока, отколкото в среда с рН 3, 4 и 5, съответно.
В киселинни разтвори на рН 7, и по-голяма, толкова по-висока алкалност на разтвора.
киселинност диапазон е от рН = 0 (изключително висока киселинност) чрез рН 7 (неутрален) до рН = 14 (много висока алкалност).
Pure естествени, по-специално на дъждовна вода, вода в отсъствието на замърсители въпреки това има леко кисела реакция (рН = 5.6), тъй като лесно се разтваря въглероден двуокис с образуването на слабо карбонова киселина:
СО2 + Н 2О Н2 CO3.
За да се определи стойността киселина при използване на различни m рН, особено скъпи електронни устройства. Един прост начин да се определи естеството на средата е използването на индикатори - химикали оцветяване, което варира в зависимост от рН на средата. Най-често индикатор - фенолфталеин, метил портокал, лакмус, както и естествени багрила, червено зеле и касис.
Ефекти на киселинните дъждове.
През 70-те години. в реките и езерата на скандинавските страни започнаха да изчезват риба, сняг в планините, боядисани в сив цвят, листата от дърветата преждевременно осеяна земята. Много скоро едни и същи явления, наблюдавани в Съединените щати, Канада, Западна Европа. В Германия претърпял 30% и понякога 50% от гори. И всичко това се случва далеч от градовете и промишлени центрове-ТА. Оказа се, че причината за всички тези проблеми - киселинни дъждове.
Стойността на рН се променя в различни водоеми, но на необезпокояван природна среда план гама от тези промени е строго ограничен. Природни водите и почвите имат буферен капацитет, те са в състояние да неутрализират някои от киселината и околната среда ко-магазин. Въпреки това е очевидно, че капацитетът на буфер при пръчките не са неограничени.
На езера, засегнати от киселинен дъжд, нов живот могат да вдишват малки количества фосфатни торове; те помагат на планктон абсорбират нитрати, като по този начин намаляване на киселинността на водата. Използване на фосфат-евтино от вар освен фосфат има минимален ефект върху химията на водата.
Земята и растенията, разбира се, също страдат от киселинен дъжд Dei: намалена производителност на почвата, намалена доставка на пи tatelnyh вещества променят състава на почвата микроорганизми.
Огромно вреди, причинени киселинен дъжд гори. Изсушаване на гората, развива загине големи площи. Киселина повишава подвижността в почвата алуминий, който е токсичен за фините корени, и това води до потискане на листни-STI нестабилни клонове. Особено засегнати са иглолистни дървета, защото иглите се заменят по-рядко от листата, и затова се натрупва повече вреда, неправителствени агенти за същия период. Иглолистните дървета пожълтяват, те izrezhivayutsya корона, повредени плитки корени. Но промяна на цвета на листа, ако преждевременно се хвърли от правителствена-листата на дърветата, корона умре част е повредена кора. подновяване Natural крак с иглолистни и широколистни гори се случи.
Увеличаването увреждане киселина дъжд причина селското-правителствена култури: покриващ повреден растителна тъкан, променя метаболизъм в клетки, растения забавят растежа и развитието, намалява тяхната устойчивост на болести и паразит-там, добивите намаляват.
North Carolina State University, американски експерти изследват ефектите упражняваните от киселинни дъждове-ми на растенията по време на тяхното максимално чувствителност към факторите на околната среда. Под влияние на киселинните дъждове не-в косвено след опрашването кочан царевица formirova лосове-малко зърно, отколкото в поливните води. И колкото повече в дъждовна вода, съдържаща киселина, по-малките зърното се формира на кочан. Въпреки това, се оказа, че киселинните дъждове, за изминалата опрашването, без забележим ефект върху формирането на зърна.
проучвания степен проведени чувствителност към киселина дъжд Nym 18 видове култури и 11 вида декоративни растения в ранните стадии на растеж. Най-конюгиран podver-зловреден активност бяха доматените листа, соя, фасул, тютюн, патладжан, слънчоглед и памук. Най-малко податливи - зимна пшеница, царевица, марулята, люцерна и детелина.
Киселинен дъжд не само убиват диви животни, но също така и да унищожи паметници. Здрав, твърд мрамор, смес от калциев оксид (СаО и СО2), взаимодейства с разтвор на солна киселина-Ser и се превръща в гипс (SaSO4). Промяна температури, дъжд и вятър потоци разрушават мек материал. Истории кал паметници на Гърция и Рим, стоящи в продължение на хилядолетия, в годините на село-Lednev унищожени пред очите ни. Същата съдба заплашва Тадж Махал - шедьовър на индийския период архитектура Вели-кал Mughals в Лондон - Кулата на Лондон и Уестминстърското абатство. В ST. Павел, Рим слой Портланд варовик подкопана от 2.5 см. В Холандия, статуи на ST. Йоан стопят като близалки. Черно депозити изядени Роял Палас на площад Дам в Амстердам.
Повече от 100 хил. Ценни витражи, които красят църквите в палатката, Konterberi, Кьолн, Ерфурт, Прага, Берн, в други европейски градове могат да бъдат напълно загубени през следващите 15 до 20 години.
След изучаване на нови данни на киселинността на валежите в различни райони на Западна Европа, както и въздействието от тях на zda-ТА и съоръжения, персонал, Университета на Дъблин (Il-Land) установи, че най-катастрофалното положение е лос в центъра на Манчестър (Великобритания), където 20 месеца утаяване киселина се разтварят 120 г на 1 т2 от камък (Единични пясъчници, мрамор или варовик).
Градът пострада значително, въпреки че общата сума на валежите в наблюдавания период от време е имало изключително ниско. Очевидно е, но това е прекалено висока степен на киселинност.
За Manchester трябва Liphun (окръг Hampshire Veli-Великобритания) и Antwerpen (Белгия), в които всеки от вътрешен въздух камък загуби 100 г 1 m 2. Дори такъв известен zagryaz nennostyu-град атмосфера, Атина, Копенхаген и Amster- дами подложени киселина разграждане в много-Men-голямата степен.
Страдат от киселинен дъжд, и хора, които са принудени да консумират питейна вода, замърсени с токсични метали - живак, олово, кадмий и др
Запазване на природата от окисляването е необходимо. За тази Xia драстично да намали емисиите на серни и азотни оксиди, но главно серен диоксид, както е сярна киселина и нейните соли в 70-80% причина дъжд киселинност, капка-позиция на големи разстояния от индустриални площи на емисиите.
сняг система за контрол на замърсяването на капака се намира на място-RII България се извършва на 625 точки, проучва площ от 15 милиона. km2. Пробите са взети в присъствието на сулфатни йони, амониев нитрат, тежки метали, определени рН стойност.
Natural валежите са с различна киселинност, но средната рН = 5,6. Киселина утаяване с рН 1 2 Виж всички