Химическа организация клетка
Съставът включва около 70 клетки на химичните елементи от периодичната система DI Менделеев. В зависимост от това колко химически елементи, включени в веществата, които са жив организъм е прието да се разпределят на няколко групи от тях.
Една група (около 98% от теглото на клетки) форма четири светлинни елементи водород, кислород, въглерод, азот. Те са наречени макронутриенти. Това са основните компоненти на органични съединения.
Друга група се състои от елементи в клетката в по-малки количества. От тях, сяра и фосфор заедно с макроелементи са част от основните органични съединения - нуклеинови киселини, протеини, мазнини, въглехидрати, хормони, калий, натрий, магнезий, манган, желязо, хлор и изпълняват важни функции в клетката. Елементите, които се съдържат в клетката в много малки количества, се наричат микроелементи.
Полярността на молекулите и способността да образуват водородни връзки направи вода добър разтворител за голям брой неорганични и органични вещества. Такива вещества се наричат хидрофилни. В допълнение, вода осигурява приток на вещества в клетката, и изхвърляне на отпадъци от тях.
Водата има добра топлопроводимост и голям топлинен капацитет, позволявайки температурата да остане непроменена при различни температури на околната среда в клетъчната среда.
Повечето клетки неорганично вещество е под формата на соли - или дисоциират на йони, или в твърдо състояние. Сред първите са от голямо значение катиони K, Na, Ca, раздразнителност, които осигуряват живи организми. От концентрацията на сол в клетката зависи буферирани клетки. Буфериране - способността на клетките да се поддържа леко алкална реакция на съдържанието му на постоянно ниво в променяща се среда.
Органични съединения на средно 20 - 30% от клетъчната маса. Това са биологични полимери: протеини, нуклеинови киселини, въглехидрати и липиди и някои малки молекули - хормони, пигменти и т.н. АТР.
Протеини. Протеини между органични вещества заемат първо място, както по брой и значимост.
Протеините се състои от 20 различни аминокиселини. Тяхната обща формула
където R - радикал различна структура. В лявата част на молекулата е амино групата на Н2 N, който има свойства на основа; Точно - карбоксилна група СООН - киселина, характерен за всички органични киселини. Следователно, аминокиселини - амфотерно съединение и съвместяващи свойства на киселина и основа. Свързване молекули аминокиселинни образуват връзки между въглеродните киселина и основните азотни групи. Тези връзки се наричат ковалентна, в този случай - чрез пептидни връзки:
Н2 N # 9472; HC # 9472; C + N # 9472; HC # 9472; СООН → Н2 N # 9472; HC # 9472; C # 9472; N # 9472; HC # 9472; COOH + Н 2О
Съединение, състояща се от 20 или повече аминокиселинни остатъци се нарича полипептид. Аминокиселинната последователност на полипептидната верига, наречена първичната структура на протеина.
Въпреки това, молекулата на протеин, както е верига от аминокиселини, последователно свързани чрез пептидни връзки, не е в състояние да изпълняват специфични функции. Това изисква по-висока структурна организация. Чрез водородни връзки между остатъци на карбоксилните и аминогрупите на различна амино киселина протеинова молекула е под формата на спирала. Тази вторична структура на протеина. Но в повечето случаи само една молекула, която има третична структура, може да изпълнява биологична роля. Третична структура се образува чрез взаимодействие на радикали, по-специално радикали цистеинови аминокиселини, които съдържат сяра. серни атоми на две аминокиселини, разположени на известно разстояние един от друг, са свързани, образувайки така наречената дисулфид или S - S-връзка. Полагане полипептидни спирали в глобули (топки) и се нарича третичната структура на протеина (Фигура 1).
Някои функции на организма се извършват с участието на протеини с още по-високи нива на организацията - кватернерния структура. Например, хемоглобин, инсулин.
Загубата на протеин молекула, наречена денатурация на структурна организация (от латинската denaturare -. За да лиши физическите свойства).
Ренатуриране - този имот на протеини напълно се възстанови загубената структура, ако не се промени в околната среда е довело до унищожаването на първичната структура.
Един от най-важните функции на протеини в клетката - строителство. uchuvstvuyut протеини в образуването на клетъчните мембрани в клетъчните органели и извънклетъчни структури.
Изключително важно е каталитична функция на протеини. Всички биологични катализатори - fermenty- вещество на протеин природата. Те се ускори химичните реакции в клетката, в размер на десетки и стотици хиляди пъти. Ензимът катализира само една реакция, т.е. той uzkospetsifichen.
Функцията двигател на тялото е предвиден контрактилните протеини. Тези протеини uchuvstvuyut във всички видове движения, които са в състояние на клетките и организмите: трептенето на ресничките и камшичета побой в най-простата, свиването на мускулите при животните.
Транспортни протеини функция се състои в присъединяването химични елементи (например, кислород) или биологично активни вещества (хормони), и прехвърлянето им в различни тъкани и органи на тялото.
Когато тялото чужди - протеини или микроорганизми в белите кръвни клетки - левкоцити - образувани специален протеин - антитяло. Те се свързват и неутрализират вещества, чужди на организма. Тази защитна функция се експресира протеини.
Протеините са също един от енергийни източници на клетката, т.е. извършване на енергия функция. При пълно милионграма протеин разцепване се разпределя 17,6 кДж на енергия.
Въглехидрати. Въглехидрати, захариди или - органични вещества с обща формула Сп (Н 2О) м.
Въглехидратите се разделят на прости и сложни. Простите въглехидрати са монозахариди. В зависимост от броя на въглеродните атоми в молекулата се наричат монозахариди триози, тетрози, пентози (рибоза и деоксирибоза), хексози (глюкоза, галактоза).
Комплексните въглехидрати, образовани много монозахариди са наречени полизахариди.
Въглехидратите имат две основни функции: строителство (хитинови) и енергия (нишесте в растенията и гликоген при животните - на енергийния резерв). Въглехидрати - основният източник на енергия в клетката. По време на окисление 1 грам въглехидрати 17,6 кДж на енергия се освобождава.
Липиди. Липиди, или мазнини, са съединения с високи молекулни киселини киселини и тривалентен алкохол глицерол. Мазнини не се разтварят във вода - те са хидрофобни. В клетки винаги има други мазнини вещества - липиди.
Липидите и липиди изпълняват конструкция и функция. те са част от клетъчните мембрани. Поради лошо топлинна грес на проводимостта може да изпълнява функцията на топлинен изолатор. Получаване на някои липиди предхожда синтеза на някои хормони. Следователно, тези вещества са присъщи на функцията на регулиране на метаболитни процеси.
Нуклеинови киселини. Nucleic (лат ядро -. Nucleus) киселина - комплекс орган-еска съединение. Те са съставени от въглерод, водород, кисел, азот и фосфор.
Има два вида на нуклеиновите киселини - РНК и ДНК. Те могат да бъдат както в ядрото и цитоплазмата и нейните органели.
ДНК - дезоксирибонуклеинова киселина. Това е биологична полимер, състоящ се от две полинуклеотидни вериги сдвоени-TION един с друг. Мономерите - нуклеотиди представляващи kazh-удар на ДНК веригите, са комплексни органични съединения. ДНК се състои от четири азотни основи: производни на пурини - аденин (А) и гуанин (G) и пиримидини производни - цитозин (С) и тимин (Т), пентахидритни пентоза захар - деоксирибоза, и остатък на фосфорна киселина (Фигура 2 ).
Нуклеотидите на всяка верига са свързани заедно чрез ковалентни връзки: един деоксирибоза нуклеотиден остатък свързан с последващо нуклеотидна фосфорна киселина. Двете вериги са комбинирани в единична молекула водородни връзки, възникващи между азотни основи, които образуват нуклеотидите, които образуват различни схеми. Пространствена Con-контур азотна база е различен и броят на Con-връзки между различни азотни бази неравномерно. След-Следствие, те могат да бъдат свързани само по двойки азотни оси съображения аденин (А), верига от пол и нуклеотидната винаги е свързан, но две водородни връзки с тимин (Т), друга верига, и гуанин (G) - три водородни връзки с азотна база -niem цитозин (с) срещу полинуклеотид TSE-бъбреците. Тази способност за селективно съединение нуклео-tidov, в която са оформени двойка А-Т и G-C, наречен допълване (виж фиг. 15). Ако известна базова последователност на една верига (например, TJ T-T-A-T), след това с принципа на комплементарност (допълване) ще бъдат известни и обратна базовата последователност (A-G-T-A-D) ,
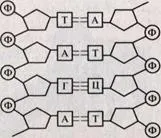
Фигура 2. Парцел на ДНК молекулата. Допълнителните нуклеотиди утежняват различни вериги.
нуклеотидни вериги образуват pravozakruchennye насипно спин-Рали на 10 бази във всяка намотка. Последователност Съед-neniya една нуклеотидна верига обратна на Дрю-GOY, т.е. верига, включваща една ДНК молекула raznonaprav-малко на брой или антипаралелен: последователност междунуклеотидни връзки в двете вериги, в посоката, в противоположни посоки: 5 '-3' и 3 '-5. Захар-фосфатни групи от нуклеотиди са къмпинг навън и азотна база-ТА - вътре. Верига усукани един спрямо друг и около общата ос, за да образуват двойно-ти спирала. Тази структура на молекула MO-поддържа предимно от водородни връзки (фиг. 3).
За първи ДНК вторична структура, въведен за първи път американски Bio-влезете Dzh.Uotson английски физик и Крик.

Фиг.3 структурата на двойната спирала на ДНК: А - равнинна модел, дебела линия означава захар-фосфатен гръбнак; Б - модел обем
Когато се присъедини ДНК със специфични протеини (хистони) степен спирала молекули увеличава - шум-кае superspiralDNK чиято дебелина се увеличава значително, а дължината се намалява (фигура 4). Уплътняване единица служи нуклеозома ДНК молекула, която се основава на 8 молекули на хистони, 2 от всеки тип (Н2А, Н2В, и Н4 NS). Повърхностите на тези протеинови молекули носят положителни заряди, и адресиране образуват скелет, около която обрат може да бъде отрицателно отрицателно заредена ДНК молекула. Всяка нуклеозома WMOs-ди от 146 до 200 двойки nukleoti-редове. Хистон пети вид - N1 - се свързва с ДНК сайтове, един нуклеозома свързване ти друга. Тази ДНК се нарича права или Comm-нителна - линкер. Nucleo
сома разположени по протежение на ДНК на определено разстояние, неравномерно в зависимост от вида на клетката - от 20 до 50 нм. Това образува структура, подобна на зърната, при което всяко зърно - нуклеозома.
Фиг. 4 Схема на ДНК супер-спирала.

Нуклеозоми и линкер ДНК в своя опаковани в фибрили, които образуват бримки върху хромозомата. По-високите нива спирала може значително да намали дължината на ДНК молекулата. Достатъчно е да се каже, че общата дължина п-ДНК молекули, съдържащи човешките хромозоми е 1.74 m, те се намират в клетките с диаметър 5 микрона -7. Тази молекула, внимателно "опаковани" протеини могат да бъдат по-са наблюдавани в светлинен микроскоп по време на клетъчното делене и оцветени продълговата телешки -hromosomy.
РНК - рибонуклеинова киселина. РНК, както и ДНК е полимер на който мономерите са NUS-leotidy близо до нуклеотидите ДНК. Азотни основи три нуклеотиди същата като тази, включена в ДНК (аденин, гуа-Ning, цитозин), четвъртата земята - урацил (U) е налице само в молекулата на РНК (вместо тимин). Нуклеотидите Otley РНК-ДНК нуклеотиди не са подобни на структурата и техните съставни въглехидрати: те включват други пентоза - рибоза (вместо desault-ksiribozy). RNKnukleotidy на веригата свързан чрез образуване на ковалентни връзки между рибозата на нуклео-употреба и фосфорна киселина остатък друга.
Според разграничи двойно верижна структура и едноверижна РНК. Двойна верижна РНК генетични пазители на информационно-ТА на редица вируси, т.е. изпълняват функциите си по хромозоми. Единична верига иРНК носят информация за последователността на аминокиселини в протеини (т.е., на структурата на протеини) в хромозома от тяхното местоположение синтез и участват в синтеза на протеини.
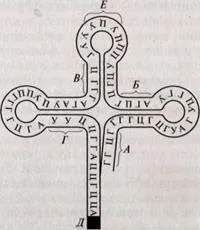
Фиг.5 схема структура на тРНК: А, В, С, Т - части на краката допълване, един мол от съединението в kuls РНК; D - раздел (активно място) с амино съединение; Е - раздел (активен център) Comp съединение с елементарен молекула и РНК (антикодон)
Съществуват няколко вида на едноверижна РНК. Техните имена са дължими за изпълнение на функцията или мястото в клетката. Повечето от цитоплазмена РНК (80-90%) Състав желаете да настроите-рибозомна РНК (рРНК) информация, съдържаща се в рибозомите. Mole Кула рРНА сравнително малка и се състои от 3 - 5 хиляди нуклеотиди .. Друг вид на РНК - информация (иРНК), прехвърляне на информацията за рибозоми schaya последователност aminokis-много в протеини, които трябва да бъдат синтезирани. Големината на РНК зависима ДНК част от дължината на която те са синтезирани. И РНК молекули могат да бъдат съставени от 300 - 30 000 нуклеотида. Тран-Спортна РНК (тРНК) включва 76 - 85 нуклеотиди (фиг.) И се изпълнява няколко функции. Те достави аминокиселина в протеин синтез място и извършва точни ориентация аминокиселини (въз основа на комплементарността) към рибозома. тРНК има две активни места, единият от които е свързан с разделен определена аминокиселина, а другият, състояща се от три реда nukleoti служи за връзка с комплементарна РНК молекула. Тази област се нарича антикодонните.