Дефекти в кристалната структура
В реално кристали не е напълно правилно подреждане на атомите в целия обем на кристала. Винаги има нарушения на правилното подреждане на атомите. Тези заболявания се наричат дефекти в кристалната структура (BCS). Те са разделени на: 1), точка; 2) линеен; 3) повърхност.
Размерите на точка дефект в близост до interatomic разстояние. Към точка дефекти са свободните работни места и заставки. Свободни места, наречени решетъчни сайтове кристал, където няма атома. Наречен интерстициален атом разположен между кристалната решетка сайтове (фиг. 1.4).

Фиг. 1.4. Point дефекти:
и - вакантно; б - изместване диаграма места в кристалната;
в - интерстициален атом
Позиция често образува при прехода от атоми от мястото на решетка и по-малко на повърхността в резултат на преминаването им в пролуката. Точка дефекти поради топлинна движение на атомите. Във всеки температура винаги има атомите, чиито кинетична енергия е по-голяма от средната стойност за дадена температура. Тези атоми могат да преодолеят потенциалната бариера, създадена от съседните атоми, и да излязат от вашия сайт на повърхността или в междинното пространство. В непосредствена опаковани решетки работата е много повече от заставки. Работа могат лесно да бъдат преместени на кристала. Колкото по-висока е температурата, толкова повече броят на свободните работни места и по-малко време за пребиваване на един възел на решетката. При температура, близка до точката на топене (т.т.), броя на свободните места може да достигне
1% в сравнение с броя на атомите в кристала. Точка дефекти предизвика локално нарушаване на кристалната решетка [2].
Основният вид на линеен BAC са размествания. Те са ръб и винт.
Умствени nadrezhem перфектно кристал в междина, образувана вложка допълнително атомен половин равнина (допълнителните). Такава "клин" нарушава кристалната решетка. Това изкривяване е от особено значение в края на допълнително. Районът около кристалните несъвършенствата на допълнително ръб се нарича край дислокация ТА (Фиг. 1.5).
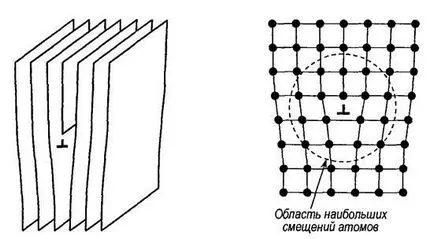
Фиг. 1.5. Един дислокация ръб (а) и подредбата на атомите
в областта на дислокацията (б)
Около решетка дислокация се деформира еластично. Ако допълнителните в горната част на кристала, дислокацията се нарича положителен и представляват. ако дъното - отрицателен и да кажа. В напречното сечение на кристала в нарушение правилното разположение на атоми, причинени от разместване, обхваща няколко решетка периоди и в посока, перпендикулярна на напречното сечение, за много хиляди interatomic разстояния.
Разместване чрез прилагане на малка сила на срязване могат лесно да бъдат преместени. В резултат на допълнително малка денивелация ще отиде в цялата равнина на кристала, и неговата функция ще бъде да се извършва в съседния самолета. Разстройството е от същия знак отблъскват и привличат различни признаци. Размествания, възникващи в процеса на кристализация, пластична деформация и т.н. Те имат голямо влияние върху металните свойства [2].
Разместване плътност е общо дължина Sl размествания на единица обем V:
В темперирани метали г = 10 юни ... 10 8 cm -2. След голяма студена пластична деформация г = 10 ноември ... 10 12 cm -2. Опитите да се увеличи плътността на изкълчвания над 10 четвър ... 10 12 cm -2 води до пукнатини и унищожаване на метала.
Особено голямо влияние върху силата на метали размествания. Когато значително увеличение на дислокация плътност и намаляване на силата на тяхната мобилност увеличава няколко пъти в сравнение с темперирани метали [3].
По повърхността BCS включват: 1) границите на зърното; 2) subzoren граница.
Поликристалната съдържа голям брой малки зърна. Границите на зърната са преход регион, в който кристалната решетка на зърното с определена ориентация в пространството гладко в мрежата с различна ориентация зърно (фиг. 1.6а).
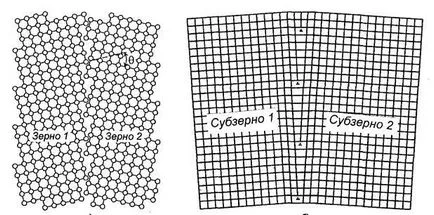
Фиг. 1.6. Повърхностни дефекти:
и - високо ъглови граници (Q - ъгъл misorientation);
б - граници нисък ъгъл
Границата между зърната е с ширина от 1 ... 5 нанометра. На границата нарушение правилното подреждане на атомите. граници висока ъгъл на зърно се нарича, защото кристалографски посоки за да се образуват ъгли на съседните зърна (р), достигайки десетки градуса.
Всеки метал зърно включва отделни блокове или subzoren. Subgrain е част от кристал спрямо правилната структура, в която не дислокация. граници нисък ъгъл между subzornami представлява размествания стена (фиг. 1.6, б).
Повърхностни дефекти засягат механични и физически свойства на метали. Фини зърното, по-висока стрес добив, вискозитет и по-малко крехък риска от фрактура.
Сплави - материали, съдържащи най-малко два елемента. Сплавите се получават чрез легиране, синтероване, плазма пръскане, електролитни и други подобни Те имат по-сложна структура. В слава елементи могат да взаимодействат различно с всеки друг, за да образуват различни фази. Това се нарича хомогенна фаза отделна част от сплав със същия състав, структура и свойства.
Следващите етапи могат да бъдат образувани в сплавите съгласно физико-химически взаимодействието на 1) течни разтвори; 2) твърди разтвори; 3) химични съединения; 4) междинните фази, които имат характеристики като твърди разтвори и химични съединения.
Твърдите разтвори са наречени фази в който атомите на един елемент, разположен вътре в кристалната решетка на друг елемент, без да променя вида на кристалната решетка. Елемент решетка, която се задържа в твърд разтвор се казва разтворител. а другият - разтворим.
Разграничаване заместване твърд разтвор (фиг. 1.7, а) и въвеждане (1.7 фунта). При образуването на заместители твърди разтвори на разтварят елемент атоми на мястото на някои от атомите разтворител при решетъчни сайтове на кристалната решетка.
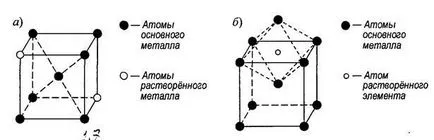
Фиг. 1.7. Схема разтвор твърдо вещество заместване (а) и въвеждането на (б)
Атомите на разтворени елементи могат да бъдат заместени за всеки от възлите на решетка разтворител. Стопилката заместване решения, образувани от елементите, атомната радиусите на които се различават с не повече от 15%.
Разтворимост елементи в твърд разтвор, намалява с увеличаване на разликата в атомната радиуса на легиращи елементи и тяхното валентността. При образуването на заместители твърди разтвори е възможно и неограничен разтворимост. Това се случва, когато за всяко съотношение на легиращи елементи всички различни атоми са разположени на възлите с обща пространствена решетка (например мед със злато, мед, никел, силиций, германий).
Много заместители твърди разтвори могат да бъдат подредени състояние, т.е. разтворителя и разтворените атоми заемат определен елемент от местата на кристалната решетка. Такива решения се наричат поръча или "надстройки".
В твърди разтвори, интерстициални атома разтворено вещество елемент, разположен в междините, т.е. в порите. Такива разтвори образуват преходен метал с неметали с малък атомен радиус (Н, N, С, В).
Въвеждането на твърди разтвори винаги имат ограничена разтворимост. Ако разтворителят е НСР или FCC решетка, разтворимостта е по-голям, тъй като тези решетки порите радиус = 0,41R. където R - радиус на атома разтворители. В Ск решетка на разтворимост чрез въвеждане на малки, тъй като размерът на порите не надвишава 0,29R.
Образуването на твърди разтвори води до нарушаване на кристалната решетка и изкривяването е по-голяма за въвеждане на твърди разтвори. Изкривяването на кристалната решетка прави сплавта по-трайни в сравнение с чистите метали, сплави, но поддържа достатъчно висока пластичност. Твърдите разтвори са в основата на повечето търговски сплави [3].
Химични съединения, открити в метални сплави, са много различни. Те се различават от твърди разтвори на следните характеристики: 1) имат строго определена структура и химична формула Am Вп. където А и В - съответните елементи, п и м - прости числа; 2) кристалната решетка на съединение различно от компонентите на решетки, които са съединение; 3) свойствата на химичните съединения се различават от свойствата на елементите на състава; 4) имат постоянна точка на топене; 5) получаване на химично съединение се придружава от значително топлинно въздействие.
За разлика от твърдите разтвор химични съединения обикновено образувани между елементите, които имат голяма разлика в атомната структура и кристалните решетки.
Най-добрите механични свойства са тези сплави, които се основават на твърди разтвори с препокриваща в него фино разделени твърди частици от химически съединения, или междинни фази. Колкото повече от тези частици в сплавта, толкова по-висока твърдост и якост но по-ниска пластичност и якост.
метален преход от течност към твърдо вещество се нарича кристализация. По време на кристализация на системата продължава към термодинамично по-стабилна държава с по-ниска свободна енергия. Промяната на свободна енергия на твърди и течни Fzh FTV метал зависи от температурата (фиг. 2.1).
Горният температура T0 по-стабилна разтопен метал. Тя е с по-ниска енергия без доставка, а под тази температура е по-устойчив твърд метал. T0 на температурата се нарича температура на равновесие кристализация. При тази температура могат да съществуват едновременно течната и твърдата фаза.
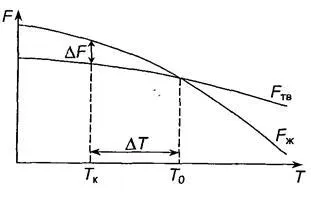
Фиг. 2.1. Промяната на свободна енергия F на течността и твърдото вещество
с температура на метала
Процесът на кристализация при тази температура още не е започнал. Това може да се случи само на метал след преохлаждане долу T0. Разликата между T0 на температурите и ТС се нарича степента на преохлаждане
Охлаждане криви характеризиращи процеса на кристализация на чисти метали при охлаждане с различни скорости са показани на Фиг. 2.2.
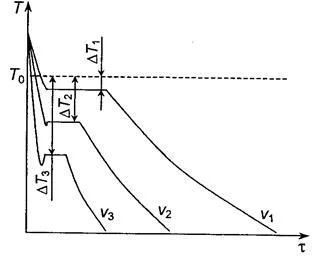
Фиг. 2.2. криви метал охлаждане
В много бавно охлаждане DT свръхохлаждане степен е малък и процеса на кристализация се извършва при температура, близка до равновесие T0 на. С увеличаване на скоростта на охлаждане увеличава свръхохлаждане степен. Когато втвърдяване много чист метали свръхохлаждане степен може да бъде голям, но за търговски чист не надвишава 10 ... 30 ° С
Когато температурата на кристализация се наблюдава хоризонтална платформа (капка стоп температура). Образованието се дължи на пускането му латентна топлина на кристализация.
Процесът на кристализация започва с образуването на течната фаза в кристалните семената, които са кристализационни центрове. След ръста на зародиш.
Най-често, образувана по време на кристализация разклонена (дървовидна) кристали, наречени дендрити. При образуването на кристали е тяхното развитие в посока, перпендикулярна на равнините на максимална плътност опаковане на атомите. Първо формира дълги клонове, осите на които се наричат първи ред. Едновременно с разширяването на първата ос около перпендикулярно на тях започне да расте два пъти ос. На осите на втория ред нараства тройно ос и т.н. Последното, което е кристализацията в областите между дендрита (фиг. 2.3).
Дендрити нарасне до толкова дълго, колкото не се свържете един с друг. След това попълнете mezhosnye пространство. Дендрити се превръщат в неправилна форма кристали, които се наричат кристалити или зърна.
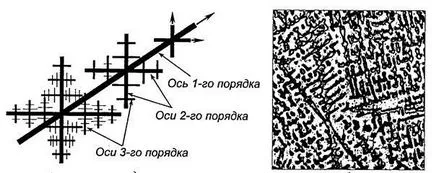
Фиг. 2.3. Схема dentdrita структура (а) и образуване на дендритни структура на тънка част (б)
Кристализацията се характеризира с два параметъра: CC - брой на зародишни центрове, които са възникнали в единица обем от течен метал за единица време; CP - темп на растеж, т.е., пътят пресича от нарастващата лицето на кристала за единица време.
Ембрионите могат да бъдат образувани като течност в определени количества, както и твърди чужди частици, присъстващи в течния метал.
Първият метод за формиране на зародишните центрове се нарича спонтанно. а вторият - nonspontaneous.
В течно състояние, атома движат произволно поради топлинна движение. Но има малки течност групи от атоми с такава конструкция, като в кристалната решетка. Тези групи са нестабилни - те се разтварят и се появяват отново. Когато след преохлаждане най-голямата от тях стават устойчиви и в състояние да расте. Тези категории са зародишните центрове, когато спонтанно кристализация. Но спонтанно генериране на кристали в течния метал е трудно.
Повечето зародишни центрове са формирани на твърдите чужди частици, присъстващи в течния метал.
Размерът на зърното по време на втвърдяване се определя от съотношението на получените ембриони и тяхната скорост на растеж. Колкото по-голям и по-малък CP CC, по-малките кристали. И двата параметри са свързани с движението на атоми и следователно зависи от температурата.
При ниски степени на преохлаждане брой зародишни центрове не е достатъчно. В груби структура е образувана от втвърдяване. С висока степен на Недогряване на водата брой зародишни центрове расте по-интензивно в сравнение с темпа на растеж. Ето защо, се получават по-малки кристали. Следователно, по-голяма от скоростта на охлаждане по време на кристализация, на фини се получава зърно. За малки зърна в разтопения метал често се прилага специален примеси. Този процес се нарича модификация [1].