Амини (Chemical клас 10)
Какво е амини
В днешния урок ние ще се запознаят със съединения като амини. Нека да разгледаме какви са тези връзки и това, което те представляват.
Амини наричат този клас от съединения, която е органично производно на амоняк, при което водородните атоми са заместени с органични групи. В този клас съединения, един или повече водородни атома могат да бъдат заместени с въглеводородни радикали.
Отличителната черта на тези съединения е наличието на такъв остатък като R-N<, где R – соответствует органической группе.
Амини са разделени в различни групи, класификацията на които зависи от структурата на знака, който се приема за своя база.
Според броя на заместени водородните атоми амини разделят на първичен, вторичен и третичен. Първичната включват тези, в които беше заменен само един водороден атом, съответно, в средното от трите атоми са заместени с два, и по-третичен заместен всичките три атома от трите налични.
Ако амини разгледани от естеството на органични групи, те могат да бъдат разделени на ограничаване, ненаситена и ароматна:
Ако разгледаме броя на амини на NH2-групи в молекулата, те могат да бъдат разделени на моноамини, диамини, триамини и т.н.
Номенклатура на амини
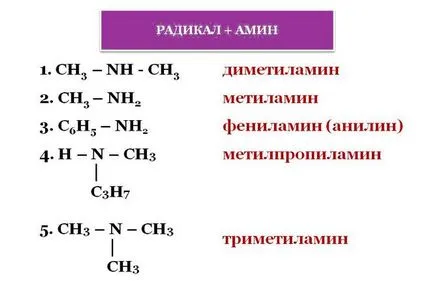
По този начин, към имената на органични групи, които са свързани с азота, доставени на думата "Амин", и да ги по азбучен ред.
Също така в получаването на заглавието, правилата позволяват база въглеводород, който може да се разглежда като заместител на амино групата. Тук позицията на амините да бъдат определени чрез цифров индекс.
Нека да видим как ще изглежда в протокола:
Тя изглежда като 3-аминопентан. Той цифрови кодове, които са разположени в горната показват реда на номерирането на атомите В. В някои случаи, някои амини опростени имена консервирани:
S6N5NH2 - анилин, все пак, ако следвате правилата на номенклатурата, тя се нарича -фениламин.
Също така по химия често използват утвърдени имена, които нарушават правилното име. Например:
N2NSN2SN2ON - едноетаноламин, въпреки че е коректно да се нарича 2-аминоетанол;
(ONSN2SN2) 2NH - диетаноламин, и ако използвате правилното име, тя ще звучи като:
Физичните свойства на амините
А сега нека да погледнем на физичните свойства на амини. Първите представители на редица амини са метиламин CH3NH2, диметиламин (CH3) 2NH, триметиламин (CH3) 3N етиламин и C2H5NH2. Това целия диапазон на амини са газове, които имат миризма на амоняк.
Средните отношение на тази серия, чрез увеличаване на броя на атоми в R, са трансформирани в течност. По-висока амини с увеличаване R верига дължина до 10 С-атома и кристализира в твърди вещества.
Също така, имайте предвид, че по-висока амин миризма е практически отсъства.
Както вече каза, че първичен амин има остър миризма на амоняк и лесно разтворим във вода. За по-сложни амини включват течност, която има мирис на риба.
Но по-високи амини са твърди вещества, които не се разтварят във вода и мирис, те имат малко. Разтворимост амини се намалява с увеличаване на дължината на веригата и нарастващи количества от органични групи. Това означава, че колкото по-високо молекулно тегло, по-ниската си разтворимост във вода.
Химичните свойства на амини
И сега до разглеждане на химичните свойства на амини:
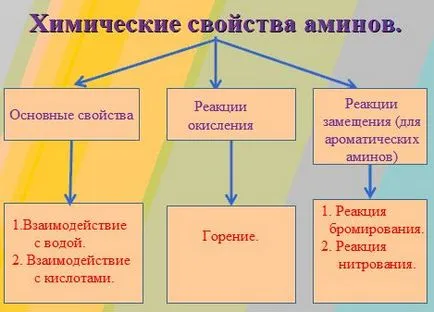
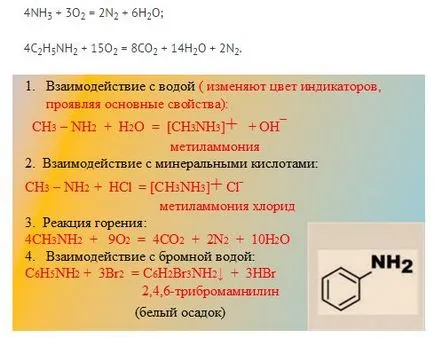
Обикновено, общите свойства на органични съединения е тяхната способност да горят. При сравняване на способността на изгаряне на амоняк с амини, първата изгарянето, но е трудно да се запалят. Но амини са склонни да бъдат лесно запалване и изгаряне на пламъците е най-често безцветен.
Намирането на амини в природата
Аминосъединения широко разпространени както в растителни и животинското царство, и са такива биологично активни вещества като витамини, хормони, метаболитни междинни продукти.
Амини срещат в природата, като продукти на разлагане, тъй като те се формират по време на разпадането на живите организми. продукти на разпадане протеин дават миризмата на херинга солев разтвор. Тази миризма показва присъствието на амини. В фантастика можете да многократно се сблъскват с такива фрази като "труп отрови" - това също е свързано с присъствието на амини.
Поради това нисш амин миризма често се бърка с амоняк. Но френски химик Шарл Vyurts през 1849 г. обръща внимание на разликата между амини и амоняк. Оказва се, че единствената разлика е, че амините са способни на изгарянето на въздуха и по този начин образуват въглероден диоксид.
Използването на амини
Сега, нека да разберете къде се използват амини? Изглежда, амини са широко използвани в производството на лекарствени вещества, производство на различни багрила, взривни вещества, както и продукти, използвани в органичния синтез.
вредни въздействия
Но също така имайте предвид, че амини - са вещества, които са доста токсични. Те представляват опасност при вдишване на изпарения, както и при контакт с кожата. А амини, такива като, например, анилин, има способността да прониква през кожата в кръвния поток и могат да нарушат функцията на хемоглобин, и по този начин да доведат до смърт.
След контакт с амини в кръвта на симптоми като задух, сини устните, носа и пръстите. Също така, в случай на отравяне се наблюдава учестено дишане и сърцебиене. А в някои случаи може да достигне до загуба на съзнание.
В случай на отравяне или амин излагане на излагане на кожата, е необходимо възможно най-бързо да се почисти засегнатата част на кожата с алкохол и вълна. Но това трябва да се прави много внимателно, опитвайки се да не се увеличава засегнатата кожа. В случай на отравяне изпарения на амини, трябва да бъде незабавно на пострадалия да осигури достъп до свеж въздух и се свържете с лекар.
Ако отравяне алифатни амини могат да се появят чернодробна дисфункция, увреждане на нервите и съдовата пропускливост.
Вдишване ароматни амини могат да причинят депресия на централната нервна система, както и рак на пикочния мехур причина.
Казус
Нека да похарчите малко опит. За тази цел ние се и се изсипва в епруветка 0,5 мл анилин. Сега вземете и съдържанието се разклаща.
Q: Каква реакция гледаш?
Сега нека в същата тръба и се добавя солна киселина, за да се наблюдава пълно разтваряне на анилин във вода.
1. Защо смятате, че е налице прекратяване на анилин, след като се добавя солна киселина?
2. Запишете тази реакция под формата на уравнения.
3. Опитайте се да се изчисли масата на вещество, което се образува.
4. Решаване на тази задача.
Отговорете на въпросите:
1. Какво известни класове органични съединения.
2. Какви са азотсъдържащи съединения са известни ви? Име тях и напишете своите формули.
3. Как да използвате амини в предприятия влияят на околната среда?
4. Каква е разликата между амоняк и амини?
5. Име подобни свойства на амоняк и амини.