степента на дисоциация
"Поведението на водни разтвори на електролити в химични реакции, е до голяма степен зависи от това колко пълен те се дисоциират на йони. За да се определи количествено параметрите на дисоциация са важни, тъй като степента и константата на дисоциация.
Степента на дисоциация и - съотношението на броя на молекулите на разпада на йони, с първоначалния брой на разтворените молекули:
Степента на дисоциация понякога се изразява като процент:
Степента на дисоциация на електролит зависи от концентрацията на разтвора: концентрация намалява с намаляване на взаимодействие на йони в разтвор, което води до образуване на молекули, следователно степента на дисоциация се увеличава. Според степента на дисоциация на електролитите могат да бъдат разделени в силен, среден и слаб. Силни електролити имат> 30%; слаб - и <3%; средние - а в пределах от 3 до 30%.
Като силни електролити във водни разтвори са почти всички соли, повечето неорганични киселини (HNO3. HCl, H 2SO 4. НСЮ4 и др.) И хидроксиди на алкални и алкалоземни метали. Средните електролити са H2 SO3. Н 3РО 4 и сътр., Съединения като Н2 S, Cu (OH) 2 и др. Са слаби електролити.
Участък от слаби електролити, средни и силни е конвенционална, тъй като степента на дисоциация в зависимост от естеството на електролита и разтворител, концентрацията и температурата на разтвора. Водни разтвори на различни соли, киселини и основи на същата концентрация се разпадат в йони в различна степен. Степента на дисоциация значително повлияни от присъствието на други йони в разтвор. По този начин, ако има разтвор CuCl2. системата за баланс
"Процесът е обратното на електролитна дисоциация molizatsiya - Реюнион йони на противоположни знаци в неутрална молекула. Ако има динамично, мобилно състояние на дисоциация между процеси и molizatsii, а след това са намерени от уравнението:
Ако имаме. т.е. в слаби разтвори на почти всички молекули са неотделими. С увеличаване на концентрацията на разтвора се понижава. В силно концентрирани разтвори
Има много необичайно и електролити. Например, електролита е стъкло, което е силно преохлажда течност с вискозитет огромна. При нагряване на стъклото омекотява и вискозитетът му е силно намалена. Натриев присъства в стъклото Na + йони стават значително мобилност и става възможно да тече електрически ток, въпреки че при обикновени температури стъклото е добър изолатор.
А ясно доказателство за това е опитът, веригата е показано на фигура 2.
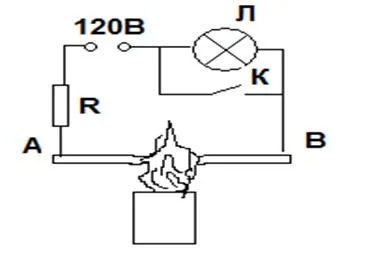
Демонстрация на стъкло проводимост при нагряване