Различните етери комплекс, каква е разликата
В органичната химия, има два основни класа на естери: прости и сложни. Тези химични съединения, образувани чрез хидролиза (отцепване водни молекули). Етери (наричани също Eterija) се получава чрез хидролиза на съответните алкохоли и естери от тях (естери) - съответния алкохол и киселина.
Въпреки подобен името, етери и естери са две напълно различен клас съединения. Те се приготвят по различни начини. Те имат различни химични свойства. Те се различават, и структурната формула. Обща има някои физични свойства на най-известните представители.
Физични свойства на Etheria и Естер
Етери - ниска разтворимост във вода, течности с ниска точка на кипене са запалими. При стайна температура, етери - приятно миришещи безцветна течност.
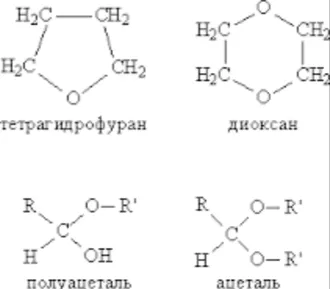
Естери с ниско молекулно тегло - лесно летливи безцветна течност приятна миризма често плодове или цветя. С увеличаване верига карбоксилна ацилна група и остатъкът алкохол, други свойства стават. Такива естери вещества. Тяхната температура на топене зависи от дължината на радикали въглеродни и молекулна структура.
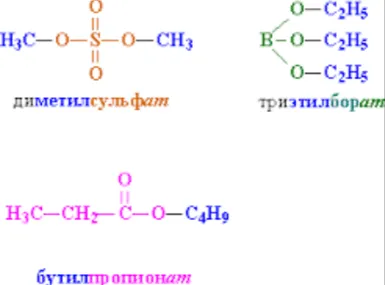
Структура етери и естери
Двете съединения имат етер връзка (-О-), но в естерите е част от комплекс функционална група (-СОО), където първият атом, свързан с кислород въглероден атом с единична връзка (-О-) и втората двойно ( = О).
Тя може да бъде схематично представена както следва:
- Етер: R-О-R1
- Естер: R-COO-R1
В зависимост от радикалите R и R1, етери са разпределени в:
- Симетричните естери - такава, в която алкиловите радикали са еднакви, например dipropilovyyefir, диетилов етер, дибутилов етер, и т.н.
- Асиметрични етери или смесени - с различни радикали като етил пропил етер, метил фенил етер и др butilizopropilovy
Естери се разделят на:
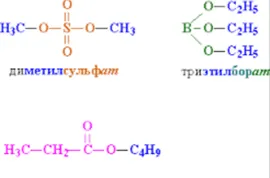
- Комплекс алкохолни естери на минерални киселини: сулфат (-SO3H) нитрат (-NO2) и други.
- Комплекс алкохол и карбоксилова киселина естери, например, S2N5SO-, S5N9SO-, SN3SO- и т. D.
Да разгледаме химични свойства естери. Етери имат ниска реактивност, поради това, те често се използват като разтворители. Те реагират само в екстремни условия, или високо реактивни съединения. За разлика Eterija, повече реактивни естери. Те лесно претърпяват хидролиза, осапунване и др ..
етери
Реакцията на етери с водородни халиди:
Повечето етери могат да се разлагат под действието на бромоводородна киселина (НВг) за образуване алкилови бромиди или чрез взаимодействие с йодоводородна киселина (HI) с polucheniemalkiliodidov.
СН3-О-СН3 + HI = СН3ОН + CH 3 I
СН3ОН + HI = CH3I + H2O
Образование оксониеви съединения:
. Сярна киселина, йод и други силни киселини чрез взаимодействие с етер за да се образуват съединения оксониева - продукти от по-висок порядък съединения.
СН3-О-СН3 + = HCl (CH3) 2О ∙ HCl
Взаимодействие етери с метален натрий:
При нагряване с неблагородни метали, например метален натрий, етери разделят на алкохолати и алкил натриев съединение.
СН3-О-СН3 + 2Na = СН3 ONa + CH3-Na
Автоокисляване на етери:
В присъствието на кислород, етери avtookislyayutsya бавно да образуват хидропероксиди idialkil пероксид. Автоокисляване е спонтанно окисляване на връзката на въздуха.
С2Н5-О-С2Н5 + O2 = СН3-СН (ООН) -О-С2Н5
естери
Хидролиза на естери:
В кисела среда хидролиза естер за образуване на съответната киселина и алкохол.
СН3 -СОО-С2Н5 = СН3 COOH + H2O
Осапунването на естери:
При повишени температури естери реагират с водни разтвори на силни основи, като натриев или калиев хидроксид, за да образуват соли на карбоксилни киселини. Соли на карбоксилни киселини zhrnyh наречени сапуни. алкохол страничен продукт е реакция на осапунване.
СН3-COO-С2Н5 + NaOH = SOONa СН3 + С2Н5-ОН
pereesterefikatsii реакция (обмен):
Естери влизат в обменни реакции под действието на алкохол (алкохолиза), киселина (ацидолиза), или чрез двойно обмен чрез реакция на два естери.
СН3-COO-С2Н5 + С3Н7-ОН = СН3-СОО-С3Н7 + С2Н5-ОН
СН3-COO-С2Н5 + С3Н7-СООН = С3Н7-COO-С2Н5 + CH3 СООН
СН3-COO-С2Н5 + С3Н7-СОО-СН3 = СН3-СОО-СН3 + С3Н7-COO-С2Н5
Реакция с амоняк:
Естерите могат да взаимодействат с амоняк (NH3) за образуване на амид и алкохол. По същия начин, те реагират с амини.
СН3-COO-С2Н5 + NH3 = СН3-CO-C2H5-NH2 + ОН
редукция Естер
Естерите могат да бъдат намалени с водород (Н2) в присъствието на меден хромит (Cu (CrO2) 2).
СН3-COO-С2Н5 + 2Н2 = СН3-СН2-С2Н5-ОН + ОН