Гипс - знаете как
РАЗДЕЛЯНЕ НА МИНЕРАЛИ със слоеста структура. Група мазилка.
От тази група, ние смятаме, само мазилката - Са [SO4] x2N2 О. гипс - старата гръцкото име за този минерал (гръцки gipsos -. Креда, гипс).
Кристална система - моноклинна форма симетрия - призма - С 2h - 2 / m (L2 PC). Структурна единица клетка съдържа 4: a0 = 5,68, б 0 = 15.18; 0 = 6.29; 0 = 113 ° 50 пространствена група "- С6 2h - A2 / а.
Кристална гипс обикновено слоеста структура. Два листа анионните групи [SO4] 2_. тясно свързани йони (фиг.) форма двойни слоеве него, ориентирани по (010) равнина. Mole Кула H2O се поставят между двойни слоеве. Калциеви йони са заобиколени от шест кислородни йони, принадлежащи към групи SO4. и две водни молекули. Всяка молекула на водните асоциирани с един йон Са йони кислород, разположена в същата двоен слой, а другата кислороден йон, който е съседен слой. Отцепването равнина гипс преминава между слоя H2O - Н2 О, успоредна на него.
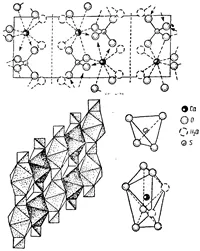
Кристалната структура на гипс
Агрегати и хабитус. Гипс образува мрамор-твърда маса, венозна конгестия, както и единични кристали и друзи. Виж неговите кристали обикновено са с плоска форма, колонен и игла (Фигура 2). Кристали почти винаги се наблюдават самолета (010), която е успоредна на много перфектен разцепване. Основните плоча навик кристални форми и ръбове са призми, и (1 10) има формата на подчинен значение. поява колонен форма obuslo на развитието на призматични страни, съединени с pinacoid, призматична същото лице и са по-чести. Ако кристалите са удължени по [001] или [111], навика на иглата. Трябва също да се отбележи, изометрични или по-скоро лещовидна кристали, разработени специално в глинени образувания. Тези кристали се характеризират и изпъкналата страна на призмата. Двойки гипс са по-чести, отколкото обикновените хора. Plane е туининг равнина pinacoid на (100) (галските колеги) или (101) (Париж колеги, фиг.3). Галски колеги обикновено се простират по протежение на третата ос. Също така добре развита повърхност, и те също имат колеги (111) равнина. Характерна особеност на Париж близнаците е неравно развитие на всички кристали. Fusion Е в единия край, с изключение на наблюдавания pinacoid равнина, а в другия край на призмата и само развити.
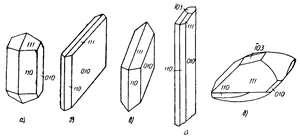
Навик гипсови кристали: А - колонен, - една плоча, а - таблични, R - на иглата, и т.н. - Изометричните
Самолет и рядко са изрично, по-често те са закръглени. Двойки гипс често е под формата на опашка лястовици, във връзка с които са получили подходящо име. Разграничаване кристален, влакнест, зърнести и трудна разлика гипс. Фиброзен разлика полупрозрачни гипс, наречен селенит. -Прецизен разлика наречена алабастър и пясъчен - poikilitic гипс. Стави могат да се образуват кристали от гипс гипс рози.
Физични свойства. Цвят бяла мазилка; vodyanoprozrachnye понякога единични кристали. P Rimes оцветени мазилка в различни цветове.
Gloss стъкло перлен на самолети разцепване. Разцепване е съвсем добра в (010) ясно от (100) и (011). Conchoidal фрактура. Tverdost- 1.5-2 (надраскани с нокът). Гъвкава, но не и еластична. Плътност на застрояване - 2,32. Оптични свойства: двуосна, положителен; нг = 1530, пт = 1528, PR = 1520, нг - PR = 0.010; 2V = 58 °.
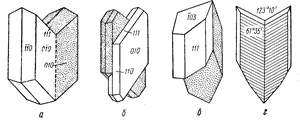
Двойки мазилка: а, б - на Галската закона, г - Закона Париж
Диагностични характеристики на гипс - перфектно разцепване на (010) и ниска твърдост. Основната линия на рентгенови лъчи: 3074; 2075; 1890. Той се разтваря в НС1, частично във вода (една част от гипс, две части вода). Най-високата разтворимост е при температура 37- 38 ° С при температури над 107 ° С се намалява разтворимостта на гипс. P. стр. М. И разцепен кондензиран в бяло емайл. На въглерод в намаляване на пламъка дава CAS. Кривите гипс отопление (има три реакции: 1) при 80-90 ° С, когато определено количество Н2 0 се разпределя; 2) при 140 ° С, когато гипсът да продължават полухидрат, и 3) при температура 140-220 ° С, когато има пълно отделяне на вода. При температура 400 ° С печен гипс е здраво.
Образованието и депозити. Гипсът е типичен морски химически утайки и пада, когато сухите помещения. Проучванията показват, че гипс се освобождава от водни разтвори при температури под 63 ° С (при по-висока температура се образува анхидрид). В присъствието на натриев хлорид температура разделяне гипс намалява. Гипс обикновено се намира под формата на голям резервоар утаечни образувания заедно с варовик, мергел, глина и пясък, най-големите натрупвания са известни във връзка с пермските и триаски утайките. Гипс хидратация възниква като анхидрит и като вторичен продукт на сяра и минерална сяра окисление. Установено е, освен това, като материалът се отлага повторно в хидрохимичните реакции.
Най-широко използвани и са важно отлагания, образувани в резултат на химически утаяването на гипса от морска вода. В тези случаи мазилката се освобождава по време на сушене otshnurovannyh морски зони и попада в първия стадий на изпаряване докато разтворът е все още не е достатъчно насища с натриев хлорид и други соли; анхидрид се образува по-късно. а по-късно Халите. Известен също гипс остава в вулканични региони, в които тя се появява около фумароли и solfataras чрез действието на сяра пара и вода калциеви съдържащи минерали. Гипсът е във връзка с анхидрит, Халите, кизерит и други солни депозити минерали.
Големи находища на гипс на западния склон на Урал, в Кама, Поволжието, в Artemovskaya басейн в Донбас, както и в Приднестровието (Лвов и региона Ивано-Франковск). Известни pseudomorphs на калцит от гипс, анхидрит и Халите. Намерено на гипсови pseudomorphs на халцедон, опал, кварц, калцит, арагонит, celestite, малахит и анхидрит.
Практическото значение. Печен гипс се използва като материал за циментови и гипсови творби, медицината и др. Г. в суров вид, тя се използва за производството на изделия (гипс) и като тор. Венозна и гъста гипс разлика са декоративен камък.
Препратки. Betehtin А. Г. курс на минералогията. Gosgeolgehizdat, 1961 Budnikov П. мазилка и му изследвания. Издателство на СССР академия на науките, 1933 Лазаренко Е, К. Лазаренко EA Баришников EK Malygina ОА Минералогия Transcarpathia. Издателство на Лвов университет, 1963.
По принцип, това е също търсят.