Cure мускулна дистрофия тип Дюшен
Конкуренция групи единство методологии
Мускулна дистрофия тип Дюшен - сериозно Х-свързана болест, ефективно лечение все още не. В последния брой на науката излезе в продължение на три статии за успешното тестване в миши модели CRISPR технология / Cas9 за лечение на това заболяване. Може би този подход има шанс да се изправи и клиники?
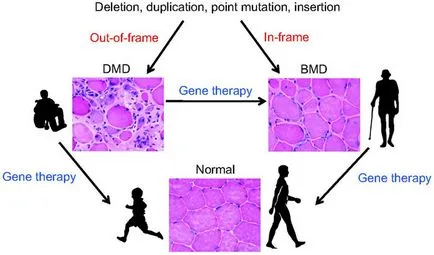
Принципът на генна терапия за мускулна дистрофия на Дюшен / Becker. Мускулна дистрофия на Дюшен (DMD) генни мутации причиняват дистрофин (DMD), което води до промяна в рамката за четене, и по-мек Бекер мускулна дистрофия (BMD) - мутацията без изместване на рамката на четене. Лечението на това заболяване все още. Генна терапия може да помогне за подобряване или дори се възстанови функцията на мускулите. Фигура [17].
Мускулна дистрофия на Дюшен, който страда от един от мъжки новородени 3600-5000, причинени от липсата на дистрофин - протеин, който свързва цитоскелета и извънклетъчната матрица в мускулните влакна и осигурява неговата стабилност при редуциращи (Фигура 1.). Поради генни мутации DMD в превод четяща рамка се поставя до синтеза на иРНК и протеин преждевременно прекратяване. Вродена заболяване прогресира много бързо: той се диагностицира на възраст от около четири години, а на 10 години на детето обикновено е вече нужда от инвалидна количка. Това е така, защото без дистрофин влакна са повредени, и веднага след като възможностите за възстановяване на мускулните влакна е изчерпана, те се заместват с фиброзна и мастна тъкан [1]. Проучванията показват, че когнитивните функции на детето също могат да бъдат нарушени. [2] За повече от 30 години с болестта, като правило, не живеят и умират от сърдечни и респираторни усложнения. В по-мек тип мускулна дистрофия, свързана с DMD ген - е Бекер мускулна дистрофия, където мутацията не води до промяна в рамката на четене [3].
Дистрофин се намира на вътреклетъчния повърхността по цялата дължина на сарколемата на мускулните влакна и част от дистрофин-свързан гликопротеин комплекс (DAGK, DGC). Той се свързва в единия край с F-актин цитоскелет, а другият - с β-distroglikanom че стабилизира влакната по време на рязане. Дистрофинът ген - един от най-дългите в хората.
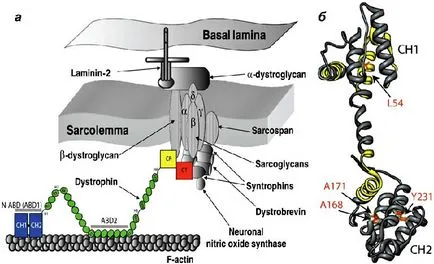
Фигура 1. мутации в дистрофин - причина за мускулна дистрофия на Дюшен.
и - Дистрофин свързва към актинови филаменти (част от цитоскелета) между домейни и N-АБД ABD2) и DAGK различни домейни CR и CT.
б - кристалната структура на N-АБД дистрофин. актин-свързващ зони са показани в жълто, четири добре характеризирани мутации, които причиняват заболяване - червено. Фигура [18].
Cure мускулна дистрофия тип Дюшен не знам колко време, а днешните терапии, насочени към забавяне на прогресията на заболяването и лечението на усложненията [4, 5]. "Златният стандарт" - е кортикостероиди, които са предложени за лечение на преди няколко десетилетия. Въпреки това, тяхната употреба предизвиква много странични ефекти.
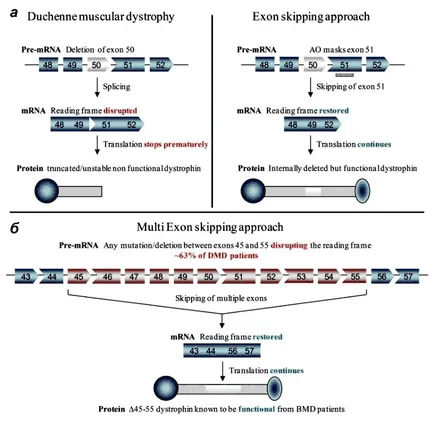
Фигура 2. Екзон пропускане в гена на дистрофин с мускулна дистрофия на Дюшен.
и - При пациенти с ДМД ДМД генни мутации са налични, които нарушават четящата рамка на протеиновия синтез. Например, когато заличаване на екзон 50 иРНК показва "vneramochnaya", което води до синтеза на пресечен нефункционален или нестабилна дистрофин (вляво). В един безсмислен олигонуклеотид терапевтичен подход "маски" екзон 51, и това е "пропуснал" по време на снаждане, рамката на четене е възстановена. Резултатът е по-кратък, но функционален дистрофин част (вдясно). Новите работни "екстра" екзони просто изрязват от генома, като се използва CRISPR / Cas9.
б - multiexon премине в лечението на мускулна дистрофия на Дюшен. Ако упражнение пропускане екзони 45-55, които мутации се срещат в приблизително 63% от пациентите, полученият кратко дистрофин води до превръщането на стандартен DMD фенотип в асимптоматични или мек BMD-фенотип. Фигура [19].
Ние имаме стратегия за отстраняване на екзони предимства пред дори пресъздава ген пълнометражен: тя е по-лесно да се развива от индивидуални изтривания възстановяване на всеки пациент [7].
За да се намали "допълнителни" нуклеотидни последователности, изследователите използват технологията CRISPR редактиране геном (клъстерирани редовно застъпени къси палиндромни повторения) / Cas9 (CRISPR-асоцииран протеин 9) * [9], който, между другото, е просто оставя да се използва в експерименти с ембриони, един от Лондон институт [10].
Конкуриращите Лаборатория: кой ще олицетворява първата технология в терапията за хората?
Учените три лаборатории успешно прилагат ин виво екзон пропускане технология на стандартен обект - мишки - и показаха, че техния метод помага за възстановяване на четящата рамка и за частично възстановяване на дистрофин. Тъй като дори ниско ниво (3-15% от нормата) терапевтична полза, резултатите може да се счита за успешна.
В последния тяхната работа за провеждане на необходимите компоненти за редактиране в тъкан адено-свързан вирус-9 (AAV9, адено-свързан вирус-9) [6]. Учените изследват няколко начина AAV9 администрация в различни дни след раждането на кученца. Във всички случаи, изразът на ген дистрофин в сърцето и скелетните мускули е възстановен, но в различна степен. Освен това, производството на протеин се увеличава от 3 до 12 седмици след инжектирането, и 4 седмици след инжектирането за подобряване на функцията на скелетни мускули. "Предизвикателството сега за учените от центъра Wellstone е да се съберат на откриването на миши модел на пациенти с тип Дюшен," - казва Pradeep Mammen (Pradeep Mammen), ко-директор на центъра Wellstone.
Изпълнител Amy Uadzhers провежда подобен експеримент в много отношения [8]. След много подготвителни етапи на работа по редактирането на генома и пропускане на екзони на клетки и животни от техния опит, също е успех: програмируеми CRISPR-комплекс, състоящ се от адено-свързан вирус (AAV) са били доставени с помощта на местно и системно прилагане на диференцирани скелетни влакна, кардиомиоцитите и сателитна мускулните клетки новородени и възрастни мишки. Ако редактиране се отнася само до мускулните влакна, след това с течение на времето ефект може да дойде до нула. Въпреки това, както е отбелязано Uadzhers гени редактиране чрез сателитни клетки може да осигури много по-дълъг резултат. Това може да доведе до създаването на пул от клетки, носещи регенеративни редактирана гена на дистрофин, и в резултат на нормална мускулна ремонт ген ще бъде редактиран в мускулните влакна.
Лечение на мускулна дистрофия тип Дюшен: стари и нови подходи
Според Olson, основната разлика между новата стратегия с помощта на вектор, съдържа компонент за редактиране на генома на други терапевтични методи с това, че премахва причината на заболяването. Какви други подходи учени разработват?
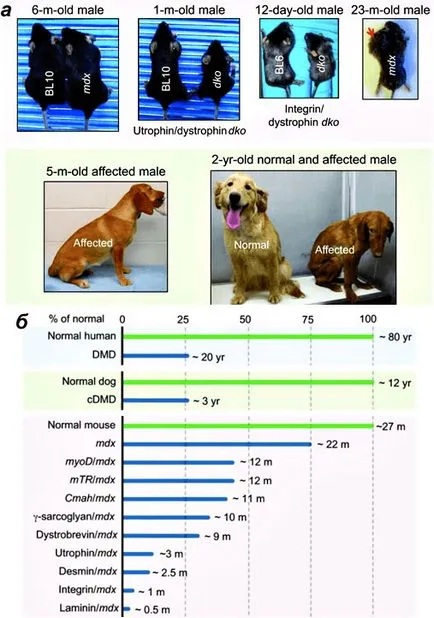
Фигура 3. Животински модели на мускулна дистрофия на Дюшен.
и - Проявите на мускулна дистрофия на Дюшен при мишки и кучета. Горе: MDX симптоми мишки се появяват само в напреднала възраст, и те са склонни към рабдомиосарком - тумори на мускулната произход. Размер мишки с генни нокаут utrophin / дистрофин интегрин и / дистрофин значително по-малко отколкото на съвпадение див тип (BL10 и BL6). По-долу: Проявите на болестта имат петмесечен болно куче. Разликите между здрави и болни кучета двугодишен.
B - Сравнение на продължителността на живота на здравите и болните хора, кучета, както и различни видове мишки. Фигура [17].
Други изследвания показват, че възстановяването на нормалните нива на синтеза на азотен оксид (NO), който се редуцира при пациенти поради нарушение активност NO-синтаза (nNOS), намалява възпалението увеличава автоложни стволови клетки активност и реконструира морфология и скелетна мускулна функция [3].
Още през фаза II на клинични изпитвания е препарат Givinostat - инхибитор на хистон деацетилази, който забавя развитието на болестта в миши модел.
Характеристики: "прокариотна система имунитет ще ви помогне да редактирате геном";
биомолекули: «CRISPR-система: имунизационни прокариоти";
биомолекула "мутагенни верижна реакция: редактиране геноми на ръба на фантазия";
биомолекули: "Не целим удар в. промяна в генома ";
биомолекули "болестта на Алцхаймер: ген, от който съм луд";
биомолекули: "Как да се запишете тринадесети? (Перспективи лечение на болестта на Хънтингтън) ";
Прочетете статии по темата:
Грешка в текста?
Изберете го и натиснете Ctrl + Enter
Прочетете също така:
Учените близо до втвърдяване слепота използване на генна терапия
Генна терапия на ретинитис пигментоза
Bioengineers медицински център Cedars-Sinai чрез CRISPR / Cas9 система излекувани плъхове ретинитис пигментоза - опасно наследствено заболяване, което води до слепота.
Генна терапия възстановява имунитета при тежки вродени аномалии
Нов метод за генна терапия, дава възможност за актуализиране на имунната система на деца и млади хора с Х-свързана форма на тежък синдром на комбиниран имунодефицит - наследствено заболяване, което засяга предимно мъжки бебета.
Генна терапия на Wiskott-Aldrich: първите успехи
Според данните, представени на Американското дружество по хематология, четири момчета с редки наследствени заболявания, след лечение се наблюдава значително подобрение в здравословното състояние.
Редакция на човешки гени: не бързайте!
Участниците в срещата на върха на водещи учени от Великобритания, САЩ и Китай, преждевременно въвеждане на технология за редактиране на ген бебето преди раждането се считат.
Удостоверение за регистрация El брой FS 77-35618