Азотните торове - блог за самостоятелно туризъм
От изхода на азотни торове са разпределени. Растения метаболизират предимно азот, свързан с други елементи. Въпреки това, тези съединения са много малко в природата и са разположени главно в Чили (Чили селитра). Чилийски нитрат преди началото на XX век е единственият източник на азотни торове. Основни азот резерви са съсредоточени във въздуха на практика не се абсорбират в свободно състояние и растенията. Следователно, същността на производството на азотни торове създава изкуствени съединения, които лесно се абсорбират от растенията. свободен азот съединение с други елементи извършва синтетично с водород до образуване на амоняк, което е основа за производството на различни азот-съдържащи продукти :. торове, азотна киселина, багрила, експлозиви, пластмаса, химически влакна и т.н. По този начин, за производството на азотни торове освен азот изисква основно водород.
Азотът получен от въздух. Първоначално той се втечнява и се диспергира в фракции. По този начин, азот като елемент на въздух с най-ниската температура на кондензация и на кипене (-196 ° С) преминава от течно към газообразно състояние на първия, и всички други елементи остават в течността. В настоящите процеси на азот от въздуха се получава директно, без дестилация.
Първо амоняк от водород и азот, се синтезира в немски химик F.Geberom 191Z През 1918 г. беше Нобелова награда за химия се присъжда "за синтез на амоняк от елементите." Изследванията му позволи да извършва първият промишлен синтез на амоняк в BASF растения.
Амоняк има остър мирис, което води до чувство на човек в безсъзнание. Въпреки това, той вдишване на големи количества води до виене на свят, болки в стомаха, задушаване. Максимално допустимата концентрация на амоняк в работните помещения 20 мг / куб.м.
по-трудно за задача - производство на водород. Производствените разходи съставляват по-голямата част от разходите за торове. водородни източници са по-ограничени географски от азот. Те са тези, които определят разположението на предприятия азотни торове промишленост.
Водородът от въглища кокс, произведен в регенеративни пещи. Когато това се пропуска през подаване на въздух пара. Последно разлага на кислород и водород. атмосферен кислород и вода, за да се окисли форми гориво въглеродни оксиди, смесени с азот и водород. Газовата смес се прекарва през абсорбер (вода). Въглероден диоксид се разтваря в нея и остава чист водород и азот. В този случай, I М амоняк консумира около 4 тона кокс до 9 или на кафяви въглища, което определя високата консумация материал и производство на азотни торове фирми териториално ориентация на въглеродни басейни. Трябва да се отбележи, че преди 60-те години. XX век почти всички торове, получени от коксов газ, въглища, кокс и азотни торове промишленост имат сурова ориентация.
Значителни ресурси са концентрирани водород във вода. Хидролиза на вода технологично относително прост разлага на водород и кислород. Това обаче изисква значителни разходи за енергия и разходите за мазнините е висока. Съгласно тази конструкция, производство на водород е създадена през Chirchik (Узбекистан) на базата на евтини електрическа енергия местните каскада ВЕЦ. На този етап, основен източник на водород в продължение на азотни торове - природен газ. Готови амоняк, което струва много по-малко от произведени от кокс, въглища и кокс газове. Развитие на газопреносна мрежа ще създаде тор освобождаване не само в близост източник на суровини, но и в районите на потребление на вносни суровини (Гродно). Това направи компании по-рационално разпределение. Първоначално синтез на амоняк се провежда чрез смесване на водород и азот, получен отделно.
Преобразуване - дума от латински произход и означава "промяна". В настоящия етап азотна смес се получава директно от суровини (метан) и въздух в един поток, без предварително изолиране освен азот и водород.
Метод схема производство амоняк включва около 30 единици. Природният газ се пречиства мивки (активен въглен, желязо, сода маса) на серни съединения и се смесва с пара и след въздух. Сместа се подава в реактора, където превръщането на метан с кислород въздух и вода в присъствието на никелови катализатори. Така химични реакции възникват:
Азотният смес се изчиства от кислород, оксиди на водни разтвори на натриев хидроксид въглерод, карбонати и течен азот в течно състояние се подава в колоната за синтез. Това е основната производствена единица. Тя има цилиндрична форма с диаметър от около 3 m и 20 м височина и изработени от отливка хром стомана с дебелина на стената до 20 см. Тук, при температура от около 500 ° С и налягане от 3000 атмосфери в присъствието на катализатор (желязо, волфрам, манган, и т.н.) е оформен течен амоняк. Нереагиралият азотна смес се отделя чрез разделяне на амоняк и се подава към ресинтез. В I R амоняк консумират до 900 кубически метра газ 1200 кВтч. електрическа енергия над 300 кубически метра вода.
Амонякът може да се получи от калциев карбид, който реагира с азотния атом образуват калциев цианамид. Последно лесно се разгражда с вода до образуване на крайния продукт и калциев карбонат:
калциев цианамид, може да се използва като тор на азот. Въпреки това, производството на калциев карбид - енергоемък процес и амоняк има висока цена.
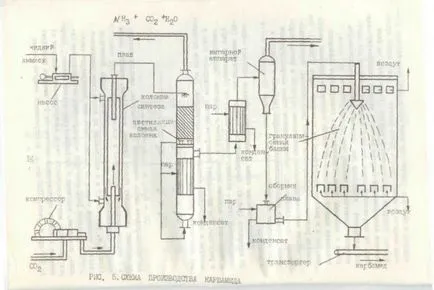
Урея продукция синтез на амоняк с въглероден диоксид. Синтезът се извършва в специални колони за да се образува разтвор урея
което се изпарява, кристализира или таблетирана. През I R урея консумират 0,6 тона амоняк, 0.8 тона въглероден диоксид.
Един от най-често срещаните видове торове - амониев нитрат, който съдържа 35% азот. Той се получава чрез взаимодействие на азотна киселина с амоняк в реактора или конвертори. В първия случай, разтвор нитрат
това се изпарява и се гранулира за разпространение на капки при специални кули. В реактора произвеждат по-концентриран сплав, която се гранулира без допълнително uparki. Следователно опростен процес Схема където методът. В т нитрат прекарват 0.21 тон амоняк, азотна киселина от 0.78 m.
амониев сулфат се получи чрез взаимодействие течен амоняк със сярна киселина в специален апарат (насищане) или газообразен амоняк с киселина спрей сух метод в специални камери;
По принцип амониев сулфат, получен като страничен продукт при пречистването на коксов газ, в производството на капролактам. На I т консумира сулфат 0.27 тон амоняк и 0,75 тона сярна киселина.
Така, производството на азотни торове се характеризира с ниска консумация на амоняк и киселини. Въпреки това, разходите за суровини, разходите за производство са значителни. Следователно, производството на различни видове азотни торове се комбинира с генерирането на амоняк, азотна киселина.